看到氢化可的松注射液的辅料里有乙醇和注射用水,想扣除辅料干扰就得配制相应浓度的辅料,谁能透露下,这处方里头的乙醇大概浓度多少啊? 叩谢各位大大。
5-单硝异山梨醇酯检查时HPLC的问题5-单硝异山梨醇酯注射液检查有关物质时,色谱图在溶剂峰处有时会出现一个很大很尖的峰,有时又没有,有做过的来讨论一下。有时含量测定时也会出现。是5-单硝异山梨醇酯分解产物吗?困惑。
【中国药典】从1985年版至1995年版均采用显微镜法检查注射液中的不溶性微粒。检查≥10μm与≥25μm两档,与美国药典标准基本相同。在2000年版【中国药典】显微镜法检查注射液中不溶性微粒的基础上增加了第二法----光阻法。在2005年版【中国药典】中增加了对小剂量注射液的检测。【中国药典】2005年版初稿对注射液中不溶性微粒污染的监控作了修订,将光阻法修订为第一法,显微镜法为第二法。修订后的结果判定也与美、英、欧共体、日本基本一致。原文来自:http://pssnicomp.cn/zhuanti.html
2010版药典中盐酸利多卡因注射液含测项下结果乘以1.156是什么意思,这个数据是根据什么公式得来的呢?
注射液是常用的药品之一,而且因其药效迅速、作用可靠,正越来越广泛地应用于临床。因注射液直接进入血液,对其无菌性的要求非常高,《中国药典》规定,注射液中不应含有任何活的微生物,这就需要抗氧剂来帮忙。那么在注射液中常用的抗氧剂 有哪些?
甘露醇注射液含量检测测出倒峰,水为流动相,如何解决出倒峰问题[img=,690,920]https://ng1.17img.cn/bbsfiles/images/2021/07/202107271704099598_9643_3978275_3.png[/img]
【序号】: 1【作者】: 徐燕 兰婉玲 傅超美 何瑶【题名】: 甘露醇及甘露醇注射液有关物质检查的研究【期刊】: 成都医学院学报【年、卷、期、起止页码】: 2008年3期【全文链接】:帮你编辑了,下次请注意一下!
想配制一个不含主药成分的注射液空白,看了下某注射液的辅料,为丙二醇,但没写浓度。有人告诉我大概就按照1%~10%的浓度配制这个辅料溶液就可以了,但我一估算,主药成分是10ml:0.1g,相当于1%的浓度。想不到名为辅料,这个浓度居然跟主药浓度相当甚至还超过啊,所以有点吃不准,特来请教各位老师,还望赐教。
单位新装了安捷伦液相,带示差折光检测器,我们就试着按药典标准走了甘露醇注射液但是光是系统适用性就不行,甘露醇和山梨醇的分离度达不到2.0的标准,而且第一针都是快可以的样子,第二针以后峰型就全塌了,分离度,塔板数都不可以了,第二针后的重现性倒是很好,都差不多工程师就是怀疑是柱子的问题,但是我们换了柱子,也确认了借来的柱子没问题现在完全不知道怎么办了,大家有什么经验么
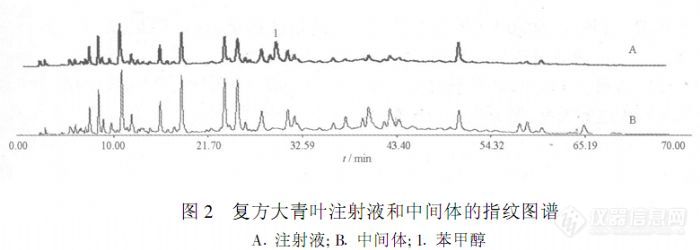
【作者中文名】刘瑞; 刘志刚; 李磊; 任冲; 袁波; 李发美;【作者英文名】LIU Rui; LIU Zhi-gang; LI Lei; REN Chong; YUAN Bo; LI Fa-mei(School of Pharmacy; Shenyang Pharmaceutical University; Shenyang 110016; China);【作者单位】沈阳药科大学药学院; 沈阳药科大学药学院 辽宁沈阳; 辽宁沈阳;【摘要】目的:采用HPLC建立复方大青叶注射液的指纹图谱测定方法。方法:采用Diamonsil C18色谱柱,甲醇-水-磷酸为流动相进行梯度洗脱,流速1.0 mL.min-1,检测波长254 nm。结果:建立了复方大青叶注射液的HPLC对照指纹图谱,标示了注射液中的20个共有峰,并初步确定注射液的相似度阈值为0.85。结论:该方法准确、重复性好,为复方大青叶注射液的质量控制提供了依据。http://ng1.17img.cn/bbsfiles/images/2012/08/201208131758_383604_2379123_3.jpg
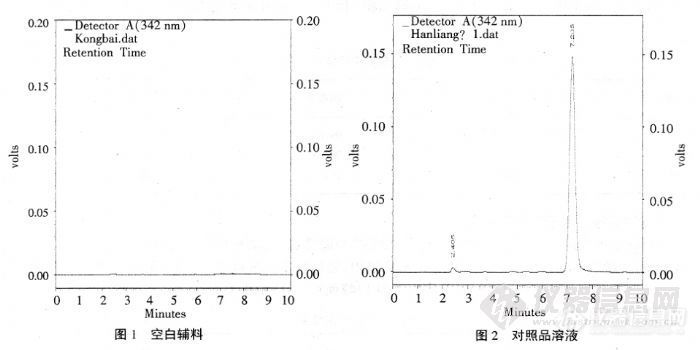
标题:5.1 甲钴胺注射液含量的方法学研究作者:常 明 1, 李 晶 1, 武玉洁 2, 张文双 2( 1.石家庄学院 化工学院, 河北 石家庄 050035; 2.石家庄栢奇制药有限公司, 河北 石家庄 050035)摘要: 摘 要: 以乙腈- 甲醇- 0.05 mol /L磷酸二氢钾溶液( 10∶ 20∶ 70) (用磷酸调节 pH 值为 4.0)为流动相, 采用迪马钻石 C18( 250 mm× 4.6 mm, 5 μ m)色谱柱及紫外检测器, 建立了甲钴胺注射液中甲钴胺含量的反相高效液相色谱检测方法. 柱温: 40℃; 检测波长为 264 nm; 流速: 1.0 mL /min. 本方法测定的日内精密度为 0.59%, 日间精密度为 0.67%, 回收率为 99.7%~ 100.5%, 在 160~ 240 μ g /mL范围内线性关系满足要求( r=0.999 9) ; 结果表明方法准确、 操作简单、 专属性强, 可用于定量测定甲钴胺注射液含量.http://ng1.17img.cn/bbsfiles/images/2012/07/201207161648_377914_2379123_3.jpg
我测的是注射液里的钠,钾,铯,可是注射液里有葡萄糖和枸橼酸,是不是必须硝化啊,硝化的方法在那里着找啊,我是新手,忘各位前辈指点指点。我在一些专利网上没有查到。
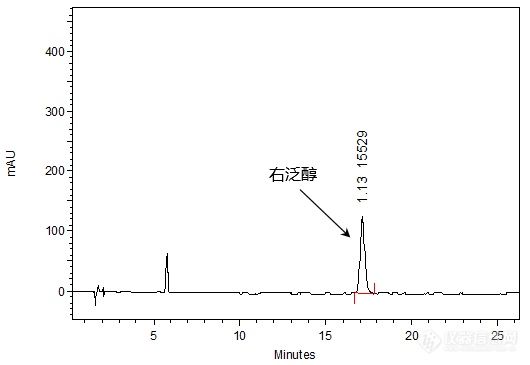
[align=center][b]BP 2015方法|复合维生素注射液的定量分析(2)[/b][/align][align=right][b]——右泛醇的分析[/b][/align]接上回的数据,客户提供了复合维生素注射液及右泛醇对照品溶液,希望本实验室参考BP 2015英国药典方法,选择合适的色谱柱对注射液样品中的右泛醇进行定量分析。依据BP 2015方法,流动相为0.01M磷酸氢二钾:甲醇(96:4),为高水相条件,且对流动相pH值进行测定发现该流动相条件为[color=#ff0000][b]pH 8.6的强碱性条件[/b][/color],若使用普通C[sub]18[/sub]色谱柱进行分析,势必会影响其[color=#ff0000]使用寿命[/color],因此,本实验室使用大阪曹達的聚合物包被型[b][color=red]耐碱性色谱柱CAPCELL PAK C[sub]18[/sub] BB[/color][/b],首先对右泛醇对照品溶液进行分析,如图1,[color=#3333ff]右泛醇主峰保留时间约为17 min,理论塔板数为15529,拖尾因子为1.13,能得到良好分析结果。[/color][align=center][img=,185,65]http://ng1.17img.cn/bbsfiles/images/2018/06/201806290957497322_9243_2222981_3.gif!w185x65.jpg[/img][/align][align=center]右泛醇[/align][align=center]Dexpanthenol[/align][align=center]M.W. : 205.25[/align][align=center][img=,530,365]http://ng1.17img.cn/bbsfiles/images/2018/06/201806290957494372_7696_2222981_3.png!w530x365.jpg[/img][/align][align=center]图1 CAPCELL PAK C[sub]18 [/sub]BB分析对照品溶液所得结果[/align][align=left]*注:峰上标数字由下至上依次为拖尾因子和理论塔板数,下同。[/align][align=left][img=,548,203]http://ng1.17img.cn/bbsfiles/images/2018/06/201806290958389242_9808_2222981_3.png!w548x203.jpg[/img][/align][align=left][/align][align=left]接下来,在相同色谱条件下对复合维生素注射液样品进行分析,如图2,亦可得到良好分析结果。[/align][align=left][/align][align=center][img=,519,362]http://ng1.17img.cn/bbsfiles/images/2018/06/201806290958577052_8694_2222981_3.png!w519x362.jpg[/img][/align][align=center]图2 CAPCELL PAK C[sub]18 [/sub]BB分析供试品溶液所得结果[/align][align=left][img=,553,200]http://ng1.17img.cn/bbsfiles/images/2018/06/201806290958578512_6104_2222981_3.png!w553x200.jpg[/img][/align][align=left][/align][align=left]综上实验结果,使用大阪曹達的[b][color=red]耐碱性[/color][color=red]色谱柱CAPCELLPAK C[sub]18 [/sub]BB [/color][/b]S5 4.6 mm i.d. × 250mm,依据BP 2015英国药典方法,在35°C柱温条件下,能够实现复合维生素注射液中右泛醇的定量分析。[/align][align=left]结合上一份数据,使用大阪曹達的[b][color=red]能耐受纯水条件的高极性色谱柱[/color][color=red]CAPCELL PAK C[sub]18 [/sub]AQ[/color][/b] S5 4.6 mm i.d. × 250 mm,依据BP 2015英国药典方法,通过调整流动相中有机相比例,能够实现复合维生素注射液中维生素B[sub]1[/sub]、维生素B[sub]6[/sub]和烟酰胺及杂质的良好分离及准确定量分析。[/align][align=left]该实验也说明了[color=#3333ff]在进行液相分析时,色谱柱选择的重要性。[/color]只有选对色谱柱,才能在得到满意的实验结果的同时,保证色谱柱寿命和分析结果的稳定性。[/align][align=right] [/align][align=right] [/align][align=right]三耀精细化工品销售(中国)有限公司技术开发部[/align][align=right]地址:北京经济技术开发区宏达南路5号宏达利德工业园1栋418室[/align][align=right]邮编:100176[/align]
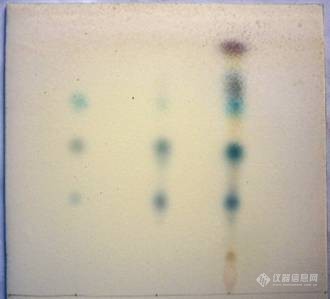
[align=center][/align][font=宋体]([/font]1[font=宋体])薄层色谱条件[/font][b] [/b] [font=宋体]薄层板:硅胶[/font]G[font=宋体]板[/font] [font=宋体]展开剂:[color=black]环己烷[/color][/font][color=black]-[/color][font=宋体][color=black]乙酸乙酯([/color][/font][color=black]17:3[/color][font=宋体][color=black],[/color][/font][color=black]V/V[/color][font=宋体][color=black])[/color][/font] [font=宋体]显色剂:[/font]5%[font=宋体]香草醛硫酸制乙醇溶液[/font][font=宋体]点样量:[/font]2 [color=black]μL[/color][font=宋体][color=black](对照溶液),[/color][/font][color=black]5μL[/color][font=宋体][color=black](供试品溶液)[/color][/font][font=宋体]([/font]2[font=宋体])对照溶液的制备[/font][font=宋体]分别取[/font]4-[font=宋体]萜烯醇、[/font]α-[font=宋体]松油醇和甲基正壬酮适量,精密称定,加正己烷配成浓度约[/font]1.0[font=宋体],[/font]0.5[font=宋体],[/font]10 mgmL[sup]-1[/sup][font=宋体]的储备液,[color=black]即得。[/color][/font][font=宋体]([/font]3[font=宋体])供试品溶液制备[/font][font=宋体][color=black]取鲜鱼腥草[/color][/font][color=black]125 g[/color][font=宋体][color=black]剪碎,照挥发油测定法《中国药典》[/color][/font][color=black]2020[/color][font=宋体][color=black]年版(四部),加正己烷[/color][/font][color=black]1 mL[/color][font=宋体][color=black],缓缓加热至沸,并保持微沸[/color][/font][color=black]4 h[/color][font=宋体][color=black],放置至室温,取正己烷层,定容至[/color][/font][color=black]2 mL[/color][font=宋体][color=black]作为药材供试品溶液。[/color][/font][font=宋体][color=black]取注射液[/color][/font][color=black]100 mL[/color][font=宋体][color=black],照挥发油测定法《中国药典》[/color][/font][color=black]2020[/color][font=宋体][color=black]年版(四部),加正己烷[/color][/font][color=black]0.5 mL[/color][font=宋体][color=black],缓缓加热至沸,并保持微沸[/color][/font][color=black]40 min[/color][font=宋体][color=black],放置至室温,取正己烷层,定容至[/color][/font][color=black]2 mL[/color][font=宋体][color=black],作为注射液供试品溶液。[/color][/font][font=宋体]([/font]4[font=宋体])[/font]TLC[font=宋体]鉴别法[/font][font=宋体][color=black]照薄层色谱法(《中国药典》[/color][/font][color=black]2020[/color][font=宋体][color=black]年版四部[/color][/font][color=black]0502[/color][font=宋体][color=black])试验,吸取上述供试品溶液[/color][/font][color=black]5 μL[/color][font=宋体][color=black]、对照品溶液[/color][/font][color=black]2 μL[/color][font=宋体][color=black],分别点于同一以羧甲基纤维素钠为黏合剂的硅胶[/color][/font][color=black]G[/color][font=宋体][color=black]薄层板上,以环己烷[/color][/font][color=black]-[/color][font=宋体][color=black]乙酸乙酯([/color][/font][color=black]17:3[/color][font=宋体][color=black],[/color][/font][color=black]V/V[/color][font=宋体][color=black])为展开剂,饱和后上行展开,将展开后的薄层板取出,晾干,喷[/color][/font][color=black]5%[/color][font=宋体][color=black]香草醛硫酸制乙醇溶液。烘干至斑点显色明显,在与对照品色谱相应的位置上,显相同的蓝色斑点,见图[/color][/font][color=black]1[/color][font=宋体][color=black]。[/color][/font][align=center][img=,330,299]https://ng1.17img.cn/bbsfiles/images/2021/10/202110091524352875_6989_3528941_3.jpg!w330x299.jpg[/img][/align][align=center][font=宋体]图[/font]1 [font=宋体]鲜鱼腥草和注射液薄层鉴别照片[/font][/align][align=center][font=宋体]点样从左至右分别为标准品、注射液、药材。[/font][/align]
近日有群友求助,群里尚未有人应答,现在版面上贴出,希望有人予以回应: 依据依######注射液处方,配制#####注射液作为制剂空白。精密量取B、Mg、Al、K、Ca、Cr、Fe、Zn、Ba、As、Cd、Pb、Co、Ti、Mn、Sb标准液适量于10ml量瓶中,用1%硝酸稀释至刻度,得对照储备液精密量取对照储备液适量于50ml量瓶中,加入制剂空白溶液10ml, 1%硝酸稀释至刻度,得系列浓度溶液。以含20%制剂空白的1%硝酸溶液为标准空白溶液。测定标准空白溶液和标准溶液系列,仪器自动绘制标准曲线。然后根据此线性进行样品测定,及方法学考察。不知这样的做法是否有不妥的地方?
多多药业有限公司生产的双黄连注射液被叫停。今天,国家食品药品监督管理局在其网站上发出通知,要求各地暂停销售使用标示为多多药业有限公司生产的双黄连注射液。 16日,国家药品不良反应监测中心报告称,标示为黑龙江多多药业有限公司生产的双黄连注射液在使用中出现严重不良事件。为确保公众用药安全,决定暂停销售和使用标示为多多药业有限公司生产的双黄连注射液。 目前,国家食品药品监督管理局和卫生部正在对该事件发生的原因进行调查。 大家对此事件如何看待的,有什么想法、看法、观点,说说,晒晒![em09502]
药典制剂通则中注射剂项下没有色泽均匀或一致的规定,如发现同批注射液色泽深浅不一、经检验均符合标准规定,如何下结论?
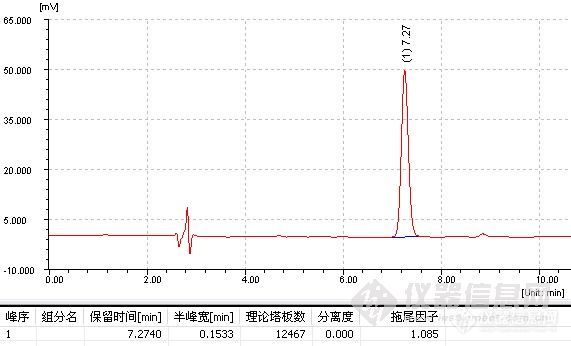
氟康唑氯化钠注射液的测定一.样品分子结构氟康唑分子结构:http://ng1.17img.cn/bbsfiles/images/2010/03/201003031435_203516_1896702_3.jpg二. 样品来源记录样品商品名:氟康唑氯化钠注射液 样品测定描述:主成分含量测定三. 液相方法条件方法来源:客户提供; 具体方法:色谱柱:Ultimate® XB-C18,5um,4.6×250mm,Ult090902P29; 检测波长:260nm ; 流动相:磷酸盐缓冲溶液:甲醇=55:45 磷酸盐缓冲溶液的配制:准确称量0.68g KH2PO4至于100ml容量瓶中,加入0.1mol/L 的NaOH溶液29.1ml,用水稀释至刻度(此时测得pH为7.59);温 度:室温20℃; 流 速:1.0ml/min; 进样量:20ul; 流动相的配制: 准确量取上述配制好pH 7.59的磷酸二氢钾缓冲溶液275ml和甲醇225ml,混合均匀,搅超声脱气,冷却至室温;样品处理方法: 取氟康唑氯化钠注射液1ml于10ml容量瓶中,用流动相稀释至刻度;注意事项: 1. 与客户提供方法完全相同; 2. 用流动相溶解样品; 3. 色谱柱的维护: 1)一天分析开始前,先用甲醇:水=40:60以1ml/min冲洗色谱柱30min,然后用流动相走基线,基线平稳后进样; 2)一天分析完成后,先用甲醇:水=40:60以1ml/min反向冲洗色谱柱40min,再用甲醇:水=90:10反向
在英国药典附录colour of solution中指描述了标准比色液的配制,但如果注射液正文中没有对颜色的描述,是否就表明对该品种的颜色不做要求呢?还是说没有描述就是要求澄清无色?药典的其他地方有没有溶液颜色的规定?请指点,谢谢!
利用[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法建立复方苦参注射液中7个成分(甲基氧化偶氮甲醇樱草糖苷、苦参碱、槐果碱、槐定碱、氧化槐果碱、氧化苦参碱、番石榴酸)的含量测定方法。采用Waters Xselect CSHTM C18色谱柱(250 mm×4.6 mm, 5μm),以甲醇-0.2%磷酸二氢钾为流动相,梯度洗脱,流速0.6 mLmin-1,柱温30℃,检测波长211 nm。测定的甲基氧化偶氮甲醇樱草糖苷、苦参碱、槐果碱、槐定碱、氧化槐果碱、氧化苦参碱、番石榴酸7个成分的平均加样回收率分别为95.7%、101.3%、100.8%、101.7%、102.6%、102.5%、99.5%,RSD分别为2.0%、0.72%、0.90%、0.74%、1.4%、0.96%、1.8% 10批次样品中7个成分的含量分别为0.53~0.73、2.66~4.22、0.75~1.11、0.70~0.89、2.20~2.84、7.62~9.95、1.63~2.20 mgmL-1。该方法稳定可靠,可为复方苦参注射液的质量控制与评价提供参考。详见王鹏飞等,药物分析杂志. 2022,42(07)
喜炎平脉络宁注射液引起严重过敏2012年06月27日08:47新华网国家食品药品监督管理局26日发布通报,提示生产企业和医患人员关注喜炎平注射液和脉络宁注射液引起严重过敏反应的问题。据了解,喜炎平注射液的成分是穿心莲内酯磺化物,主要用于解热消炎。2011年,国家药品不良反应监测中心病例报告数据库有关喜炎平注射液的病例报告数共计1476例,其中涉及14岁以下儿童报告达1048例。主要不良反应表现为过敏样反应、过敏性休克、紫绀、呼吸困难等。脉络宁注射液是2009版国家基本药目录品种,其功能与主治为清热养阴、活血化瘀。用于血栓闭塞性脉管炎、动脉硬化性闭塞症、脑血栓形成及后遗症、静脉血栓形成等。2011年,国家药品不良反应监测中心病例报告数据库共收到有关脉络宁注射液药品不良反应病例报告1500例,其中严重病例报告189例。严重不良反应主要为呼吸系统损害、全身性损害和心血管系统损害等。国家食品药品监管局建议,由于这两种注射液易发生过敏反应,建议医护人员在用药前详细询问患者的过敏史,特殊人群和过敏体质者应慎重使用。使用时应严格按照说明书规定的用法用量给药,不得超剂量使用;谨慎联合用药。如确需联合使用其他药品时,应谨慎考虑与此两种药品的间隔时间以及药物相互作用等问题。对于药品生产企业,国家食品药品监管局建议,加强临床合理用药的宣传,确保产品的安全性信息及时传达给患者和医生;完善生产工艺、提高产品质量标准,开展相应安全性研究。(新华网)
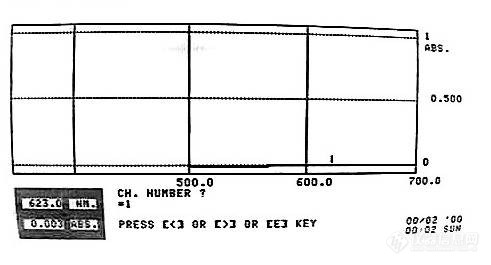
[align=center][b]鱼腥草注射液中增溶剂吐温80的限量测定[/b][/align][b]1 [/b][font=黑体]溶液的制备[/font][font=黑体]对照品溶液的制备[/font][font=宋体]取吐温[/font]80[font=宋体]对照品适量至[/font]100mL[font=宋体]量瓶中,精密称定,加重蒸水制成[/font]9.83 mgmL[sup]-1[/sup][font=宋体]的溶液。[/font][font=黑体]供试品溶液的制备[/font][font=宋体]精密移取鱼腥草注射液[/font]1mL[font=宋体]置[/font]100 mL[font=宋体]离心管中,加铵钴硫氰酸盐溶液[/font]15 mL[font=宋体](取硝酸钴[/font]6g[font=宋体],硫氰酸铵[/font]40 g[font=宋体],加水溶解并稀释至[/font]200 mL[font=宋体],摇匀,即得),精密加入二氯甲烷[/font]10mL[font=宋体],称定重量,置调速多用振荡器振荡[/font]30 min[font=宋体],取出,用二氯甲烷补足减失的重量,移至分液漏斗中,静置[/font]30 min[font=宋体],分取二氯甲烷层溶液,作为供试品溶液。[/font][b]2[/b][font=黑体]测定波长的选择[/font] [font=宋体]对照品溶液与供试品溶液经显色反应后,在[/font]400~ 700 nm[font=宋体]波长范围内分别进行扫描,结果发现吐温[/font]80[font=宋体]对照品溶液与鱼腥草注射液供试品溶液峰形一致,最大吸收波长一致,均为[/font]623 nm[font=宋体]。[/font][b]3[/b][font=黑体]方法学考察[/font] [font=黑体]专属性试验[/font][font=宋体]取空白溶液(水)、鱼腥草重蒸馏液(未加吐温[/font]80[font=宋体],作阴性对照)、对照品吐温[/font]80[font=宋体]、鱼腥草注射液照,按“供试品溶液的制备”项下方法显色后比较吸光度,结果在[/font]623 nm[font=宋体]波长处,空白溶液的吸光度为[/font]0.002[font=宋体],阴性对照溶液的吸光度为[/font]0.001[font=宋体],鱼腥草注射液和对照品均有较好吸收,表明鱼腥草注射液中其它组分对本试验测定结果无干扰,阴性对照溶液与空白溶液在[/font]623nm[font=宋体]波长处无吸收。见[/font]Fig.1[font=宋体]。[/font][align=center][img=,491,265]https://ng1.17img.cn/bbsfiles/images/2022/09/202209011436509666_4892_3527494_3.jpg!w491x265.jpg[/img][/align][align=center][b](A)[/b][/align][font='Times New Roman'][/font][align=center][img=,490,250]https://ng1.17img.cn/bbsfiles/images/2022/09/202209011437018380_6503_3527494_3.jpg!w490x250.jpg[/img][/align][font='Times New Roman'][/font][b](B)[/b][align=center][img=,490,267]https://ng1.17img.cn/bbsfiles/images/2022/09/202209011437115097_5280_3527494_3.jpg!w490x267.jpg[/img][/align][align=center] ([b]C)[/b][/align][align=center] [/align][align=center][img=,491,265]https://ng1.17img.cn/bbsfiles/images/2022/09/202209011437184190_6882_3527494_3.jpg!w491x265.jpg[/img][/align][align=center][b](D)[/b][/align][align=center]Fig.1 The ultraviolet spectra of the blank solution (A)[font=宋体]、[/font]negative control sample (B)[font=宋体]、[/font]tween80 control sample (C) and real sample (D)[/align][b] [/b][font=黑体]线性和范围[/font][font=宋体]精密量取吐温[/font]80[font=宋体]对照品溶液[/font]0.5[font=宋体],[/font]1.0[font=宋体],[/font]2.0[font=宋体],[/font]4.0[font=宋体],[/font]8.0[font=宋体],[/font]10mL,[font=宋体]置[/font]100 mL[font=宋体]离心管中,分别加入硫氰钴铵溶液[/font]15mL[font=宋体],精密加入二氯甲烷[/font] 10 mL[font=宋体],称定重量,置调速多用振荡器上振荡[/font][font=宋体](室温,[/font]88rpm[font=宋体])[/font]30 min[font=宋体],取出,用二氯甲烷补足减失的重量,移至分液漏斗中,静置[/font]30min[font=宋体],分取下层溶液,在[/font] 623 nm[font=宋体]波长处测定吸光度,以二氯甲烷为空白对照,以吸光度([/font][i]A[/i][font=宋体])对吐温[/font]80[font=宋体]对照品浓度([/font][i]C[/i][font=宋体])进行线性回归,绘制标准曲线,回归方程为[/font]:[i]A [/i]= 1.57×10[sup]-1[/sup][i]C[/i]+ 2.5×10[sup]-3[/sup][font=宋体],[/font][i]r[/i]= 0.9999[font=宋体]。结果表明,吐温[/font]80[font=宋体]在[/font]0.49 ~ 9.83 mgmL[sup]- 1[/sup][font=宋体]范围内与吸光度呈良好的线性关系。[/font][b] [/b][font=黑体]精密度试验[/font][font=宋体]取同一“供试品溶液的制备”项下的鱼腥草注射液供试品溶液,在[/font]623nm[font=宋体]波长下进行测定[/font]6[font=宋体]次,测定结果[/font]RSD[font=宋体]为[/font]0.4%[font=宋体],表明仪器精密度良好。[/font][font=黑体]重复性试验[/font][font=宋体]取同一批鱼腥草注射液[/font]6[font=宋体]份,按“供试品溶液的制备”项下制备供试品溶液,在[/font]623 nm[font=宋体]波长处测定,所测吐温[/font]80[font=宋体]含量的[/font]RSD[font=宋体]为[/font]0.5%[font=宋体],表明该方法重复性良好。[/font][font=黑体]稳定性试验[/font][font=宋体]取“供试品溶液的制备”项下的鱼腥草注射液供试品溶液,在[/font]623nm[font=宋体]波长下分别于[/font]0[font=宋体]、[/font]1[font=宋体]、[/font]2[font=宋体]、[/font]4[font=宋体]、[/font]8[font=宋体]、[/font]12h[font=宋体]测定吸光度,测定结果[/font]RSD[font=宋体]为[/font]0.5%[font=宋体],表明供试品溶液在显色后[/font]12 h[font=宋体]内稳定。[/font][font=黑体]回收率试验[/font][font=宋体]精密量取已知含量的鱼腥草注射液[/font]0.5mL [font=宋体]置[/font]100 mL[font=宋体]离心管中,共[/font]9[font=宋体]份,每[/font]3[font=宋体]份[/font]1[font=宋体]组,分别精密加入吐温[/font]80[font=宋体]对照品[/font]sd[sub]2[/sub][font=宋体]溶液[/font]1.1[font=宋体],[/font]1.3[font=宋体],[/font]1.6mL[font=宋体],按“供试品溶液的制备”项下的方法制备供试品溶液,在[/font]623 nm[font=宋体]波长下测定,测定吐温[/font]80[font=宋体]的平均回收率为[/font]99.2%[font=宋体],[/font]RSD[font=宋体]为[/font]0.4%[font=宋体]([/font][i]n[/i]=9[font=宋体])。[/font][b]4.[font=宋体]样品测定[/font][/b][font=宋体]精密移取各批鱼腥草注射液[/font]1 mL[font=宋体],置[/font]100mL[font=宋体]离心管中,按“供试品溶液的制备”项下进行显色反应,在[/font]623 nm[font=宋体]波长下测定吸光度。对鱼腥草注射液([/font]10[font=宋体]批)中的吐温[/font]80[font=宋体]含量进行了测定,其含量在[/font]1.44~ 2.50 mgmL[sup]-1[/sup][font=宋体]。[/font]
最近做葡萄糖酸钙注射液样品,发现总是有钙沉淀影响澄清度,请教大家如何解决啊
土霉素注射液用高效液相怎么检测?谢谢!
复方氨基比林注射液说明书(兽用)【兽药名称】通用名:复方氨基比林注射液 英文名:Compound Aminophenzone Injection 汉语拼音:Fufang Anjibilin Zhusheye【主要成分】为氨基比林与巴比妥混合制成的灭菌水溶液。含氨基比林7.15%和巴比妥2.85%。【性 状】本品为无色或淡黄色的澄明液体。【药理作用】本品给药后即时产生镇痛作用,其解热镇痛作用强而持久,氨基比林与巴比妥合用能增强其镇痛作用,有利于缓解疼痛症状。本品还有抗风湿和消炎作用。半衰期为1~4小时。【适 应 症】用于发热性疾患、关节炎、肌肉痛和风湿症等。【用法用量】 肌内、皮下注射:一次量,马、牛20~50mg;羊、猪5~10mg。【注意事项】连续长期应用可引起粒性白细胞减少症,应定期检查血象。【停 药 期】28日,弃奶期7日。【有 效 期】二年【规 格】10ml【包 装】10ml /支×5支/盒【贮 藏】遮光、密闭保存。
各位大侠: 按照药典方法测定乳酸钠林格注射液中氯化钠的含量,吸光度在0.1左右,线性很不好,同样样品,运行两次结果相差也很大,不知道是什么原因,希望能给予帮助,谢谢!!!!

ELSD法测定某种药注射液中吐温-80的含量前言:吐温80(Tweem80,聚山梨醇脂80),是一种非离子型表面活性剂。常作为增溶剂,乳化剂、分散剂或稳定剂广泛应用于食品和药品的生产。随着中药注射剂在临床上的广泛应用,含吐温80的中药注射剂经常出现一些不良反应,为控制中药注射剂中吐温80的含量,需要拥有准确快速的检测方法来保证产品的质量,保障临床用药安全。1.仪器与试药仪器:安捷伦1260高效液相色谱仪(四元泵,385蒸发光检测器)及色谱工作站万分之一电子天平(型号T-214 美国DENVER)十万分之一电子天平(型号TB-215 D 美国DENVER)KQ-5200超声仪试药:乙腈为色谱纯,水为纯化水,其余试剂均为分析纯对照品:吐温-80(批号:G01359 USP)样 品:某种药注射液批号: 20120206,20121002,20121012,20121119,20121132,20121203,20121234,20130109,20130134,20130202,20130314,20130501,20130506,20130517,201311062.含量测定方法学考察2.1色谱条件色谱柱:TSKgel G2000SWXL(7.8mm*300mm,5μm)及保护柱;流动相:20mmol·L-1醋酸铵一乙睛(88:12),流速:0.6mL·min-1;柱温:30℃;ELSD检测条件:蒸发器温度80℃,雾化器温度60℃,氮气流速2L·min-1;进样量:对照品溶液10μL与[
中药注射液的前途渺茫还是?大家说说看[em0801]
中药注射液,确切的说我要做香丹注射液的重金属及有害元素检查,可以制剂取10ml加5ml置赶酸仪中130°,加热至近干,就稀释等上机做可以吗?

【作者】 马琳; 李勇军; 何迅; 兰燕宇; 王爱民; 王永林;【Author】 Ma Lin,Li Yongjun,He Xun,Lan Yanyu,Wang Aimin,Wang Yonglin(Guiyang Medical College,Guiyang,Guizhou,China 550004)【机构】 贵阳医学院; 贵阳医学院 贵州贵阳550004; 贵州贵阳550004;【摘要】 目的建立辛芍注射液的含量测定方法。方法采用Diamonsil C18柱(250mm×4.6mm,5μm),以甲醇-0.1%甲酸溶液(40∶60)为流动相,流速1.0mL/min,检测波长230nm,柱温40℃。结果芍药苷质量浓度的线性范围为49~173μg/mL,r=0.9999,平均回收率为98.44%,RSD=2.0%(n=6)。结论所用方法简单、准确、重现性好,适用于辛芍注射液的质量控制。 更多还原【Abstract】 Objective To establish a method for determining paeoniflorin in Xinshao Injection.Methods Diamonsil C18 column(250 mm× 4.6 mm,5 μ m) was used with mixture of methanol-0.1% formic acid(40 ∶ 60) as the mobile phase and the flow rate of 1.0 mL/min.The detection wavelength was 230 nm and the temperature of column was 40 ℃.Results The linear range of paeoniflorin was 49-173 μ g/mL(r=0.999 9).The average recovery rate was 98.44% and RSD was 2.0%(n=6).Conclusion The method is simple,accurate,reproducib... 更多还原【关键词】 辛芍注射液; 赤芍; 芍药苷; 高效液相色谱法; 【Key words】 Xinshao Injection; Radix Paeoniae Rubra; paeoniflorin; HPLC; 【基金】 贵州省中药现代化科技产业研究开发专项基金项目,项目编号:黔科合农字5003。http://ng1.17img.cn/bbsfiles/images/2012/08/201208271547_386445_2352694_3.jpg