我将需要浓缩的蛋白质溶液在-20℃下冷冻20h后在室温下冷却,结果蛋白质形成絮状析出,而且析出的蛋白质能用砂芯过滤器过滤得到比较干的滤饼。这样等到的蛋白质变性了吗?低温可使蛋白质浓缩凝胶析出,这样的蛋白质与之前没处理的蛋白质溶液相比变性了吗?
请教:双缩脲反应测定蛋白质含量时,绘制标准曲线时需要标准蛋白溶液,标准蛋白溶液要用什么蛋白质?我见有用酪蛋白的,可以用胶原蛋白吗?谢谢……
有奖问答:当调节溶液pH值,使蛋白质分子的正、负离子数目相等,此时溶液的pH值即为该蛋白质的?
我是做蛋白质SDS-PAGE电泳的。蛋白质样品用碘乙酸溶液处理后如何除去过量的碘乙酸?1、取约1 mg的总蛋白样品放入离心管中,加入1ml 6M 的尿素溶液,得到1 mg/mL的蛋白溶液。2、加入20微升1M的巯基乙醇到上述离心管中,震荡混合5秒钟。3、将上述离心管恒温在37oC条件下反应1小时 (以还原蛋白中的双硫键)。4、加入25µ L 1M新鲜配制在1M NaOH中的碘乙酸,在避光、室温条件下放置30 分钟。(烷基化将巯基保护起来) 接下来我准备做SDS-PAGE还原电泳,我不清楚样品中的过量碘乙酸对电泳有没有影响?应该怎么除掉?求高人指点![em0808][em0808][em0808][em0808][em0808]
工厂生产时,怀疑盐酸溶液中有蛋白质,我应该怎么判定和测定呢?
请问核磁在蛋白质溶液中有什么应用,至少需要多少MHz?
请教大家:对保存在PBS溶液中的蛋白质样品,要进质谱。但是不知通过什么样的前处理方式,才能去掉蛋白质溶液中的磷酸盐呢?谢谢!
云唐蛋白质检测仪为集成化食品安全快速检测分析设备,广泛应用于液态奶、奶粉等乳品中的蛋白质含量的测定。 测定奶粉中蛋白质含量的过程通常涉及一系列化学反应和分析步骤。以下是一般情况下使用蛋白质检测仪来测定奶粉蛋白质含量的一般操作步骤: 样品准备: 从奶粉中取样,确保样品的代表性。样品量的选择可能因仪器型号和分析方法的要求而有所不同。 样品预处理: 根据仪器要求,可能需要对样品进行预处理。例如,可以使用适当的溶液进行提取、稀释或其他处理,以确保样品的蛋白质能够被准确测定。 仪器准备: 打开蛋白质检测仪,根据仪器的操作手册进行系统的准备和预热,以确保仪器处于合适的工作状态。 校准: 根据仪器的要求,进行校准操作。校准是确保测量结果准确的关键步骤,通常会使用标准溶液进行校准。 装载样品: 将预处理好的样品加入仪器的样品槽中,根据仪器的要求确定每次装样的量。 测定: 根据仪器的指示,启动测定过程。仪器会自动进行反应和测量,然后计算出样品中的蛋白质含量。 结果显示和记录: 测定完成后,仪器会显示蛋白质含量的测定结果。记录结果,可以根据需要打印报告或保存数据。 清洁和维护: 在完成测定后,根据仪器的要求进行清洁和维护,以确保仪器的正常运行和延长使用寿命。 数据分析: 分析测定结果,确保奶粉中的蛋白质含量符合法规要求或产品标准。
请教各位高手:含有蛋白质的溶液如何进行吸收光谱试验?我的是 Ca2+和清蛋白的水溶液,在吸收光谱测量含量时,偏差较大,估计清蛋白的影响,请问有什么办法消除白蛋白的影响么?谢先!!
[font=-apple-system, BlinkMacSystemFont, &][color=#05073b][size=16px]奶粉蛋白质检测仪检测样品处理简单吗,奶粉蛋白质检测仪的样品处理相对简单。奶粉蛋白质快速检测仪具有简单、快速、准确的优点,用于快速检测奶粉中的蛋白质含量。它采用进口超高亮发光二极管作为光路系统,内置工作曲线,无需配制标准溶液,只需使用配套试剂进行零点校准,即可实现样品的快速定量测定。同时,该仪器提供齐全的专用前处理设备及耗材,配备专用预制试剂,缩短试剂配制时间,操作使用方便。总的来说,奶粉蛋白质检测仪简化了传统检测方法中复杂的样品处理步骤,使得样品处理变得相对简单和快速。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2024/05/202405161010150026_3092_6098850_3.jpg!w690x690.jpg[/img][/size][/color][/font]
再传些上来[em09510][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=183555]蛋白质.doc[/url]方法3这个方法(通常称为布拉德福德法)是基于当蛋白质与酸性蓝90燃料结合时在波长470nm-595nm之间有一个吸收峰。酸性蓝90燃料很容易与蛋白质中的精氨酸和赖氨酸的残基结合导致对于不同蛋白质试验具有特异的反应。因此作为参考物的蛋白质必须测定的蛋白质相同。有相对较少的干扰物,但是最好避免试验样品中的洗涤剂和两性电解质。强碱性样品可能会干扰酸性试剂。使用标准蒸馏水来配置此方法中用到的缓冲液和试剂。试验溶液.将待测蛋白质的参考物质溶解在描述的缓冲溶液中配制成浓度在标准曲线范围内的溶液。参考溶液.用描述的缓冲溶液溶解待测蛋白质的参考物质。用相同的缓冲溶液来稀释这个蛋白质溶液制的不少于5个参考溶液,溶液的蛋白质浓度在一个合适的范围内均匀分布在0.1mg/ml和1mg/ml之间。空白.用使用的缓冲溶液来制备测试溶液和参考溶液。酸性蓝90试剂.溶解0.10g酸性蓝90标准试剂在50ml标准酒精溶液中。加入100ml磷酸标准溶液,用标准蒸馏水稀释至1000ml,混匀。过滤此溶液,室温条件下储存在棕色瓶中。储存期间,燃料发生缓慢的沉淀。使用前过滤试剂。步骤.每个测试溶液和空白的参比溶液取0.100ml,加5ml酸性蓝90试剂。倒转混匀。防止发泡,发泡会导致重复性较差。测定标准溶液和待测溶液595nm处的吸光度(2.5.25),把空白作为补偿液体。不要使用石英(二氧化硅)分光光度计比色皿,因为石英会和这些染料结合。计算.吸光度与蛋白质浓度的关系是非线性的;然而,假如,制备标准曲线的浓度范围足够小,后者将接近线性。以标准溶液的吸光度对蛋白质的浓度作图,再线性回归得到标准曲线。从标准曲线和待测溶液的吸光度来计算得到待测溶液的蛋白质浓度。方法4这个方法(通常被称为喹啉酸法或者BCA法)这个基于蛋白质与铜离子反应生成亚铜离子。喹啉酸试剂用于检测亚铜离子。很少物质会干扰这个反应。当存在干扰物质的影响时可以通过稀释来最小化干扰,但必须使得待测的蛋白质的浓度足够精确测量。或者,在方法2中给出的蛋白质凝结的的程序可能被用于去除干扰物质。因为不同的蛋白质种类可能给出不同的颜色反应强度,参考蛋白质和待测蛋白质必须相同。使用蒸馏水R来制备此法中用到的所有缓冲溶液和试剂。测试溶液.用描述的缓冲溶液溶解适宜数量的待测物质制得浓度在参考溶液浓度范围内的溶液。参考溶液.用描述的缓冲溶液溶解蛋白质的参考物质。用同一缓冲稀释部分该溶液制得不少于5个参考溶液,制的的溶液蛋白质浓度均匀分布在10μg/ml-1200μg/ml之间的合适的范围内。空白.使用缓冲溶液来制备测试溶液和参比溶液。BCA试剂.溶解10g的二钠试剂R,20g碳酸钠一水合物R,1.6g酒石酸钠R,4g氢氧化钠R,和9.5g碳酸氢钠R在蒸馏水(R)中。如果有必要,用氢氧化钠溶液R或者碳酸氢钠溶液R调节pH至11.25,用蒸馏水R稀释至1000ml,混匀。步骤.分别将0.1ml的参比溶液,待测溶液,和空白溶液与铜-BCA试剂混合。在37℃条件下反应30min,注意时间,允许混合物冷却至室温。在反应中点60min内,562nm处用石英比色杯测定参考物质和待测物质的吸光度(2.2.25),用空白溶液作为补偿溶液。待溶液冷却至室温后,颜色强度逐渐加深。计算.吸光度对蛋白质的浓度的关系不是线性的。然而,假如,制备标准曲线的浓度范围足够小,后者将接近线性。以参比溶液的吸光度对蛋白质的浓度作图,再线性回归得到标准曲线。从标准曲线和待测溶液的吸光度来计算得到待测溶液的蛋白质浓度。方法5这个方法(通过常称为缩二脲法)基于铜离子与蛋白质在碱性溶液中的反应而引起的545nm处的吸光度的变化。这个试验在IgG与白蛋白之间差异不大。氢氧化钠和缩二脲试剂的加入作为一个联合试剂,在氢氧化钠加入后不充分的混合,或者在氢氧化钠溶液的加入和缩二脲试剂的加入之间额外的时间将会使得IgG样品比白蛋白样品较高的反应。三氯酸原理用于减小干扰物质,也可以用于测定待测溶液中蛋白质的含量,在浓度小于500μg/ml的情况下。使用蒸馏水R来制备所有此试验中用到的缓冲溶液和试剂。待测溶液.用9g/l的氯化钠溶液R溶解适宜数量的待测物质制的浓度在参比溶液浓度范围内的溶液。参比溶液. 用9g/l的氯化钠溶液R溶解待测蛋白质的参比物质。用9g/l的氯化钠溶液R稀释部分此溶液制的不少于3个参比溶液,这一列溶液的蛋白质浓度均匀分布在0.5mg/ml-10mg/ml之间的适宜范围内。空白.使用9g/l的氯化钠溶液R。缩二脲试剂.用10ml的蒸馏水溶解3.46g的硫酸铜,冷却(溶液A)。用80ml的热蒸馏水溶解34.6g的柠檬酸钠R20.0g的无水碳酸钠R。冷却(溶液B)。混合溶液A和溶液B,用蒸馏水R稀释至200ml假如试剂发生浑浊或者包含任何沉淀,不要使用此试剂。步骤.在一个待测溶液中加入等体积的60g/l的氢氧化钠R,混合。立刻加入相当于0.4倍体积待测溶液的缩二脲试剂,迅速混匀。在15℃-25℃的条件下放置不少于15min。90min内加入缩二脲试剂,在最大吸收波长545nm处测定参比溶液和待测溶液的吸光度(2.2.25),用空白溶液作为补偿液体。在蛋白质浓度计算中,任何产生混浊或者沉淀的溶液都是不被接受的。计算.吸光度对蛋白质浓度的关系接近线性在参比溶液指定的蛋白质浓度范围内。以参比溶液的吸光度对蛋白质浓度作图,利用线性回归做标准曲线。计算标准曲线的相关系数,一个好的系统产生的标准曲线的相关系数不少于0.99.从标准曲线和待测溶液的吸光度来测定待测溶液中的蛋白质浓度。干扰物质.为了家少干扰物质的影响,蛋白质可以按以下步骤进行沉淀:加入0.1倍体积的500g/l三氯酸溶液R到1倍体积待测样品溶液中,取走上清液,用较小体积的0.5M的氢氧化钠溶解沉淀。用制得的溶液来制备待测溶液。方法6荧光法是基于o-邻苯二醛对蛋白质的化学衍生反应。它与蛋白质的伯胺基发生反应(N-末端氨基酸和θ-氨基的赖氨酸残基)此法的灵敏度可以通过在加o-邻苯二醛之前按水解蛋白质来增加。水解可以使组成氨基酸的α-氨基可以和邻苯二醛试剂反应。此法需要非常少量的蛋白质。伯胺,例如三(羟甲基)氨基甲烷和氨基酸缓冲溶液,与邻苯二醛反应的必须避免或者替换。高浓度的氨水与邻苯二醛反应。氨与邻苯二醛反应产生的荧光不稳定。自动化程序的使用来标准化这个程序可以增加测试的准确性和精密度。待测溶液.用9g/l氯化钠溶液R溶解适宜数量待测物质制的浓度在参比溶液浓度范围内的溶液。在加邻苯二醛试剂之前调节8-10.5。参比溶液.溶解蛋白质的参比溶液杂9g/l的氯化钠溶液R中。用9g/l氯化钠溶液R稀释部分此溶液制的不少于5个参比溶液,参比溶液蛋白质浓度均匀分布在10μg/ml和200μg/ml之间的适宜范围内。在加邻苯二醛试剂之前调节8-10.5。空白溶液. 用9g/l氯化钠溶液R。硼酸盐缓冲液.用蒸馏水R溶解61.83g的硼酸R,用氢氧化钾R调节pH10.4,用蒸馏水稀释至1000ml,混匀。邻苯二醛储备溶液.用1.5ml的甲醇溶解1.20g的邻苯二醛试剂R,加入100ml的硼酸缓冲溶液,混匀。加0.6ml300g/l 十二烷基醚聚乙二醇23溶液R,混匀。室温下储存,3星期内使用。邻苯二醛试剂.在5ml的邻苯二醛储存溶液中加入15μl的2-巯基乙醇R。至少在使用前30min内植被。24h内使用。步骤.将0.1ml的邻苯二醛试剂与10μl待测溶液和每个参比溶液混合,室温摁下放置15min。加入0.5M的氢氧化钠3ml混匀。在激发波长340nm和发射波长440和455nm处测得参比溶液和待测溶液的荧光强度(2.2.21)。因为照射荧光强度降低,对一个给定的样品的荧光强度只测定一次。计算.荧光强度与蛋白质浓度的关系是线性的。用参比溶液的荧光强度对蛋白质浓度作图,线性回归得到标准曲线,根据待测溶液的荧光强度得到待测溶液的浓度。
请问杭州哪里可以测定溶液态蛋白质的三维荧光光谱,用于测定蛋白质与其他分子作用后的构象变化。
蛋白质分子中,酪氨酸、苯丙氨酸和色氨酸残基的苯环含有共轭双键,使蛋白质具有吸收紫外光的性质。吸收高峰在280nm处,其吸光度(即光密度值)与蛋白质含量成正比。此外,蛋白质溶液在238nm的光吸收值与肽键含量成正比。利用一定波长下,蛋白质溶液的光吸收值与蛋白质浓度的正比关系,可以进行蛋白质含量的测定。紫外吸收法简便、灵敏、快速,不消耗样品,测定后仍能回收使用。低浓度的盐,例如生化制备中常用的(NH4)2SO4等和大多数缓冲液不干扰测定。特别适用于柱层析洗脱液的快速连续检测,因为此时只需测定蛋白质浓度的变化,而不需知道其绝对值。此法的特点是测定蛋白质含量的准确度较差,干扰物质多,在用标准曲线法测定蛋白质含量时,对那些与标准蛋白质中酪氨酸和色氨酸含量差异大的蛋白质,有一定的误差。故该法适于用测定与标准蛋白质氨基酸组成相似的蛋白质。若样品中含有嘌呤、嘧啶及核酸等吸收紫外光的物质,会出现较大的干扰。核酸的干扰可以通过查校正表,再进行计算的方法,加以适当的校正。但是因为不同的蛋白质和核酸的紫外吸收是不相同的,虽然经过校正,测定的结果还是存在一定的误差。此外,进行紫外吸收法测定时,由于蛋白质吸收高峰常因pH的改变而有变化,因此要注意溶液的pH值,测定样品时的pH要与测定标准曲线的pH相一致。1.280nm的光吸收法因蛋白质分子中的酪氨酸、苯丙氨酸和色氨酸在280nm处具有最大吸收,且各种蛋白质的这三种氨基酸的含量差别不大,因此测定蛋白质溶液在280nm处的吸光度值是最常用的紫外吸收法。测定时,将待测蛋白质溶液倒入石英比色皿中,用配制蛋白质溶液的溶剂(水或缓冲液)作空白对照,在紫外分光度计上直接读取280nm的吸光度值A280。蛋白质浓度可控制在0.1~1.0mg/ml左右。通常用1cm光径的标准石英比色皿,盛有浓度为1mg/ml的蛋白质溶液时,A280约为1.0左右。由此可立即计算出蛋白质的大致浓度。许多蛋白质在一定浓度和一定波长下的光吸收值(A1%1cm)有文献数据可查,根据此光吸收值可以较准确地计算蛋白质浓度。下式列出了蛋白质浓度与(A1%1cm)值(即蛋白质溶液浓度为1%,光径为1cm时的光吸收值)的关系。文献值A1%1cm,λ称为百分吸收系数或比吸收系数。蛋白质浓度= (A280´10 )/ A1%1cm,280nm (mg/ml)(Q 1%浓度»10mg/ml)
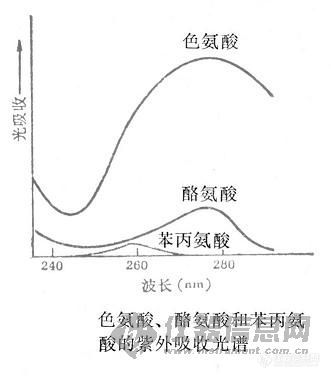
实验原理本实验采用紫外分光光度法测定蛋白质含量。蛋白质中酪氨酸和色氨酸残基的苯环含有共轭双键,因此,蛋白质具有吸收紫外光的性质,其最大吸收峰位于280 nm附近(不同的蛋白质吸收波长略有差别)。在最大吸收波长处,吸光度与蛋白质溶液的浓度的关系服从朗伯-比耳定律。仪器与试剂紫外-可见分光光度计,比色管,吸量管标准蛋白质溶液:5.00 mg.mL-1溶液,0.9% NaCl溶液,待测蛋白质溶液实验步骤1. 标准曲线的制作 : 用吸量管分别吸取1.0 、1.5、 2.0 、2.5 、3.0 mL 5.00 mg.mL-1标准蛋白质溶液于5只10 mL 比色管中,用0.9% NaCl溶液稀释至刻度,摇匀。用1 cm石英比色皿,以0.9%NaCl溶液为参比,在280 nm处分别测定各标准溶液的吸光度A280,记录所得读数。2. 样品测定: 取待测蛋白质溶液3 mL,按上述方法测定280 nm处的吸光度。平行测定三份。数据处理1. 以蛋白质浓度为横坐标,吸光度为纵坐标绘制标准曲线。2. 根据样品溶液的吸光度,从标准曲线上查出待测蛋白质的浓度。注意事项和问题1. 紫外吸收法与Folin-酚比色法测定蛋白质含量相比,有何缺点及优点?2. 若样品中含有核酸类杂质,应如何校正?[img]http://ng1.17img.cn/bbsfiles/images/2008/04/200804041741_83891_1604910_3.jpg[/img]
能不能用NMR来测定蛋白质水溶液中氢键强度的变化抑或说,在蛋白质的变性过程中,氢键强度能不能够测定?并且能用某种试剂完全屏蔽氢键的作用吗。。
分析化学和生物学科之间的交叉越来越多,大家在用电泳分离蛋白质、多肽的时候都用的什么缓冲溶液?您分离的是那类的蛋白质、多肽?
目的]掌握双缩脲法测定蛋白质浓度的原理和标准曲线的绘制。[align=center]原理][/align][align=center]双缩脲(NH2CONHCONH2)在碱性溶液中与硫酸铜反应生成紫红色化合物,称为双缩脲[/align][align=center]反应,蛋白质分子中含有许多肽键(-CONH-)在碱性溶液中也能与Cu2+反应产生紫红色化合物。在一定范围内,其颜色的深浅与蛋白质浓度成正比。因此,可以利用比色法测定蛋白质浓度。[/align][align=center]双缩脲法是测定蛋白质浓度的常用方法之一。操作简便、迅速、受蛋白质种类性质的影响较小,但灵敏度较差,而且特异性不高。除-CONH-有此反应外,-CONH2、-CH2NH2、-CS-NH2等基团也有此反应。[/align][align=center]操作][/align][align=center](一) 绘制标准曲线[/align][align=center](二) 未知样品蛋白质浓度的测定 [/align][align=center] 1.取12支试管[/align][align=center]6支分别加入0,0.4,0.8,1.2,1.6,2.0毫升的标准[/align][align=center] 6支分别加入1毫升不同稀释浓度的待测液(两两相同)。[/align][align=center] 2.分别加水补足到2毫升。[/align][align=center] 3.分别加入4毫升双缩脲试剂在室温/37℃下放置30分钟。[/align][align=center][
大家好,使用毛细管电泳时,样品都要过滤的,可是我提取的蛋白质量很少,怎么过滤啊?我的毛细管已经堵过一次了!有做蛋白质电泳的朋友,帮帮我吧!我的QQ:419817903欢迎一起讨论哦谢谢![em04]
一、样品的浓缩生物大分子在制备过程中由于过柱纯化而样品变得很稀,为了保存和鉴定的目的,往往需要进行浓缩。常用的浓缩方法的:1. 减压加温蒸发浓缩通过降低液面压力使液体沸点降低,减压的真空度愈高,液体沸点降得愈低,蒸发愈快,此法适用于一些不耐热的生物大分子的浓缩。2. 空气流动蒸发浓缩 空气的流动可使液体加速蒸发,铺成薄层的溶液,表面不断通过空气流;或将生物大分子溶液装入透析袋 内置于冷室,用电扇对准吹风,使透过膜外的溶剂不沁蒸发,而达到浓缩目的,此法浓缩速度慢,不适于大量溶液的浓缩。3. 冰冻法 生物大分子在低温结成冰,盐类及生物大分子不进入冰内而留在液相中,操作时先将待浓缩的溶液冷却使之变成固体,然后缓慢地融解,利用溶剂与溶质融点介点的差别而达到除去大部分溶剂的目的。如蛋白质和酶的盐溶液 用此法浓缩时,不含蛋白质和酶的纯冰结晶浮于液面,蛋白质和酶则集中于下层溶液中,移去上层冰块,可得蛋白质和酶的浓缩液。4. 吸收法 通过吸收剂直接收除去溶液中溶液分子使之浓缩。所用的吸收剂必需与溶液不起化学反应,对生物大分子不吸附,易与溶液分开。常用的吸收剂有聚乙二醇,聚乙稀吡咯酮、蔗糖和凝胶等,使用聚乙二醇吸收剂时,先将生物大分子溶液装入半透膜的袋里,外加聚乙二醇复盖置于4度下,袋内溶剂渗出即被聚乙二醇迅速吸去,聚乙二醇被水饱和后要更换新的直至达到所需要的体积。5. 超滤法 超滤法是使用一种特别的薄膜对溶液中各种溶质分子进行选择性过滤的方法,不液体在一定压力下(氮气压或真空泵 压)通过膜时,溶剂和小分子透过,大分子受阻保留,这是近年来发展起来的新方法,最适于生物大分子尤其是蛋白质和酶的浓缩或脱盐,并具有成本低,操作方便,条件温和,能较好地保持生物大分子的活性,回收率高等优点。应用超滤法关键在于膜的选择,不同类型和规格的膜,水的流速,分子量截止值(即大体上能被膜保留分子最小分子量值)等参数均不同,必须根据工作需要来选用。另外,超滤装置形式,溶质成份及性质、溶液浓度等都对超滤效果的一定影响。Diaflo 超滤膜的分子量截留值http://img.dxycdn.com/trademd/upload/userfiles/image/2013/10/A1381571714_small.jpg 用上面的超滤膜制成空心的纤维管,将很多根这样的管拢成一束,管的两端与低离子强度的缓冲液相连,使缓冲液不断地在管中流动。然后将纤维管浸入待透析的蛋白质溶液中。当缓冲液流过纤维管时,则小分子很易透过膜而扩散,大分子则不能。这就是纤维过滤秀析法,由于透析面积增大,因而使透析时间缩短10倍。二、干燥生物大分子制备得到产品,为防止变质,易于保存,常需要干燥处理,最常用的方法是冷冻干燥和真空干燥。真空干燥适用于不耐高温,易于氧化物质的干燥和保存,整个装置包括干燥器、冷凝器及真空干燥原理外,同时增加了温度因素。在相同压力下,水蒸汽压随温度下降而下降,故在低温低压下,冰很易升华为气体。操作时一般先将待干燥的液体冷冻到冰点以下使之变成固体,然后在低温低压下将溶剂变成气体而除去。此法干后的产品具有疏松、溶解度好、保持天然结构等优点,适用于各类生物大分子的干燥保存。三、贮存生物大分子的稳定性与保存方法的很大关系。干燥的制品一般比较稳定,在低温情况下其活性可在数日甚至数年无明显变化,贮藏要求简单,只要将干燥的样品置于干燥器内(内装有干燥剂)密封,保持0-4度冰箱即可,液态贮藏时应注意以下几点。样品不能太稀,必须浓缩到一定浓度才能封装贮藏,样品太稀易使生物大分子变性。一般需加入防腐剂和稳定剂,常用的防腐剂有甲苯、苯甲酸、氯仿、百里酚等。蛋白质和酶常用的稳定剂有硫酸铵糊、蔗糖、甘油等,如酶也可加入底物和辅酶以提高其稳定性。此外,钙、锌、硼酸等溶液对某些酶也有一定保护作用。核酸大分子一般保存在氯化钠或柠檬酸钠的标准缓冲液中。贮藏温度要求低,大多数在0度左右冰箱保存,有的则要求更低,应视不同物质而定。
(一)蛋白质的盐析 取1.5mL蛋白质溶液,加入等体积饱和硫酸铵溶液(浓度为50%饱和),微微摇动试管,使溶液混合均匀后,静置数分钟,球蛋白即析出呈絮状沉淀(如无沉淀可再加少许饱和硫酸铵),用滤纸滤取上清液,滤液中再加入固体硫酸铵粉末至不再溶解,析出的即为清蛋白,再加水稀释,观察沉淀是否溶解。 (二)蛋白质的沉淀 1.用重金属盐沉淀蛋白质 取三支试管,各加1mL蛋白质溶液,分别各加3滴6%醋酸铅溶液、3滴2%硫酸铜溶液和3滴1%硝酸银溶液,观察蛋白质沉淀的析出。 2.用有机酸沉淀蛋白质 取二支试管,各加1mL蛋白质溶液,并加5%醋酸溶液使之呈酸性(该沉淀反应最好在弱酸中进行)。然后分别滴加饱和苦味酸、饱鞣酸溶液,直至沉淀产生为止。 用10%三氯醋酸溶液、3%磺柳酸溶液进行类似实验(用量同前),观察现象。
《从稀释水溶液中萃取和浓缩蛋白质》(Extraction and Concentration of Protein from Dilute Aqueous Solution)应用领域:生物/生物科技目标分析物:牛血清白蛋白BSA样品基质:水萃取柱:BAKERBOND spe™ Wide-Pore Butyl (C4), 500 mg, 6 mL安全防护设备:护目镜和防护面罩,手套,实验服,B型灭火器,通风橱样品制备:配置20mL BSA溶液(1mg/1mL),以0.025M pH=7磷酸缓冲溶液为溶剂小柱活化:加入10mL甲醇活化,5mL 0.5M pH=7磷酸盐缓冲溶液活化,6mL 0.025M pH=7磷酸盐缓冲溶液平衡,保持过程中小柱始终处于润湿状态上样与清洗:关闭真空泵,加入5mL 0.025M pH=7磷酸盐缓冲溶液,装上75mL储液器,缓慢抽出20mL的样品,用4mL0.025M pH=7磷酸盐缓冲溶液淋洗,移去储液器洗脱:用2 X 0.5mL 异丙醇:水:三氟乙酸 60:40:0.1,收集洗脱液分析方法:UV您也可以点击下载英文原版应用文献:http://jtbaker.instrument.com.cn/down_172268.htm
纤维素),当被分离的蛋白质溶液流经离子交换层析柱时,带有与离子交换剂相反电荷的蛋白质被吸附在离子交换剂上,随后用改变pH或离子强度办法将吸附的蛋白质洗脱下来。(详见层析技术章)(四)根据配体特异性的分离方法-亲和色谱法亲和层析法(aflinity chromatography)是分离蛋白质的一种极为有效的方法,它经常只需经过一步处理即可使某种待提纯的蛋白质从很复杂的蛋白质混合物中分离出来,而且纯度很高。这种方法是根据某些蛋白质与另一种称为配体(Ligand)的分子能特异而非共价地结合。其基本原理:蛋白质在组织或细胞中是以复杂的混合物形式存在,每种类型的细胞都含有上千种不同的蛋白质,因此蛋白质的分离(Separation),提纯(Purification)和鉴定(Characterization)是生物化学中的重要的一部分,至今还没的单独或一套现成的方法能移把任何一种蛋白质从复杂的混合蛋白质中提取出来,因此往往采取几种方法联合使用。浓缩、干燥及保存一、样品的浓缩生物大分子在制备过程中由于过柱纯化而样品变得很稀,为了保存和鉴定的目的,往往需要进行浓缩。常用的浓缩方法的:1. 减压加温蒸发浓缩通过降低液面压力使液体沸点降低,减压的真空度愈高,液体沸点降得愈低,蒸发愈快,此法适用于一些不耐热的生物大分子的浓缩。2. 空气流动蒸发浓缩 空气的流动可使液体加速蒸发,铺成薄层的溶液,表面不断通过空气流;或将生物大分子溶液装入透析袋内置于冷室,用电扇对准吹风,使透过膜外的溶剂不沁蒸发,而达到浓缩目的,此法浓缩速度慢,不适于大量溶液的浓缩。3. 冰冻法 生物大分子在低温结成冰,盐类及生物大分子不进入冰内而留在液相中,操作时先将待浓缩的溶液冷却使之变成固体,然后缓慢地融解,利用溶剂与溶质融点介点的差别而达到除去大部分溶剂的目的。如蛋白质和酶的盐溶液用此法浓缩时,不含蛋白质和酶的纯冰结晶浮于液面,蛋白质和酶则集中于下层溶液中,移去上层冰块,可得蛋白质和酶的浓缩液。4. 吸收法 通过吸收剂直接收除去溶液中溶液分子使之浓缩。所用的吸收剂必需与溶液不起化学反应,对生物大分子不吸附,易与溶液分开。常用的吸收剂有聚乙二醇,聚乙稀吡咯酮、蔗糖和凝胶等,使用聚乙二醇吸收剂时,先将生物大分子溶液装入半透膜的袋里,外加聚乙二醇复盖置于4度下,袋内溶剂渗出即被聚乙二醇迅速吸去,聚乙二醇被水饱和后要更换新的直至达到所需要的体积。5. 超滤法 超滤法是使用一种特别的薄膜对溶液中各种溶质分子进行选择性过滤的方法,不液体在一定压力下(氮气压或真空泵压)通过膜时,溶剂和小分子透过,大分子受阻保留,这是近年来发展起来的新方法,最适于生物大分子尤其是蛋白质和酶的浓缩或脱盐,并具有成本低,操作方便,条件温和,能较好地保持生物大分子的活性,回收率高等优点。应用超滤法关键在于膜的选择,不同类型和规格的膜,水的流速,分子量截止值(即大体上能被膜保留分子最小分子量值)等参数均不同,必须根据工作需要来选用。另外,超滤装置形式,溶质成份及性质、溶液浓度等都对超滤效果的一定影响。用上面的超滤膜制成空心的纤维管,将很多根这样的管拢成一束,管的两端与低离子强度的缓冲液相连,使缓冲液不断地在管中流动。然后将纤维管浸入待透析的蛋白质溶液中。当缓冲液流过纤维管时,则小分子很易透过膜而扩散,大分子则不能。这就是纤维过滤秀析法,由于透析面积增大,因而使透析时间缩短10倍。二、干燥生物大分子制备得到产品,为防止变质,易于保存,常需要干燥处理,最常用的方法是冷冻干燥和真空干燥。真空干燥适用于不耐高温,易于氧化物质的干燥和保存,整个装置包括干燥器、冷凝器及真空干燥原理外,同时增加了温度因素。在相同压力下,水蒸汽压随温度下降而下降,故在低温低压下,冰很易升华为气体。操作时一般先将待干燥的液体冷冻到冰点以下使之变成固体,然后在低温低压下将溶剂变成气体而除去。此法干后的产品具有疏松、溶解度好、保持天然结构等优点,适用于各类生物大分子的干燥保存。三、贮存生物大分子的稳定性与保存方法的很大关系。干燥的制品一般比较稳定,在低温情况下其活性可在数日甚至数年无明显变化,贮藏要求简单,只要将干燥的样品置于干燥器内(内装有干燥剂)密封,保持0-4度冰箱即可,液态贮藏时应注意以下几点。1. 样品不能太稀,必须浓缩到一定浓度才能封装贮藏,样品太稀易使生物大分子变性。2. 一般需加入防腐剂和稳定剂,常用的防腐剂有甲苯、苯甲酸、氯仿、百里酚等。蛋白质和酶常用的稳定剂有硫酸铵糊、蔗糖、甘油等,如酶也可加入底物和辅酶以提高其稳定性。此外,钙、锌、硼酸等溶液对某些酶也有一定保护作用。核酸大分子一般保存在氯化钠或柠檬酸钠的标准缓冲液中。3. 贮藏温度要求低,大多数在0度左右冰箱保存,有的则要求更低,应视不同物质而定。
如何利用红外光谱测定溶液中蛋白质的二级结构?有哪些注意事项?谢谢 !期待您的回复!

[size=16px] 食品蛋白质检测仪通常使用一系列的化学、生物化学或物理方法来检测乳制品中的蛋白质含量。以下是一种可能的检测过程: 样品制备: 从乳制品中取得样品,通常需要将样品进行处理,以确保蛋白质在检测过程中能够充分释放和反应。 蛋白质提取: 样品中的蛋白质需要从其他成分中分离出来。这可能涉及到样品的离心、过滤和/或溶解等步骤,以获得含有蛋白质的提取物。 显色/反应: 蛋白质的浓度可以通过与特定试剂发生化学反应或形成复合物来测量。例如,比目鱼法(Bradford法)或比二巴脱酰基试剂(BCA法)都是常用于蛋白质浓度测定的方法。这些试剂与蛋白质反应后会产生颜色变化,颜色的强度可以与蛋白质的浓度成正比。 分光光度测量: 使用分光光度计来测量显色产物的吸光度,从而确定蛋白质的浓度。通常,会建立一个标准曲线,其中包含已知浓度的蛋白质标准样品,用于校准测量结果。 计算浓度: 通过比较待测样品的吸光度与标准曲线上的数据,可以计算出待测样品中蛋白质的浓度。 需要注意的是,不同类型的食品蛋白质检测仪可能会采用不同的方法和试剂,具体的步骤和操作可能会有所不同。此外,为了获得准确的结果,操作者需要在操作过程中遵循标准操作规程,并确保仪器的准确校准和维护。最终结果的准确性也可能会受到样品的处理、试剂的质量以及操作技术等因素的影响。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2023/08/202308291345517046_7349_6098850_3.png!w690x690.jpg[/img][/size]
我用DSC测蛋白质的变性温度,但是重复性很差,有时候有峰,有时候没有。蛋白质是溶液状态的。请问做试验的时候有哪些需要注意的地方呢?哪家哪个型号的DSC比较适合做这个呢?
曲拉通X-114溶液分析蛋白质应选用那种分析柱,我用C8柱,但是谱图基线不稳定,可能是强保留性物质,请专家高手为小弟分析原因,看选择那种柱子合适! 十分感谢!
双缩脲试剂(biuret reagent)是由双缩脲试剂A(NaOH)和双缩脲试剂B(CuSO4)两种试剂组成.双缩脲试剂A的成分是氢氧化钠的质量分数为0.1 g/mL的水溶液;双缩脲试剂B的成分是硫酸铜的质量分数为0.01 g/mL的水溶液。双缩脲试剂可以验证蛋白质的存在。具体方法是:先将双缩脲试剂A加入组织样液,振荡均匀(必须营造碱性环境),再加入双缩脲试剂B,摇荡均匀。如果组织里含有蛋白质,那么会看到溶液变成紫色。具有两个或两个以上肽键的化合物皆可与双缩脲试剂产生紫色反应。蛋白质的肽键在碱性溶液中能与Cu2+络合成紫红色的化合物。颜色深浅与蛋白质浓度成正比。双缩脲(NH2CONHCONH2)是两个分子脲经180℃左右加热,放出一个分子氨后得到的产物。双缩脲试剂本是用来检测双缩脲,因蛋白质中也有-CONH-基也可用于检验蛋白质,与蛋白质接触后的颜色呈紫色
自80年代以来一系列新的软电离技术如快原子轰击电离 、基质辅助激光解吸电离 、电喷雾电离等发现后,生物质谱技术迅速发展,已成为现代科学研究前沿的热点之一。而其中又以基质辅助激光解吸质谱(MALD I2MS)和电喷雾电离质谱(ESI2MS)应用最为广泛。基质辅助激光解吸质谱灵敏度高、可操作性强且对生物样品中的无机盐和缓冲溶液具有较好包容性;电喷雾电离质谱选择性好、分析质量范围宽、样品消耗量小、易于与各种色谱联用。在生物样品的处理中常常需要用到非挥发性的盐,用于为细胞营造无毒的环境,稳定溶剂化的样品及维持酶的活性等。此外,许多用于分离生物分子的分离方法也需要高浓度的盐和缓冲溶液 。但是,样品处理及分离过程中所用的NaCl、十二烷基磺酸钠、盐酸胍、尿素、甘油、二甲基亚砜等都会影响后续质谱高灵敏的分析 。因为这些不挥发的低分子量污染物会导致复杂加合物的形成,增加噪音及造成明显的信号抑制 。此外,在复杂的组织或细胞蛋白质组中,与疾病和信号传导相关的蛋白质往往是属于低丰度的蛋白质,这些重要的蛋白质由于本身存在的量极少而很难得以有效鉴定 。因此,对蛋白质/多肽样品的预富集处理将是MALD I2MS或ESI2MS得到高质量质谱图的前提,也是成功鉴定蛋白质的关键。该文献主要侧重于相关工作的概述。
蛋白质纯化 蛋白质分离纯化是用生物工程下游技术从混合物之当中分离纯化出所需要得目的蛋白质的方法。 是当代生物产业当中的核心技术。该技术难度、成本均高;例如一个生物药品的成本75%都花在下游蛋白质分离纯化当中。常用技术有: 1、沉淀, 2、电泳:蛋白质在高于或低于其等电点的溶液中是带电的,在电场中能向电场的正极或负极移动。根据支撑物不同,有薄膜电泳、凝胶电泳等。 3、透析:利用透析袋把大分子蛋白质与小分子化合物分开的方法。 4、层析: a.离子交换层析,利用蛋白质的两性游离性质,在某一特定PH时,各蛋白质的电荷量及性质不同,故可以通过离子交换层析得以分离。如阴离子交换层析,含负电量小的蛋白质首先被洗脱下来。 b.分子筛,又称凝胶过滤。小分子蛋白质进入孔内,滞留时间长,大分子蛋白质不能时入孔内而径直流出。 5、超速离心:既可以用来分离纯化蛋白质也可以用作测定蛋白质的分子量。不同蛋白质其密度与形态各不相同而分开。
UV紫外吸收法测protein蛋白质含量 蛋白质分子中,酪氨酸、苯丙氨酸和色氨酸残基的苯环含有共轭双键,使蛋白质具有吸收紫外光的性质。吸收高峰在280nm处,其吸光度(即光密度值)与蛋白质含量成正比。此外,蛋白质溶液在238nm的光吸收值与肽键含量成正比。利用一定波长下,蛋白质溶液的光吸收值与蛋白质浓度的正比关系,可以进行蛋白质含量的测定。紫外吸收法简便、灵敏、快速,不消耗样品,测定后仍能回收使用。低浓度的盐,例如生化制备中常用的(NH4)2SO4等和大多数缓冲液不干扰测定。特别适用于柱层析洗脱液的快速连续检测,因为此时只需测定蛋白质浓度的变化,而不需知道其绝对值。此法的特点是测定蛋白质含量的准确度较差,干扰物质多,在用标准曲线法测定蛋白质含量时,对那些与标准蛋白质中酪氨酸和色氨酸含量差异大的蛋白质,有一定的误差。故该法适于用测定与标准蛋白质氨基酸组成相似的蛋白质。若样品中含有嘌呤、嘧啶及核酸等吸收紫外光的物质,会出现较大的干扰。核酸的干扰可以通过查校正表,再进行计算的方法,加以适当的校正。但是因为不同的蛋白质和核酸的紫外吸收是不相同的,虽然经过校正,测定的结果还是存在一定的误差。此外,进行紫外吸收法测定时,由于蛋白质吸收高峰常因pH的改变而有变化,因此要注意溶液的pH值,测定样品时的pH要与测定标准曲线的pH相一致。