在GCMS中经常会看到内标物和替代物(例如: 水质 硝基苯类化合物的测定 气相色谱-质谱法 HJ 716-2014),而且一份标准里面,有一堆内标物和替代物,大家通常是怎么选择?另外,以下是我对内标物的含义,不知道是否正确,但替代物的意思,我还是不太清楚,能指教一下吗?内标物含义:将一个已知质量,样品中不含有杂质的纯物质,加入至待测样品溶液中,以此纯物质的量为标准,对比测定待测组分的含量,该纯物质称为内标物现在一般标准上的内标物的选用是指在目标物质附近出峰,但其化学性质相对稳定,可作为对比测定待测组分的含量。所以内标物不是指特别纯度的物质,只要它满足作为定量参考的要求即可
啥区别?其实一句话来概括就是:内标物是用来定量的,而替代物是监控整个分析过程的。所以替代物(surrogate)必定是在测试初始就加入,而内标物(internal standard)加入时间一般在定容时。内标物和替代物定义内标物--是加到样品、提取物或标准溶液中已知量的纯物质,是用来测定同一溶液中其它分析物质和替代物的相对响应值。内标物质必须是分析的样品组分中所不含有的,一般是目标物的氘代物,用来体现目标物的基底效应。替代物--是一种在任何样品中都不可能被发现的纯物质,其在样品提取和进行其它处理前被加入的等分和量是已知的。它的量是同样品中其它组分一样被测定,它的作用是监控每个样品的方法性能。它是一种与目标物性质相近的物质,一般在前处理之前加,用来表征整个前处理过程的损失或回收率。只是用来监测萃取效率,一般认为其回收率在某一范围(不同标准要求不同)内即认为萃取结果可以定量作为检查结果。异同点首先都要在标准溶液中加入替代加标物和内标,两者最主要的区别在于加入的时间点,萃取前加入,通过最后萃取液的定量,可以确定整个过程的萃取效率及损失,而进样前加入可以修正进样误差,替代加标物如在标液中选择为内标,就可以修正全过程误差,如果视为外标,主要是监控回收效率。内标法在具体做的时候其实包括两部分吧,一个是内标标准曲线的绘制;一个是样品前处理。在绘制内标法标准曲线时,纵、横坐标中,一个是浓度,一个比值(待分析物与内标物峰面积之比,内标物的浓度是固定的),待分析物的浓度是通过把比值(待分析物与内标物的比值)代人内标标准曲线求出的,样品处理虽然会使内标物有所损失,但是由于待分析物与内标物浓度是同方向变化的,并不影响定量结果,这也是内标法的一个优势所在。环境样品应用举例1.替代物的作用替代物监控样品预处理过程中标物的损失或玷污,样品中不应含替代物,替代物也不应是目标物,但应是和目标物的物理化学性质相似的化合物,且能够被定量测定。替代物在样品预处理前定量加入样品中,随样品走完预处理和仪器分析的全过程。由于替代物不断存在于样品中,可以认为替代物的损失或者玷污的程度,即回收率,能够准确测量。又由于替代物和目标物的物理化学性质相似,在预处理过程中两者的损失或玷污的程度是一致的。因此,未知目标物在预处理过程中的回收率,可由已知的替代物的回收率来衡量。这就是替代物在环境样品的分析中的作用。鉴于对替代物的要求,样品的替代物通常是目标物的同位素化合物。例如,测定多环芳烃时,可选用萘、二氢苊、菲、屈等的氘代化合物。它们的物理化学性质与待测的目标物极其相似,萃取过程中的损失或玷污是一致的。经过气相色谱柱的分离后,氘代多环芳烃可以与待测的多环芳烃部分分离。接在色谱后的质谱检测器,可把这些质量数不同的氘代物检出。由于氘代物在天然环境样品中含量极微,替代物的回收率可视为目标物的回收率。2.内标物、替代物与回收率的关系目标物回收率的计算依靠内标物,内标物与替代物一样,不应在样品中出现,也不应是目标物。但对其的物理化学性质的要求不像替代物那么严,只要与目标物相近,在检测器上能被定量检测就行。例如,在分析多环芳烃时,内标物可以是氘代物,也可以是甲基或硝基苯类化合物。内标物在每个样品预处理后,仪器分析前加入样品中,同处理过的试样一起走完仪器分析的全过程。内标物的作用是计算替代物的回收率,美国EPA标准方法中也用来作定量分析的依据。回收率过高或过低说明操作过程有误差,应该避免。替代物的回收率在40%至120%间,分析误差在要求的范围内。这与传统的加标回收率必须达到近 100%的要求有很大差别。传统的定量分析一般是利用工作 曲线来进行的, 其间的内标物可校正仪器分析的误差,对于预处理过程 中误差的校正无能为力,因此希望回收率接近100%。而采用替代物后,定量分析依靠替代物进行,利用回收率对数据进行校正 。
請問有哪位大俠知道是否有磁帶中不含六價鉻的廠商?六價鉻在磁帶生產流程中有什麼作用?請詳細介紹,先謝謝了!
[color=#444444]请问各位大侠,[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]中得选一种中等极性到极性的氘代内标物,用作线性验证和加标回收,请问选择哪些氘代物的极性是中等极性到极性的那,一般选什么那?[/color]
最近发现的,跑氘代孔雀石绿、隐色孔雀石绿内标时(里面不含孔雀石绿和隐色孔雀石绿)竟然出现了孔雀石绿和隐色孔雀石绿本底,响应值还不低,这是怎么回事??[font=&]配置了一个乙腈+水+2种内标混标,内标能打出来的同时,也能打出不低响应值的孔雀石绿和隐色孔雀石绿,但是乙腈+水进样,就没有任何本底了。[/font][font=&]之前怀疑是标的问题,可是换了另一家的还是一样啊。[/font][font=&]只要加了氘代孔雀石绿、隐色孔雀石绿内标,就能出孔雀石绿、隐色孔雀石绿的峰。求救![/font]
[size=4]请问各位老师,[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]中得选一种中等极性到极性的氘代内标物,用作线性验证和加标回收,请问哪些氘代物的极性是中等极性到极性的,一般选什么那? 怎么没有人回答那[/size]
在做油脂中的多环芳烃,购买有氘代内标和EPA16标准品,现在有几个问题想请教一下1、加入氘代内标的作用?在称量样品时加入我知道的作用为监测样品前处理时的损失。2、该如何确定样品中氘代内标的含量?是在制作EPA16标曲时的各个浓度加入同样量的内标?还是使用内标制作标准曲线,测样品时将氘代内标的峰带入得到氘代内标含量,从而与加入量对比确定损失率?3、每个样品中都加入了氘代内标,是否每个样品都需要使用氘代内标计算损失率,然后在计算EPA16时也要加上损失掉的一部分?还是直接使用EPA16标曲的结果作为最终结果结果?4、看到有老师说在使用氘代内标的溶液萃取和定容为最好的方法,想请问下是如何操作的,比如我现在为1g样品+5ml乙腈+氘代内标,该如何操作?5、看到有说一个氘代内标只能监测部分多环芳烃,这是为什么?如果只是为了监测前处理的损失是否符合要求需要多种氘代内标吗?若需要计算每次的损失率来反应真实结果是不是需要EPA16的所有氘代内标。
做的是多环芳烃EPA16,目前有[font=&]氘代内标(菲-D10,芘-D12),想用菲-D10(3环)来校正2-3环的多环芳烃(在开始时加入,每次计算回收率校正数据),用芘-D12(4环)来校正4-6环多环芳烃,请问这种做法可以吗?各种氘代多环芳烃内标具体可以监测那些多环芳烃呢?有无明确要求呢?是每一个环数的多环芳烃都要有氘代内标吗?(高环数氘代内标太贵了)[/font]
如题,是否需要内标?
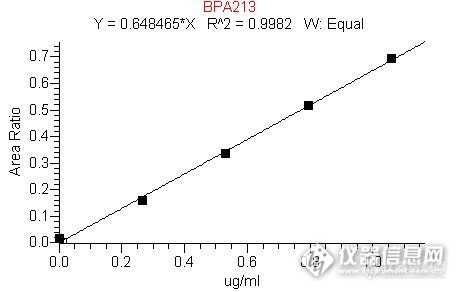
氘代内标在双酚A衍生气质法测定中作用1 方法依据为LPS_004,略有改动以适应于食品模拟物中双酚A的测定,加入乙酸酐次数为1次。http://ng1.17img.cn/bbsfiles/images/2012/12/201212071235_410284_1627834_3.jpg2 衍生化祥细操作步骤http://ng1.17img.cn/bbsfiles/images/2012/12/201212071236_410286_1627834_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/12/201212071239_410289_1627834_3.jpg3 双酚A及16氘代双酚A衍生产物色谱质谱图http://ng1.17img.cn/bbsfiles/images/2012/12/201212071241_410290_1627834_3.jpg4 样品及标品、空白的内标物响应离散(图有误,应为D-14)http://ng1.17img.cn/bbsfiles/images/2012/12/201212071242_410291_1627834_3.jpg5 内标法校准线二http://ng1.17img.cn/bbsfiles/images/2012/12/201212071243_410292_1627834_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/12/201212071252_410296_1627834_3.jpg6 校准线点的内标面积http://ng1.17img.cn/bbsfiles/images/2012/12/201212071245_410294_1627834_3.jpg7 随手在维普查阅双酚A衍生化气质测试文献,有内标的比例,很低。8 结论: 衍生,有内标真好!9 意尽,仍未达版主要求500字,惭愧
由于我们组买的氘代氯仿不含TMS,我昨天做个过夜硅谱,有三个峰,与文献中与文献中机构与此极为相似的化合物的硅谱很接近,文献在氘代苯中做的。请问老师,用不同的氘代试剂,对硅谱中的硅的化学位移是不是没有影响?做硅谱不加内标获得的化学位移可靠吗?谢谢。
岛津EDX-720合金标样中不含汞,也就是说如铝合金、铜合金标准样品中含有铅、铬、镉,但是不含汞,所以测试样品没办法测试汞含量,厂家的解释说合金不会含汞,但没有相关文件,我们对客户没有说服力,咋办啊?
请问在用GC/MS检测溴代酚和氯代酚时,为什么替代物氘代芘和内标氘代双酚A不出峰?我的操作步骤是,先向样品中加入替代物氘代芘,样品首先是固相萃取浓缩,用丙酮-二氯甲烷(50:50)洗脱,加入内标氘代双酚A,然后氮吹吹干,加入100微升吡啶和100微升硅烷化试剂(BSTFA:TMCS=99:1)在70度衍生1h。然后向衍生完毕的样品中加入1 mL丙酮-二氯甲烷(50:50)有机溶剂,最后进行GC/MS分析,仪器是岛津GCMS-QP2010plus,柱子是DB-5ms。分析结果中,溴代酚类和氯代酚类的衍生化产物都可以都可以检测出来,但是却没有氘代芘和氘代双酚A对应的物质峰。然后我又单独检测了氘代芘和氘代双酚A衍生前和衍生后的样品,氘代双酚A衍生前后都不出峰,氘代芘样品只出了一个C14D10的峰,但是氘代芘不是C16D10吗?请知道的和做过的各位高手帮帮忙,能帮我分析一下可能的原因吗,看看要怎么做才可以,谢谢!!
8月29日,海南省食品药品监督管理局向海南椰岛(集团)股份有限公司发出通知,确定“椰岛鹿龟酒”不含非法添加物,可继续正常生产和上架销售。这也意味着,在近一个月的时间里,深受“非法添加违禁物质”舆论危机困扰的海南椰岛(集团)股份有限公司得到官方正式澄清。 29日,海南椰岛(集团)股份有限公司接到海南省食品药品监督管理局发出的《海南省食品药品监督管理局关于海南椰岛(集团)股份有限公司恢复生产和销售的通知》(16号),对此前国内媒体广泛报道的“椰岛鹿龟酒”涉嫌非法添加事件,予以正式澄清:“椰岛鹿龟酒”不含非法添加物,可继续正常生产和上架销售。 今年7月31日,国家食品药品监督管理总局发布《关于51家保健酒、配制酒企业69种产品违法添加行为的通告(2015年第45号)》(以下简称通告),称为海南椰岛(集团)股份有限公司(以下简称“海南椰岛公司”)生产的椰岛鹿龟酒1种产品,涉嫌违法添加行为。 海南省食品药品监督管理局对通告事件高度重视,本着维护消费者切身利益及对企业负责的积极态度,立即组成专案联合调查组,对椰岛公司的原料、生产、流通环节进行了核查,并第一时间赶赴四川进行调查,同时将各地市场下架涉嫌批次产品和其他批次产品,送至国家权威第三方检测机构(海南省食品检测中心、广州SGS、广州金域医学检验中心有限公司和四川省食品药品检验检测院)重新检测,调查及检测结果均显示“椰岛鹿龟酒”不含非法添加物(豪莫本地那非、红地那非、伪伐地那非等非法化学成分),产品质量全部合格。 8月30日,海南椰岛公司相关负责人接受记者采访时表示,29日本是周六,省食品药品监督管理局工作人员加班加点,及时向企业发出通告澄清事实,维护了企业的正当权益。 海南椰岛公司相关负责人表示,作为目前全国保健酒品牌价值第一的国有上市公司,海南椰岛公司是有60多年历史的中国知名企业,在发展历程中始终坚持“质量第一、顾客至上”的宗旨,公司严格按照ISO9001质量标准体系和GMP标准要求建立企业质量管理体系,严把产品质量关,按照国家相关法律法规和GMP标准进行生产,从未添加也绝不添加非法添加物。 这位负责人称,公司产品质量经得起社会各界的监督与检查。在政府监管部门的规范执法和严格监管下,椰岛公司责无旁贷地通过行业自律为保健酒行业的规范发展做出贡献。此次事件之后,椰岛公司将更加强化内控质量体系建设,并积极配合国家有关监管部门的监督、检查。
小弟最近买了两个氘代内标,溶于乙腈的。由于之前配标准曲线都是用的壬烷,防治挥发且比较稳定。但是乙腈与壬烷不互溶,导致混不均匀。而用都用乙腈的话又怕DB-5MS的柱子流失严重。考虑以上这些原因,用什么溶剂来配制标准曲线呢?甲苯?丙酮?二氯甲烷?哪一个比较靠谱呢?
请问各位大佬们,我目前是检测阿替洛尔,硝苯地平,卡托普利,利血平等11中心血管物质,大多数文献都采用的内标法,选择的氘代物作为内标,那么有些物质像卡托普利,利血平等文献上没有合适的内标(氘代物),1.像利血平有的文献会用不是氘代物的内标,那会不会和其他物质反应冲突,还有的文献利血平没有内标,那它根据什么定量啊?2.十几种药物的替代物怎么选择?大多数文献都没有选择替代物的内容,那我可以将几种定量内标(氘代物)的操作步骤移到样品前处理之前 ,当做替代物吗?这样做会对后面的定量或者回收率有影响吗?请各位帮帮忙,谢谢!
有谁能说说为什么有些测试需要使用氘代内标物,内标物标准试剂国内买不到,国外买的貌似不好溯源,怎么办
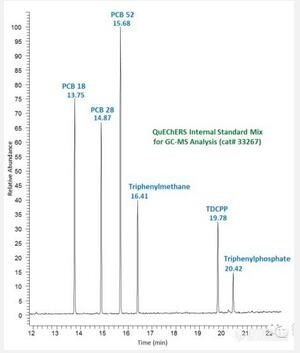
方法中使用内标,可以有效的提高方法的精密度和准确度,可以很好的校准由基质干扰造成的信号抑制或放大(suppression or enhancement)。另外,由于标样和样品中的内标含量是一定的,可以用来校准进样带来的偏差,同时通过计算与目标物保留时间的比值,也可以用来定性。选择合适的内标是关键,内标的化学性质应该与目标物相近,并且样品不含有内标物,避免带来干扰。我们可以通过查询目标物的结构和沸点,来寻找合适的内标物。理论上每个目标物都对应一个内标物,但这对多组分的测试是不切实际的,实际上我们可以根据物质的出峰时间早,中,晚分成几个系列,每个系列对应一种内标物。如果使用的是质谱检测器,目标物的同位素化合物是极佳的内标选择,例如氘标记化合物(包含代替氢氘)或13C标记(含碳原子代替12C原子)。但对于其它检测器(FID, ECD, or NPD or LC detector),由于同位素内标物和目标物是同一时间出峰的,就不是很合适,许多环境分析的方法,会选择含氯或的溴的物质作为内标。例如杀虫剂的测试,会选择以下6种物质作为内标:http://ng1.17img.cn/bbsfiles/images/2016/07/201607151336_600643_1610895_3.jpg来源:互联网
请教一下各位老师,铝合金中含不含C元素?如何用直读光谱仪检测?
如题,请教:内标有一定的氘代率,例如:D0=0.1%,D1=0.4%,D2=0.6%,D3=40%,D4=50%,D5=8.9%内标为D4,在计算储备液浓度时是否需要乘以丰度,
[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]采用内标法定性一个杂质,需要内标物与待测杂质的含量一致嘛。比较相对保留时间是样品中内标物与待测杂质保留时间之比与标准溶液中内标物与已知杂质保留时间之一致或在误差范围内嘛(是不是相对保留时间在正负0.1范围内,就能确定待测杂质是我猜测的已知杂质呀)
求教各位:氘代盐酸试剂说明书中介绍"浓度不低于20%,氘代度不低于99.0%"的含义是什么?就我所知,氘代盐酸的制备一般用HCl通入D2O中实现.其"浓度不低于20%"应该是指HCl在重水中的浓度不低于20%,这一结果是如何测定的?是用普通的酸碱滴定法吗?从氘代度的定义来看,99.0%的氘代度是指含99个DCl,一个HCl.但如果用普通的滴定法滴定氘代盐酸的浓度,滴定的结果又应该说明什么?上述概念不清楚,烦劳各位大虾指教.谢谢!
2009年1月22日,欧盟出台了利于麸质不耐症患者的食品标签和成分新规定。根据新的欧盟条例,要求将“不含麸质”或“含微量麸质”注明于食品成分标签中,规定只有含低于20ppm麸质的食品才允许在其预包装上标注“不含麸质”,而之前食品中“不含麸质”标注的含量可能为目前的10倍或更高;此外,“含微量麸质”标签适用于已经进行特殊处理及去除大量麸质,但食品成分中仍存在低于100ppm麸质的食品。这些食品包括某些主食替代物,如面包。上述两种食品中麸质标示方式旨在确保所有食品的麸质成分使用统一标语,便于麸质不耐受的消费者选购及确保安全使用的知情权。制造商可以立即使用新的标签制度,但为了确保其有足够的时间以适应新规则并对产品或包装进行重新更改,法规允许制造商在2012年1月1日之前对其产品进行调整。来源:flex-news刘亚力编辑
版友的问题:GC待测物含内标,用安捷伦6890或者7890在内标含量里如何输值?
HJ700-2014 水质 65种元素的测定方法中,标准溶液皆为多种元素的混标,但是其中又含有内标物,这如何定量?如Ba的推荐内标物为In,而推荐的混标里Ba和In是在同一个混标里的,哪位做过这个方法的同行能解释一下吗?另外顺便问一下这些混哪里有买?
氘带硫酸里面没有内标物,如何用来定标?
请问[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]内标法应用有内标物必须与待测物含量相当的要求吗?
请问大家,我目前在研究阿替洛尔,硝苯地平,卡托普利,利血平等11种心血管药物的检测方法,使用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url],文献普遍使用内标法定量,多为氘代物,那么问题来了1.卡托普利,利血平还有其他没有找到合适的内标,有的文献中这些药物测定没有内标物,这是为什么啊?2.内标物质(氘代物)定量,定容的时候加入。那这么多物质的替代物怎么选择(大部分文献都没有替代物的信息),那那些文献怎么算回收率的啊?3.可以从内标物里选择几种,在样品前处理之前加入,充当替代物算回收率吗?会影响后续待测物质的定量吗?
[align=center][b][size=18px]运用气相色谱内标法测定食品中甜蜜素含量 [/size][/b] [/align] 甜蜜素化学名称为环己基氨基磺酸钠,于1937年发现,1950年开始生产应用。它是由环己胺和氨基磺酸或三氧化硫反应后用NaOH处理,再重结晶制得的一种白色结晶粉末,甜度为蔗糖的30~80倍。风味较自然,后苦不明显,热稳定性高,是不被人体吸收的低热能甜味剂。1969年曾因其致畸性的报道而被世界各国禁用,后来由于大量试验表明它并无致畸、致癌等作用,许多国家重又许可使用。我国于1987年开始应用甜蜜素,它是目前我国食品行业中应用蕞多的一种甜味剂。甜蜜素含量检测目前有气相色谱检测方法、液相色谱检测方法和液相色谱-质谱/质谱法等,但应用最为广泛的方法是依据GB/T5009.97-2016《食品中环己基氨基磺酸钠的测定》标准中的气相色谱仪分析法。色谱分析技术人员采用在提取溶剂正己烷中加入两种内标物质(甲苯和乙酸正丁酯)对甜蜜素经过衍生后的产物进行定量,具有快捷,准确等特点,受到普遍欢迎。1.试验部分1.1原理在硫酸介质中甜蜜素与亚硝酸钠反应,生成环己醇亚硝酸酯,利用气相色谱法进行定性和定量。1.2试剂(所用试剂不做说明皆为分析纯,水为蒸馏水)1.2.1甜蜜素储备溶液:称取1.0000g甜蜜素(含量≥99.0%),加水溶解并定容至100mL,此溶液浓度为10.00mg/mL,为储备液。置于4℃的冰箱中。本次试验溶液浓度为:10.320mg/mL1.2.2甜蜜素标准使用溶液:取1.2.1储备液10mL,加水定容至100mL,为使用液,浓度为1.0000mg/mL。本次试验使用溶液浓度为:1.0320mg/mL1.2.3100g/L硫酸溶液:称取50g浓硫酸,用水定容至500mL。1.2.450g/L亚硝酸钠溶液:称取25g亚硝酸钠,用水定容至500mL。1.2.5正己烷1.2.6甲苯(内标)1.2.7乙酸丁酯(内标)1.2.8氯化钠1.3仪器1.3.1气相色谱仪GC-2020(带FID检测器、毛细管进样口、N2000色谱工作站)1.3.2DB-5毛细管柱(30m×0.32mm×0.25μm)或其它类型毛细管柱,如DB-1、DB-17011.3.3离心机1.3.410μL微量进样器1.4仪器操作条件1.4.1检测器:200℃1.4.2汽化室:180℃1.4.3柱温:70℃1.4.4载气流速(压力):100kPa1.4.5氢气流速(压力):50kPa1.4.6空气流速(压力):60kPa1.5样品前处理1.5.1内标溶液的配置:在正己烷中加入一定量的内标(乙酸丁酯和甲苯)1,加入的量以出色谱峰合适为宜。一般为500mL正己烷中加入内标100μL~200μL。本次实验乙酸丁酯的浓度为0.1344mg/mL(称量0.0672g乙酸丁酯于装有10mL左右正己烷的25mL容量瓶中,再将溶液转移至500mL容量瓶中并定容至刻度线,摇匀,备用。1.5.2标准溶液前处理:吸取1.2.2标准溶液10mL于50mL比色管中,加10mL水,摇匀,置于冰浴中。加入5mL50g/L亚硝酸钠溶液,5mL100g/L硫酸溶液,在冰浴中放置30min,并时常摇动,然后准确加入10mL1.5.1溶剂,5g氯化钠,摇匀后振摇80次。静置分层。吸出正己烷层于10mL带塞离心管中进行离心分层(如有机溶剂和水相很快就有分层或只要进样针能吸出提取的溶剂,就可以不需离心分离这一步骤),吸取正己烷层1μL注入色谱仪进行分析。算出校正因子2。1.5.3液体样品前处理:称取试样20.0g于50mL带塞比色管中,加10mL水。摇匀,置于冰浴中。处理过程同标准溶液前处理1.5.2。吸取正己烷层试样1μL注入色谱仪进行分析。1.5.4固体样品前处理:称取已磨碎(剪碎)试样2.0~10.0g(根据样品中甜蜜素含量而定称取质量,使甜蜜素的量在1~10mg之间)于50mL带塞比色管中,加10mL水。一些样品不易溶解,如蜜饯类、山楂等,置于水浴锅中煮沸15min左右,冷却至60℃以下,置于冰浴中。处理过程同标准溶液前处理1.5.2。吸取正己烷层试样1μL注入色谱仪进行分析。2结果与讨论2.1.1分析方法的线性相关性的测定分别吸取1.2.1标准溶液1mL、3mL、5mL、10mL、20mL于5个100mL容量瓶中,并定容至刻度,配成浓度分别为0.1032mg/mL、0.3096mg/mL、0.5160mg/mL、1.0320mg/mL、2.0640mg/mL的标准溶液。分别吸取以上标准溶液10mL于5支50mL比色管中,按1.5.2方法进行处理。每个标准点分别进样5次,每次进样1μL,以甜蜜素与内标物的质量比为横坐标,甜蜜素与内标物的峰面积比(取五次进样平均值)为纵坐标绘制标准曲线,得线性方程为y=0.43991x-0.00088,其线性相关系数为0.99999。2.1.2分析方法的准确度的测定从市场上购买一种不含甜蜜素的饮料(样品名称:鲜橙多橙汁饮料生产单位:昆山统一企业食品有限公司净含量:2L生产日期:20060307),称取5份一定量的试样,用移液管分别加入1.2.2标准溶液1、3、5、10、15mL,按上述气相色谱操作条件测定甜蜜素回收率,结果都在99.7%~101.1%之间。2.1.3分析方法的精密度的测定从市场上购买一种含有甜蜜素的饮料(样品名称:鲜橙多生产单位:康裕食品有限公司净含量:1.5L生产日期:20060415),从同一产品中称取五个试样。按1.5.2方法进行处理后,按上述气相色谱操作条件测定甜蜜素含量,得到标准偏差为0.0027,变异系数(RSD)为0.55%。3结论综上所述,本方法简便、快速、准确,具有较高的准确度、精密度和回收率,线性关系好,是一种非常可行的分析方法。注:1用甲苯和乙酸丁酯做内标都可以,可同时加入两种内标(选其中一种作为参照计算),也可以只加其中一种。本次试验的数据是以乙酸丁酯为内标进行计算而获得的。2甜蜜素用本方法衍生处理后,在毛细管柱上会出两个峰,一般是刚开始前面的大,后面的很小,但时间长了,后面的峰越来越大,相应的,前面的峰越来越小直至消失,但两个峰面积和是不变的(48小时之内)。计算校正因子时,用甜蜜素衍生产物的两个峰的面积和计算。检测样品时,两个峰可单独识别并采用同一个校正因子计算,结果相加,也可以使用工作站将峰面积相加,再计算含量。一批样品检测,样品和标准品使用同一浓度的内标溶剂,在计算校正因子时,可将内标物的量假定为1(任一定值皆可),使用非常方便,不需知道加入的内标物的质量。否则,要称量内标物的质量,[font=FZSSK--GBK1-0]精确[/font]至0.0001g,再定容至一定体积。算出内标物浓度,再进行校正因子的计算。
按照标准操作的话,内标物正戊烷的溶剂应使用甲苯,但甲苯的毒性是不是有点大?另外,查看了一下以前的帖子,貌似可溶氟、游离氟、总氟量正常情况下应该是一致的吧,企业内部自控是不是可以用离子电极法进行控制呢?2016.2.26修改及补充内容:25日发帖的内容有误,之前仅认为甲苯为内标物溶剂,但后来仔细查看标准,甲苯在本标准中还是后续衍生反应的溶剂并萃取衍生产物。这里进行一下更正。整个反应生成三甲基氟硅烷,最后检测的应该就是这种物质,关于衍生产物的溶解性没有查到。三甲基氯硅烷溶于苯、乙醚和过氯乙烯,这几样溶剂安全性也不是很高。基于以上的信息,不知是否意味着没有替代溶剂?