方案详情文
智能文字提取功能测试中
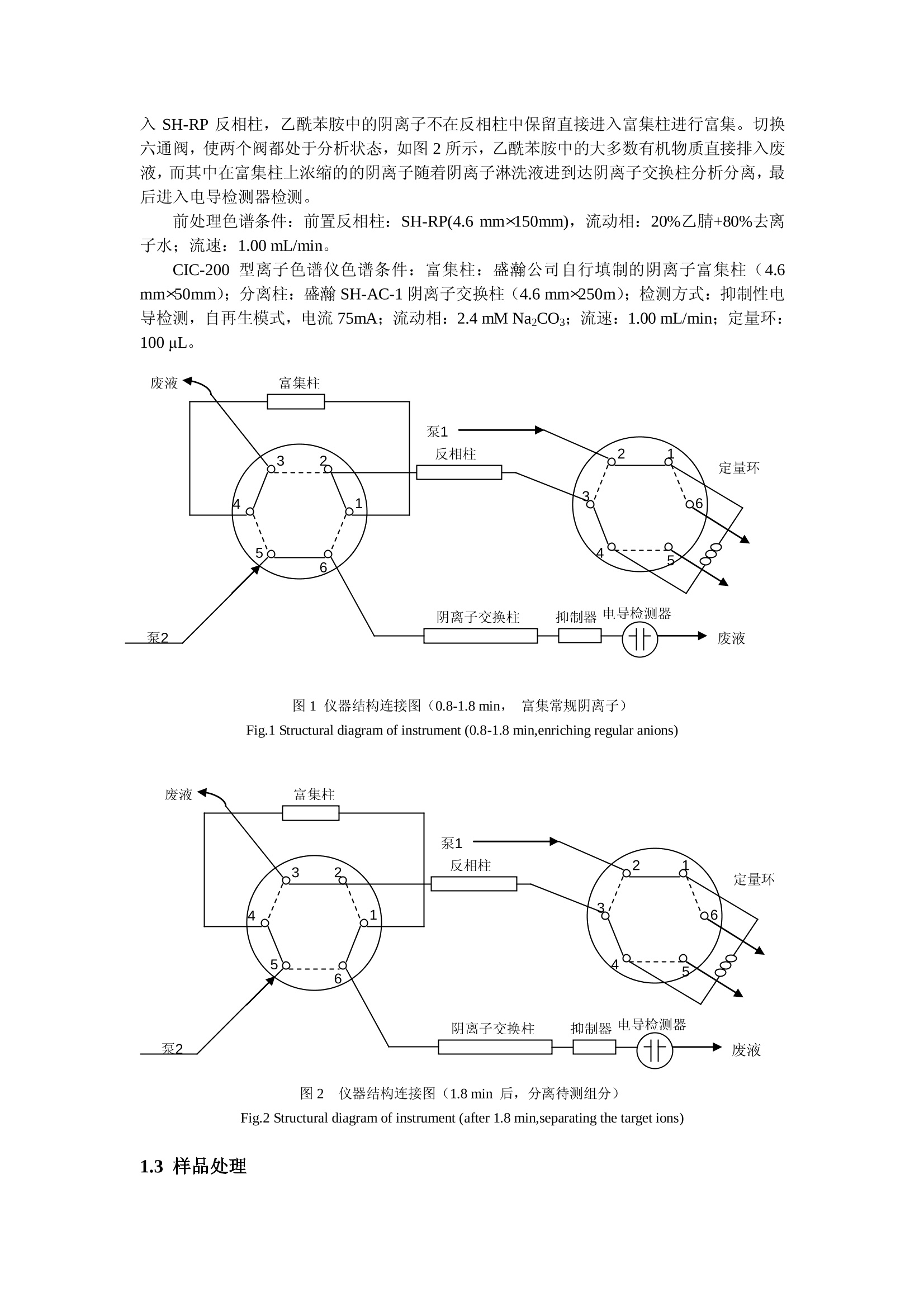
柱切换离子色谱法测定乙酰苯胺中的硫酸根离子 王敬花*,张锦梅,王钧 (青岛盛瀚色谱技术有限公司,青岛266101) 摘要:采用国产离子色谱仪(CIC-200型)建立了测定乙酰苯胺中硫酸根离子的离子色谱分析方法。使用SH-RP (4. 6 mm×150mm)反相柱将所需分析的 SO.离子从乙酰苯胺中分离出来,再将被分离组分通过阴离子交换富集柱 SH-AC-1 (4.6 mmx 50mm)进行富集,最后将富集后的样品通过 SH-AC-1(4.6 mm×250mm)色谱柱进行分离,抑制型电导检测器进行检测。用于实际样品分析时, S0 的加标回收率分别为92.7-97.7%。线性良好,且具有较好的重现性和较低的检出限。 关键词:离子色谱;柱切换; 乙酰苯胺;硫酸根离子 中图分类号:0657.7 文献标识码:A 前言 乙酰苯胺是磺胺类药物的原料,可用作止痛剂、退热剂和防腐剂。在合成工艺过程中引入硫酸根离子,其含量高低对人体的健康及对医药中间体的评价有重要意义。目前,检测硫酸根离子的方法主要有:重量法、滴定法2、间接原子吸收分光光度法3、间接紫外分光光度法12.41和间接电感耦合等离子体原子发射光谱法⑤。这些方法前处理时间较长,检出限高,重现性差,很难满足检测要求。自从离子色谱法发展起来后,对于测试这种复杂有机基体中的少量离子,可以用反相柱切换-离子色谱法简单完成,该方法无需前处理,检测限低。 在线浓缩富集和基体消除的柱切换技术无需特殊仪器设备、操作简单,而且具有较大的灵活性,已经成为复杂基体中痕量离子的有效方法16,7。目前,柱切换技术已经被用于测定高浓度无机酸中的痕量阴离子[8,9]和水溶性有机溶剂中的杂质阴离子[10,11]。本文采用国产离子色谱仪 (CIC-200 型)[12],使用 SH-RP 反相柱将待测无机离子与乙酰苯胺预分离,调节淋洗液中乙腈与水的比例,使乙酰苯胺的出峰时间在无机离子完全冲出之后。同时在定量环上连接一根 SH-AC-1阴离子交换柱(4.6mmx50mm)对样品进行富集。富集后的阴离子进入 SH-AC-1(4.6 mmx250mm)离子交换柱进行分离,经抑制电导检测器检测。该法克服了乙酰苯胺中阴离子含量低的问题,可以对其中的硫酸根离子进行准确的测定。对其它有机试剂中的阴离子测定有借鉴作用。 1实验部分 1.1试剂和仪器 标准溶液(1000 mg/L):用基准试剂 Na2SO4配制 SOz的混合标准液。用时根据需要稀释成系列标准溶液。溶液都用 18.2 MQ·cm 的二次去离子水配制。反相柱的淋洗液采用20%乙腈+80%水的混合液;离子交换柱的淋洗液用2.4mM NazCO3. CIC-200 型离子色谱仪(青岛盛瀚), UC-3281 高效液相泵(北京优联), Smartline 100 型高效液相泵(德国诺尔),7725i-Rheodyne(美国阀), MHP 9900-500-1-Rheodyne(美国阀),SHY-2 自再生抑制器(青岛盛瀚), DDC 电导检测器(青岛盛瀚), UC-3292 紫外检测器(北京优联), SH-RP 反相柱(4.6 mmx150mm), SH-AC-1 阴离子富集柱(4.6mm×50mm)(青岛盛瀚);;SH-AC-1 阴离子交换柱(4.6 mmx250mm)(青岛盛瀚)。 UC-3268 色谱工作站,HW-2000色谱工作站。 1.2色谱条件 图1和图2显示了色谱系统的工作时仪器。在连接仪器时尽量缩短仪器单元与单元之间的连线,,以减少死体积。图1中样品装载到定量环中,乙酰苯胺样品随着乙腈/水淋洗液进 ( 基金项目:科技部科技型中小企业技术创新基金(09C26213711749)资助 ) ( 作者简介:王敬花(1983-),女,硕士研究生; Email:qduwjh@hotmail.com ) 入 SH-RP反相柱,乙酰苯胺中的阴离子不在反相柱中保留直接进入富集柱进行富集。切换六通阀,使两个阀都处于分析状态,如图2所示,乙酰苯胺中的大多数有机物质直接排入废液,而其中在富集柱上浓缩的的阴离子随着阴离子淋洗液进到达阴离子交换柱分析分离,最后进入电导检测器检测。 前处理色谱条件:前置反相柱: SH-RP(4.6 mmx150mm), 流动相:20%乙腈+80%去离子水;流速::1.00mL/min。 CIC-200 型离子色谱仪色谱条件:富集柱:盛瀚公司自行填制的阴离子富集柱(4.6mmx50mm);分离柱:盛瀚 SH-AC-1阴离子交换柱(4.6mmx250m);检测方式:抑制性电导检测,自再生模式,电流75mA;流动相:2.4 mM NazCO3;流速:1.00mL/min;定量环:100 pL。 图1仪器结构连接图(0.8-1.8 min, 富集常规阴离子) Fig.1 Structural diagram of instrument (0.8-1.8 min,enriching regular anions) 图2 仪器结构连接图(1.8min 后,分离待测组分) Fig.2 Structural diagram of instrument (after 1.8 min,separating the target ions) 1.3样品处理 称2.5 g乙酰苯胺样品用乙腈溶解,定容到50mL, 超声 20min, 过0.22um滤膜进样。 2结果与讨论 2.1乙酰苯胺稀释浓度的选择 分别取 1.0 g、2.5 g、5.0g乙酰苯胺溶于 50 mL 乙腈进样出峰研究,结果表明:取1g乙酰苯胺时离子浓度太低,不能够准确定量;取 5.0g 乙酰苯胺时进样线性较差,故选择取2.5 g 乙酰苯胺用乙腈溶解,定容至 50mL。 2.2切换时间的确定 反相柱可以对有机物质进行保留,样品进样后,经反相柱预分离,后串联电导检测器和紫外检测器。由电导检测器所得谱图(图3)可知无机离子在 0.8-1.8 min 内冲出,同时由紫外检测器所得谱图(图4)可知对乙酰苯胺及其有机物杂质在3 min 后冲出。因此选择切换时间为 0.8-1.8 min, 保证无机离子全部流入富集柱,乙酰苯胺及其所含有的有机成分尽可能少的进入富集柱。 图3电导检测器测无机离子 1-无机离子 Fig.3 Direct conductivity detection of inorganic ions1-inorganic ions 图4紫外检测器测乙酰苯胺(X=254nm)1-杂质;2-乙酰苯胺 Fig.4 UV detection of acetanilide (=254 nm)1-impurities;2-acetanilide-+ 2.2方法的检出限和工作曲线 在所采用的色谱条件下 1000mg/L 的 SO4贮备液逐级稀释至2.5 mg/L、5 mg/L、10 mg/L、20 mg/L、40 mg/L,依次进样,在所选用的色谱条件下测得峰面积,绘制标准曲线。 SO4的线性关系和检出限见表1。配制标准溶液进行重现性试验,连续进针5次, SOA离子重复性较好,结果表明,它的保留时间的 RSD 为0.21%,峰面积的 RSD 为 3.8%,峰高的 RSD为 2.9%。 表1线性关系及检出限 Tab.1 The linear relationships and detection limits of anion samples 组分 线性范围 线性关系 相关系数(R*) 检 出 限 (mg/L) (mg/L)(S/N=3) SO4 2.5-40 y=5.227×10x-9.003×10* 0.9986 0.057 2.3样品分析及回收率实验 样品直接进样,由标准曲线计算样品中 SOA离子含量。按照1:0.5加标,连续进样三次。测得的回收率,结果见表2。由表可知,回收率在 92.7%-97.7%之间,结果较为满意。图5为乙酰苯胺样品中的 SO4离子的色谱图,图6为样品加标图。 表2分析结果及方法的回收率 Tab.2 Analytical results and the recovery data of anions in samples 离子 含量 加入量 回收率 (mg/L) (mg/L) (%) SO4 8.913 4.5 95.55±2.85 150 图5乙酰苯胺样品中的 SOZ离子的色谱图1-SO离子 Fig.5 Chromatogram of SO anion in acetanilide 1-SOA anion 150 图6乙酰苯胺样品中的 SO2离子加标色谱图1-SO离子 Fig.6 Chromatogram of SO anion added in acetanilide 1- SOA anion 3结论 本方法采用反相柱预分离后富集柱浓缩阴离子进入离子交换色谱分离的方法,对乙酰苯胺样品中的阴离子做了系统的分析测定,既解决了该类化合物直接进样对色谱柱有破坏使得被分析检测的离子受到影响的难题,又解决了这类样品阴离子水溶液稀释后浓度过低检测灵敏度不够的问题。结果表明,所使用的方法真实可靠,重现性良好,分析方法简单,峰形较好。这种方法对其它高浓度基体离子对痕量离子的测定也有一定的启发作用。 ( 参考文献 ) ( [1]GB/T 11899-1989.水质硫酸盐的测定重量法 ) ( [2]GB/T 13025.8-1991.制盐工业通用试验方法硫酸根离子的测定 ) ( [3]GB/T 13196-1991.水质硫酸盐的测定火焰原子吸收分光光度法 ) ( [4]邱勋鹏,黄承玲,鄢建平.理化检验:化学分册,2003,39(12):711 ) ( [5]徐鹏,王莹,辛士刚.光谱实验室, 2006,23(3):458 ) ( [6]牟世芬,刘克纳,丁晓静.离子色谱方法及应用.北京:化学工业出版社,2005.66 ) ( [7]Y. Shi, Y. Cai, J. Liu, S. Mou, Microchim. Acta 2006,154:213 ) ( [8]VERMEIREN K.Trace anion determination i n concentrated hydrofluoric acid solutions by two-dimensional ionchromatography I . Matrix elimination by ion- ) ( exclusion chromatography [J].J of Chromatography A,2005,1085:60 ) ( [9]任丹丹,方晓霞,姚超英,朱海豹,叶明立,朱岩.离子色谱柱切换法测定酒石酸中的痕量阴离子[].浙江大学 学报:理学版,2010,37(4): 446 ) ( [10]陈梅兰,李长安,焦霞,朱岩.离子色谱柱切换进样抑制电导检测环丁砜中的杂质阴离子[].浙江大学学报: 理学版,2008,35(12):200 ) ( [11]陈梅兰,焦霞,叶明立,朱岩.柱切换离子色谱法测定丙酮中痕量阴离子[].分析实验室,2007 ,26(12):102 ) ( [12]袁悦,张宁,卢造权,叶红梅.离子色谱法分析亚硫酸盐时与其它阴离子的相互影响[].分析试验室, 2010,29(5):281 ) Determination of sulfate anion in acetanilide by ionchromatography with column-switching Abstract: A method has been described for the determination of trace of sulfate anion inacetanilide by domestic ion chromatographic (CIC-200 type).The application of HPLC columnSH-RP (4.6 mmx150mm) was aimed to separate sulfate anion from acetanilide, and a guardcolumn SH-AC-1 (4.6 mmx50mm) made low concentration trace anion enrichment. The traceanions were separated and determined in an analytical column SH-AC-1(4.6 mmx250mm) by ionchoromatography with suppress conductivity. The recovery of sulfate anion added was in therange 92.7-97.7%.Good linearity, repeatability and low detection were obtained. Keywords: I on chromatography; Column-switching; Acetanilide ; Sulfate anion
关闭-
1/6

-
2/6
还剩4页未读,是否继续阅读?
继续免费阅读全文产品配置单
青岛盛瀚色谱技术有限公司为您提供《柱切换离子色谱法测定乙酰苯胺中的硫酸根离子》,该方案主要用于其他中null检测,参考标准《暂无》,《柱切换离子色谱法测定乙酰苯胺中的硫酸根离子》用到的仪器有null。
我要纠错
相关方案


 咨询
咨询