方案详情文
智能文字提取功能测试中
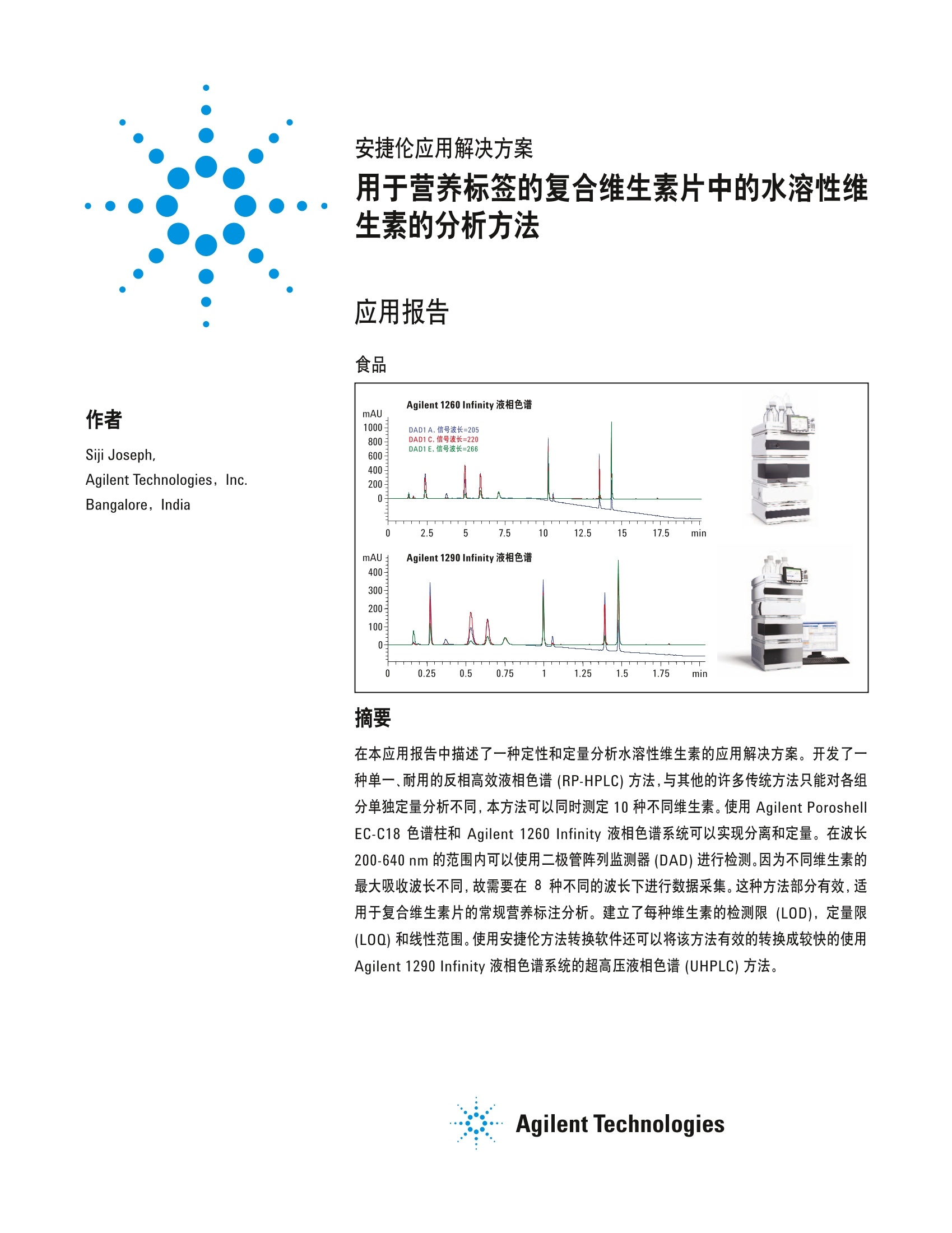
作者 Siji Joseph,Agilent Technologies, Inc.Bangalore, India 安捷伦应用解决方案 用于营养标签的复合维生素片中的水溶性维生素的分析方法 应用报告 食品 摘要 在本应用报告中描述了一种定性和定量分析水溶性维生素的应用解决方案。开发了了种单一、耐用的反相高效液相色谱(RP-HPLC) 方法,与其他的许多传统方法只能对各组分单独定量分析不同,本方法可以同时测定10种不同维生素。使用Agilent PoroshellEC-C18色谱柱和 Agilent 1260 Infinity 液相色谱系统可以实现分离和定量。在波长200-640 nm的范围内可以使用二极管阵列监测器 (DAD)进行检测。因为不同维生素的最大吸收波长不同,故需要在8种不同的波长下进行数据采集。这种方法部分有效,适用于复合维生素片的常规营养标注分析。建立了每种维生素的检测限 (LOD),定量限(LOQ)和线性范围。使用安捷伦方法转换软件还可以将该方法有效的转换成较快的使用Agilent 1290 Infinity 液相色谱系统的超高压液相色谱 (UHPLC) 方法。 前言 维生素是一类小分子化合物,需要量不大但确非常重要,对于保持正常的健康和生长具有特殊的作用。因为维生素不是由人体自然合成的,因此必须保持平衡的饮食以保证维生素的摄取水平。然而,有时候饮食习惯会造成维生素的缺乏。在这种情况下,市售复合维生素片可以适当对其进行补充。虽然缺乏维生素会引起的疾病,但是过量的维生素也会损害身体健康。食品和药物管理局(FDA)要求对复合维生素片中的维生素进行标注。这就尤为需要开发一种能够定量分析维生素进行 FDA营养标注的有效方法了。 ( 许多不同的传统分析方法可以分析单个或少量的维生素。其中大多数方法需要繁重 的,长时间的样品制备,而且是非特异性 的。由于不同维生素的化学性质不同,因此同时进行可靠的多种维生素分析是非常 困难的。而且由于维生素片中的浓度范围 较宽,从几微克到几十毫克,这样就使分析工作更加难以完成了。另外,某些维生素还具有稳定性、基质复杂性以及溶解性等问题。 ) ( 本文描述了一种简单、可靠的采用紫外检测同时测定10种水溶性维生素的方法,只需20分钟即可完成。 ) 方法 仪器和软件 ( 采用 Agilent 1260 Infinity 液相色谱系 统,包括以下部分: ) ( · Agilent 1260 系列四元泵和真空兑气 机(G1311B) ) ( · A gilent 1260 系列高效自动进样器 (G1367E) ) ( · Agilent 1260系列柱温箱 (G1316C) ) ( ·Agilent 1260 系列二级管阵列检测器 (G4212B),配置最大光强流通池(光程 60 mm) (G421260007) ) ( · Agilent Poroshell 120 EC-C18色谱柱 3.0 mm x150 mm, 2.7 p m(部件号 693975302) ) ( · 使用 Agilent 1 290 Infinity 液相色谱系 统开发并实验超高液相色谱分析方法 ) ( · Agilent 1290 Infinity 二元泵配备内置 的真空脱气机 (G4220 A) 以及 100 pL Jet Weaver混合器 ) ( · Agilent 1290 Infinity 高效自动进样器 (G4226A) ) ( · A gilent 1290 Infinity 柱温箱 (G1316C) ) ( · Agilent 1290 Infinity二级管阵列检测 器 (G4212A),配置最大光强流通池(体 积1.0pL,光程10mm) (G421260008) ) ( · A gilent Poroshell 120 EC-C18色谱柱, 内径2.1 mm, 长75 mm, 采用 2.7 pm 粒径料填装(部件号697775902) ) ( 两个系统控制都采用 Agilent ChemStationB.04.02软件。 ) 试剂和材料 ( 所有的化合物和溶剂均为色谱级纯度,超 纯水使用Milli Q 水纯化系统 (MilliporeElix 10 model, USA) 制得。乙腈梯度级别, 购自 L a bScan 公司 (B a ngkok, Th a iland)。 ) ( 磷酸氢二钾购自 Fluka 公司 (Germany)。 磷酸购自 Fluka 公司 (Switzerland),氢氧化钠购自 Sigma 公司 (Germany)。标准样 品抗坏血酸(C)、烟 酸 (B3)、泛酸钙(B5)、 吡哆醇(B6)、烟酸胺(B3)、硫胺(B)、叶酸 (B9)、生物素(B7)、氰钴胺(B12)和核黄 素(B2)购自Aldrich 公司 (India)。 ) 色谱参数 反相液相色谱和超高液相色谱仪的色谱参数列于表1中。 水溶性维生素标准品 维生素标准品抗坏血酸,烟酸,泛酸钙,吡哆醇,烟酸胺,硫胺,叶酸,生物素,氰钴胺和核黄素的配制:分别准确确量50mg 左右的维生素粉末,转移到 25mL 标准容量瓶。用Milli Q水,定容配成 2.0 mg/mL(2000 ppm) 的贮备液。如有需要,超声溶解。作为游离酸叶酸水溶性很差。需要将叶酸转化成叶酸盐,首先将标准品溶于 20 mL Milli Q水,后滴加 0.25M氢氧化钠至叶酸刚好转化成叶酸钠为止。然后使用 Milli Q 水配制成浓度为2.0 mg/mL 的溶液。采用相似的方法制备生物素和核黄素标准溶液。不用时, 水溶性维生素的贮备液保存于+4.0°C。取每种标准品品液大概200 pL 混合制成 2000 pL 水溶性维生素的添加混标,其中每个组分浓度200ppm。使用200ppm 的添加混标和流动相A稀释配制得到不同线性浓度。 样品制备 将某一欧洲重要品牌的三个复合维生素片分别溶于200mL水,超声。加入最少量的 0.25 M NaOH 以解决某些维生素的溶解性问题。之后使用00.25 pm 安捷伦Econofilter 注射过滤器过滤样品溶液,用于营养标注和回收率分析。 参数 Agilent 1260 Infinity 液相色谱 Agilent 1290 Infinity 液相色谱 柱温 35°C 35°C 采集速率 20 Hz 80 Hz 数据采集波长 205,214,220, 232,266, 268, 280 nm 205, 214, 220,232,266, 268, 280 nm 流通池 60 mm 光程 10 mm 光程 进样量 5pL(进样针清洗,冲洗口活化5秒) 1pL(进样针清洗,冲洗口活化3秒) 恒温进样器 5°℃ 5°℃ 流动相A 25 mM HK,POq, pH 7.0 25mMHK,PO4, pH 7.0 流动相B 乙腈 乙腈 梯度 0 min 时 →1%B 0 min 时→1%B 5 min 时 →1%B 0.56 min 时→1%B 15 min 时 →30%B 1.66 min 时→30%B 20 min 时 →30%B 2.2 min 时→30%B 20.1 min 时→1%B 2.22 min 时→1%B 后运行时间 5 minutes 1 minute 流速 0.45 mL/min 1.0 mL/min Agilent 1260 Infinity 液相色谱系统和 1290 Infinity液相色谱系统所用的色谱参数 贮备方法 维生素对光和热很敏感。为了增加溶液稳定性,将所有溶液贮存于冰箱。恒温自动进样器分析时保持4℃。 步骤 进样5pL流动相A作为空白,之后对每个线性浓度进行分析,每个浓度重复进样六次。计算每个浓度的峰面积和保留时间(RT) 的标准偏差 (SD) 和相对标准偏差(RSD)。用较低的线性浓度确定 LOD 和LOQ。用每个线性浓度的平均面积对浓度作图得到线性曲线。 改变方法的六个关键参数评估方法的耐用性。对 5 ppm 添加混标六次重复进样,记录数据用于耐用性测定。 三个复合维生素片样品分别在添加和不添加 5 ppm 混标的条件下三次重复进样。峰面积和保留时间用来回收率和营养标注计算。 使用安捷伦方法转换软件可将该方法有效转移到超高液相色谱仪上。评估了每种维生素的 LOD, LOQ以及线性,用峰面积和保留时间 RSD 建立了方法的准确度。 结果和讨论分离和检测 用不同流动相在不同梯度和等梯度条件下分析添加混标。发现用25 mMK2HP04 pH 7梯度分离得到最好的分离度。图1表示使用 Agilent Poroshell 120EC-C18,150 mm ×3.0 mm, 2.7 pm色谱柱在20分钟内就分离10种水溶性维生素,分离度优异。由于这些维生素的结构不同,因而每种维生素的谱图和最大吸收也不同。抗坏血酸在266nm 有强吸收,而叶酸的最大吸收在 280 nm。生物素和泛酸钙的 UV 吸收很差,因此选择205nm 波长用于分析。烟酸,烟酸胺和氰钴胺的最大吸收波长在214 nm。而吡哆醇最大吸收大约在220nm。硫胺分析选择232nm, 核黄素的分析选择 268nm。图1是7个不同波长下的色谱叠加图。可以很清楚的看到在不同采集波长下每种维生素峰高的变化。梯度运行时基线吸收会发生变化,这是因为流动相中的缓冲液的量发生了变化。较低波长条件下这个现象更加明显,这就解释了 205 nm波长下的基线漂移。ChemStation 软件的高级特性使其能够查看每个峰的纯度以及评估方法的特异性。本文中采用准确性、线性范围、精确性、特异性、回收率以及耐用性研究来评估这一方法。 图1 线性 每种维生素都建立了从 LOQ到最大浓度的线性曲线,结果列于表2。每个线性浓度重复进样六次,采用峰面积平均值绘制线性曲线。这一线性范围覆盖了大多数复合维生素片中维生素的含量。图3所示为生物素的线性曲线。除了抗坏血酸之外,所有维生素的回归系数都很高。在溶液中,由于溶解氧的含量不同抗坏血酸与它的脱氢氧化态之间存在一个可逆平衡1,2,3。降低流动相的 pH 到酸性范围可使这一反应最小化。叶酸会在较低 pH下沉淀,因此不能保持酸性 pH。抗坏血酸的峰面积响应重现性不一致,因此抗坏血酸R2值较低。表2包括 LOD, LOQ 和线性结果。 图3 生物素的线性曲线,浓度范围从5 ng/mL 到 500 ng/mL, 线性系数很高 LOD L0Q 线性范围 浓度 SI no: 名称: ng/pL (ppm) S/N ng/uL (ppm) S/N (ppm)浓度范围 R2值 n =6 1 抗坏血酸 1 4.8 2.5 9.7 2.5-500 0.9827 8 2 烟酸 0.025 3.1 0.05 10.9 0.05-250 1 12 3 泛酸钙 1 5.0 2.5 12.6 2.5-500 0.9998 8 4 吡哆醇 0.025 4.4 0.05 9.9 0.05-250 0.9994 12 5 烟酸胺 0.025 4.8 0.05 9.8 0.05-250 1 12 6 硫胺 0.025 3.1 0.1 9.9 0.1-250 1 11 7 烟酸 0.01 4.7 0.025 10.3 0.025-250 0.9985 13 8 生物素 2.5 4.2 5 9.7 5-500 0.9999 7 9 氰钴胺 0.01 6.4 0.025 15.2 0.025-250 0.9994 13 10 核黄素 0.005 8.1 0.01 12.4 0.01-250 0.9985 14 表2 全部10种维生素的 LOD, LOQ, S/N 和线性结果 保留时间和峰面积的准确性 全部10种维生素在不同线性浓度下保留时间的 RSD 均小于0.65%。除了抗坏血酸之外,所有维生素不同线性浓度下的峰面积 RSD 都很小。由于抗坏血酸峰面积不稳定,其峰面积在一段时间内不能测量一致。最小的峰面积和保留时间 RSD 值保证了该方法的重现性以及系统的准确性是可以接受的。图4和图5分别代表了一些维生素的峰面积和保留时间 RSD. 图4 不同维生素不同浓度下峰面积的准确度,每个浓度重复进样六次 图5 不同维生素保留时间的准确度,每个浓度重复进样六次 观测到的保留时间偏差 观测到的峰面积偏差 Sl no: 参数 原始方法值 测量偏差 改进值 (允许范围=±2%) (允许范围=±5%) 1 柱温 35°C ±5% 33°C 通过 通过 37 °C 三种中度洗脱 通过 化合物未通过 2 色谱柱流速 0.45 mL/min ±2% 0.44 mL/min 最后洗脱的五 种化合物通过 通过 0.46 mL/min 最后洗脱的五 种化合物通过 通过 3 进样量 5 pL ±5% 4.75 pL 通过 通过 5.25 pL 通过 通过 4 梯度斜度 2.9(在10分钟的 10% 3.2(在9分钟的 最先洗脱的八 通过 时间内从1到30) 时间内从1到30) 种化合物通过 2.6(在11分钟的 最先洗脱的八 通过 时间内从1到30) 种化合物通过 5 检测波长 205,214,220, ±3nm 202,211,217,229, 通过 七种化合物通过 232,266,268, 263,265, 277nm 280 nm 208, 217,223,235, 通过 五种化合物通过 269,271,283nm 6 流动相 pH 7.0 ±0.2 6.8 未通过 未通过 7.2 未通过 未通过 耐用性 使用 10 ng/mL 的维生素添加混标测试方法耐用性。进样量设为5pL,该混标的柱上浓度是 50 ng/mL (ppm)。改变六个关键参数,10次重复进样采集数据。取最后六次的重复数据用于分析。保留时间和峰面积允许的偏差分别设定为±2.0%和±5%。 耐用性测试的结果总结于表3。结果清楚表示准确选择最大吸收波长对维生素测定非常重要。一些维生素的峰面积对检测波长的改变非常敏感,仅仅增加或减少3nm,响应变化就非常明显。考察了柱温对保留时间的影响,发现当柱温比实际方法低2℃(33°C)时,偏差在允许范围内。当柱温比实际方法高2℃(37°C),三个中度洗脱峰的保留时间时偏差就会 图6 图7 回收率(%) 样品1 样品2 样品3 维生素 R2 线性方程 样品1 稀释 样品2 稀释 样品3 稀释 烟酸 1 y=44.956x+9.8116 95.4 96.3 94.2 99.1 97.5 95.1 泛酸钙 0.9998 y=8.1153x+13.278 84.2 93.4 92.0 92.0 86.4 80.2 吡哆醇 0.9994 v=64.275x-102.77 125.3 96.3 123.6 98.1 125.7 94.5 烟酸胺 1 y=51.034x+6.7257 96.9 100.0 99.6 98.3 100.1 87.0 硫胺 1 y=23.202x-8.8965 100.7 99.7 100.6 102.3 99.2 98.0 叶酸 0.9985 y=38.06x+42.787 80.8 82.2 81.6 85.1 82.3 81.8 生物素 0.9999 v=7.3515x+10.517 82.2 94.8 80.4 96.3 84.0 95.6 氰钴胺 0.9994 y=31.164x+31.428 84.9 83.8 85.6 87.3 80.5 83.0 核黄素 0.9985 v=50.904x+71.323 82.7 82.2 81.6 85.4 84.1 80.6 营养标注 在本研究中,用色谱方法计算复合维生素片中的维生素含量,并与标签上的浓度进行了对比。在复合维生素片溶于200 mL 水后进行了三次重复分析。因为维生素具有很宽的浓度范围,所以也进行了稀释样品分析。抗坏血酸含量很高, 产生的色谱峰使检测器饱和。对于抗坏血酸,稀释样品的分析更准确,因为较低的峰高和峰面积在检测器的线性范围内。但在稀释样品中,检测不到一些微克级的维生素的峰。在样品的色谱分析中,没有检测到任何维生素峰的干扰。在样品和稀释样品分析中,使用各维生 素峰的相应峰面积用于复合维生素片的营养标注分析。使用从线性曲线得到的线性方程进行计算。提取步骤非常简单,可用于常规分析。正如标签所示,样品中没有烟酸(B3的酸形式),因此在样品色谱图中也未见烟酸的峰。这些结果表明该方法适用于复合维生素片中维生素的定量分析。 复合维生素片1 复合维生素片2 复合维生素片3 维生素 标注含量 未稀释 稀释 未稀释 稀释 未稀释 稀释 抗坏血酸 (C) 80 mg 饱和峰 201.7 饱和峰 203.7 饱和峰 198.7 泛酸钙(B5) 6 mg 6.7 6.1 6.6 6.5 6.6 6.3 吡哆醇 (B6) 1.4 mg 1.2 1.2 1.2 1.2 1.2 1.2 烟酸胺(B3) 16 mg 15.7 16.0 15.4 16.0 15.2 15.6 硫胺 (B1) 1.1 mg 1.3 1.3 1.3 1.3 1.2 1.2 叶酸 (B9) 200 pg 114.9 117.6 114.3 120.6 115.3 121.0 生物素 (B7) 50 pg 42.4 35.7 38.5 氰钴胺(B12) 2.5 pg 0.5 0.4 0.4 核黄素(B2) 1.4 mg 1.4 1.4 1.3 超高液相色谱方法 使用安捷伦方法转换软件建立了配备二级管阵列检测器的超高液相色谱的方法来分离水溶性维生素。该软件能很容易将二元或四元泵系统的方法转换为适合Agilent 1290 Infinity 液相色谱系统的优化方法。转换的超高液相色谱方法分析速度很快,相对于20分钟的较长梯度,它能节省90%的分析时间和70%的溶剂。表现出良好的分离度和优异的峰形(图8)。这种方法也可以用于维生素片的快速营养标注分析。建立了 LOD 和 LOQ,同样使用超高液相色谱方法对每种维生素的线性进行了评估。峰面积和保留时间的 RSD 较低,证明了方法的准确度。表6列出了实验的LOD,LOQ.图9的例子表现出良好的线性,图10表示的是保留时间和峰面积的RSD 值,柱上浓度50 ppm,羊样量1pL。结果证明了超高液相色谱方法快速、灵敏、可靠。 图8 使用75mm 的 Agilent Poroshell 120 EC-C18 色谱柱和超高液相色谱方法分离10种水溶性维生素。不同检测波长采集的色谱叠加图 LOD L0Q SINo: 名称: 浓度(ppm) S/N 浓度(ppm) S/N 1 烟酸 0.02 4.3 0.05 12.8 2 泛酸钙 0.5 4.2 1.0 11.3 3 吡哆醇 0.05 5.3 0.1 9.6 4 烟酸胺 0.05 4.3 0.1 11.1 5 硫胺 0.1 3.1 0.5 11.3 6 叶酸 0.02 3.1 0.1 16.3 7 生物素 0.5 5.3 1 16.5 8 氰钴胺 0.002 3.9 0.005 10.2 9 核黄素 0.02 3.5 0.05 9.6 表6 超高液相色谱方法的 LOD 和 LOQ值 结论 采用 Agilent Poroshell 120 EC-C18色谱柱分离和定量分析了多维片中的水溶性维生素。使用 Agilent 1260 Infinity 液相色谱系统建立了一种耐用的反相液相色谱方法,只需20分钟即可完成分析。用安捷伦方法转换软件将其有效地转换为只需2分钟的超高液相色谱方法。使用Agilent 1290 Infinity 液相色谱系统进行了超高液相色谱分析。尽管每次进样的浓度范围不同,还是可以将该方法成功的用于维生素 C、B1、B2、B3、B5、B6、B7、B9和B12的定量分析。梯度洗脱能够确保更好的色谱分离度,提高灵敏度并减少基质干扰。该方法简单、特异、灵敏、快速,并能提供良好的准确度、线性和回收率。它可以简单有效的用于复合维生素片中上述水溶性维生素的常规分析。 图9 核黄素线性曲线,浓度范围从0.05 ppm 到 200 ppm, 相关系数 0.99999(12个浓度,六次重复进样)进样量1 pL 图10 全部10种维生素(柱上浓度 50ppm) 超高液相色谱分析的峰面积和保留时间 RSD。 进样量1pL,六次重复进样 参考文献 1. Katherine E. Sharpless, Sam Margolis,Jeanice Brown Thomas,“Determination of vitamins in food-matrix Standard Reference Materials,"FINational Institute of Standards andTechnology, 100 Bureau Drive, Stop8392, Gaithersburg, MD 20899-8392,USA 2. A. Jedlicka and J. Klimes,"Determination of Water-and Fat-Soluble Vitamins in Different MatricesUsing High-Performance LiquidChromatography," Chem. Pap.,2005, 59,202-222. 3. Sam A. Margolis, David L Duewer,"Measurement of Ascorbic Acid inHuman Plasma and Serum: Stability,Intralaboratory Repeatability,andInterlaboratory Reproducibility," ClinicalChemistry, 1996, 42, 1257-1262. 4.A0AC Official Method 2004.07 VitaminB6 in Reconstituted Infant FormulaLiquid Chromatographic Method FirstAction 2004. 5.Duncan Thorburn Burns, Klaus Danzer,and Alan Townshend, “Use of theterms recovery'and 'apparentrecovery'in analytical procedures,"Pure Appl. Chem., Vol.74, No. 11, pp.2201-2205,2002. www.agilent.com/chem/lc 安捷伦科技(中国)有限公司, 2011 2011年6月1日 ( 出版号5990-7950CHCN ) Agilent Technologies Agilent Technologies 在本应用报告中描述了一种定性和定量分析水溶性维生素的应用解决方案。开发了一种单一、耐用的反相高效液相色谱(RP-HPLC) 方法,与其他的许多传统方法只能对各组分单独定量分析不同,本方法可以同时测定10 种不同维生素。使用Agilent Poroshell EC-C18 色谱柱和Agilent 1260 Infinity 液相色谱系统可以实现分离和定量。在波长 200-640 nm 的范围内可以使用二极管阵列监测器(DAD) 进行检测。因为不同维生素的最大吸收波长不同,故需要在8 种不同的波长下进行数据采集。这种方法部分有效,适用于复合维生素片的常规营养标注分析。建立了每种维生素的检测限(LOD),定量限(LOQ) 和线性范围。使用安捷伦方法转换软件还可以将该方法有效的转换成较快的使用 Agilent 1290 Infinity 液相色谱系统的超高压液相色谱(UHPLC) 方法。
关闭-
1/12
-
2/12

还剩10页未读,是否继续阅读?
继续免费阅读全文产品配置单
安捷伦科技(中国)有限公司为您提供《复合维生素片中吡哆醇检测方案(液相色谱仪)》,该方案主要用于其他特殊膳食产品中营养成分检测,参考标准《暂无》,《复合维生素片中吡哆醇检测方案(液相色谱仪)》用到的仪器有Agilent 1260 Infinity II 液相色谱系统、Agilent 1290 Infinity II Multisampler、OpenLAB 软件。
我要纠错
推荐专场
相关方案













 咨询
咨询

