方案详情文
智能文字提取功能测试中
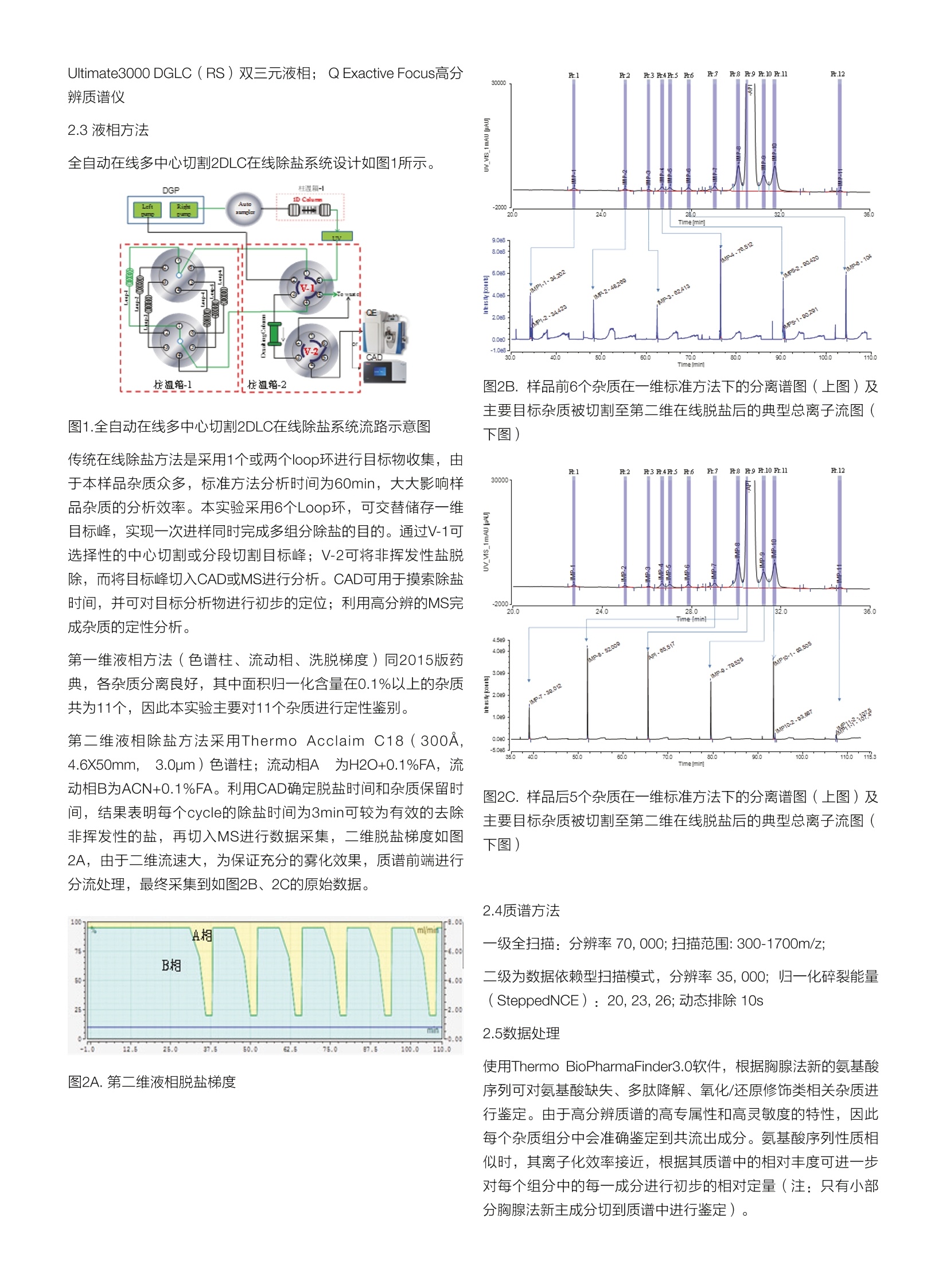
thermoscientific 基于双三元液相高通量在线除盐技术与Orbitrap高分辨质谱联用在合成类多肽药物杂质鉴定中的应用 孙佳楠张艳海赛默飞世尔科技(中国)有限公司色谱质谱部 关键词: 双三元液相色谱,在线多组分中心切割二维除盐技术, Q Exactive Focus,合成多肽杂质鉴定 前言 根据美国药典(USP)定义,多肽药物指在不考虑工艺的条件下,氨基酸数目≤40属于多肽药物;当采用化学合成方法制备时,其多肽药物指氨基酸数目<100。多肽类药物的制备目前主要有化学合成、基因重组和从动植物中提取三种方法,其中固相多肽合成技术的产生极大推动了多肽药物的发展。多肽药物在合成和储存的过程中,容易形成结构相关杂质,杂质的类型主要分为两类,一类为固相合成工艺相关的杂质,如氨基酸的丢失、氨基酸插入、保护基残留、氧化/还原以及残留溶剂、试剂、无机杂质等;另一类来源多肽的降解,如β-消除反应、焦谷氨酸和琥珀酰亚胺的形成。许多结构相关杂质不但没有药物疗效,反而具有一定的毒副作用。欧盟药典规定需对含量在0.5%以上的相关结构杂质进行定性分析,对含量在1%以上的结构相关杂质进行定量分析并考察其毒副作用,美国药典也有类似规定[1][2],因此在多肽药物开发阶段控制杂质的性质及含 量至关重要。 胸腺法新是化学合成的由28个氨基酸组成的多肽,相对分子质量3108.28。注射用胸腺法新是胸腺法新加适量赋形剂制成的无菌冻干粉针,主要用于治疗慢性乙肝、丙肝,也可与其他药物联用治疗肿瘤、免疫缺陷等疾病。目前胸腺法新的合成方法主要为固相合成多肽法,合成步骤烦琐,易产生与胸腺法新结构类似的杂质。2015版中国药典采用LC-UV主成分自身对照法对单个杂质和杂质总量进行了规定,当相关的杂质高于0.1%时需要体现,高于0.5%时需要进行杂质鉴定,高于1%时则需要对杂质精确定量,总杂质的含量要小于5%。液质联用技 术因其快速、高灵敏度和高专属性的分析能力,已经被广泛的应用于药物杂质鉴定,但药典LC方法中流动相为硫酸铵缓冲液-乙腈条件,硫酸铵缓冲液与质谱不兼容,因此当进行杂质鉴定时,传统方法需对目标杂质峰进行收集、富集、除盐、旋干再鉴定,过程繁琐、且增加了杂质成分降解等不确定影响因素[2] 本篇利用赛默飞特色的双三元液相色谱在线多组分中心切割二维除盐方法,可实现一次进样同时完成多组分除盐的目的,电雾式检测器(CAD)作为一种通用型检测器可辅助建立除盐方法,评价除盐效果。在确定了二维除盐条件后,利用Orbitrap高分辨质谱的高分辨率、出色的灵敏度、高质量精度等优势性能,实现对未知杂质组分的快速精确鉴定。大大的提升了样品的稳定性和分析效率,本实验结果为多肽药物的质量评价提供重要参考,同时为其纯化工艺和储存条件的优化提供重要的指导。 2.1样品信息 国内某厂家在研胸腺法新多肽药物,采用1mL pH=7的磷酸盐溶解,并稀稀3倍,制成浓度为0.53mg/mL样品溶液,直接进样20pL分析(同2015版药典)。 2.2仪器型号 全自动在线多中心切割2DLC在线除盐系统设计如图1所示。 图1.全自动在线多中心切割2DLC在线除盐系统流路示意图 传统在线除盐方法是采用1个或两个loop环进行目标物收集,由于本样品杂质众多,标准方法分析时间为60min,大大影响样品杂质的分析效率。本实验采用6个Loop环,可交替储存一维目标峰,实现一次进样同时完成多组分除盐的目的。通过V-1可选择性的中心切割或分段切割目标峰;;VV-2可将非挥发性盐脱除,而将目标峰切入CAD或MS进行分析。CAD可用于摸索除盐时间,并可对目标分析物进行初步的定位;利用高分辨的MS完成杂质的定性分析。 第一维液相方法(色谱柱、流动相、洗脱梯度)同2015版药典,各杂质分离良好,其中面积归一化含量在0.1%以上的杂质共为11个,因此本实验主要对11个杂质进行定性鉴别。 第二维液相除盐方法采用Thermo Acclaim C18(300A,4.6X50mm.3.0um)色谱柱;流动相A 为H2O+0.1%FA, 流动相B为ACN+0.1%FA。利用CAD确定脱盐时间和杂质保留时间,结果表明每个cycle的除盐时间为3min可较为有效的去除非挥发性的盐,再切入MS进行数据采集,二维脱盐梯度如图2A, 由于二维流速大,为保证充分的雾化效果,质谱前端进行分流处理,最终采集到如图2B、2C的原始数据。 图2A.第二维液相脱盐梯度 图2B.样品前6个杂质在一维标准方法下的分离谱图(上图)及主要目标杂质被切割至第二维在线脱盐后的典型总离子流图(下图) 图2C.样品后5个杂质在一维标准方法下的分离谱图(上图)及主要目标杂质被切割至第二维在线脱盐后的典型总离子流图(下图) 2.4质谱方法 一级全扫描:分辨率 70,000;扫描范围:300-1700m/z; 二级为数据依赖型扫描模式,分辨率35,000;归一化碎裂能量(SteppedNCE): 20,23,26;动态排除 10s 2.5数据处理 使用Thermo BioPharmaFinder3.0软件,根据胸腺法新的氨基酸序列可对氨基酸缺失、多肽降解、氧化/还原修饰类相关杂质进行鉴定。由于高分辨质谱的高专属性和高灵敏度的特性,因此每个杂质组分中会准确鉴定到共流出成分。氨基酸序列性质相似时,其离子化效率接近,根据其质谱中的相对丰度可进一步对每个组分中的每一成分进行初步的相对定量(注:只有小部分胸腺法新主成分切到质谱中进行鉴定)。 三、实验结果与讨论 1-6杂质组分的鉴定结果如图3A,展示每一个不同保留时间杂质峰中含量最高的杂质成分,如鉴定到S1-N28的非乙酰化杂质、N端或C端氨基酸的缺失及S1-N28乙酰化二聚体等形式;7-11组分的鉴定结果如图3B。每个杂质成分的质谱一级质量偏差均小于2ppm,且含有丰富的二级碎片进行精确确认鉴定序列。以杂质A3-N28(保留时间在34.2min)为例,其一级质量偏差为0.16ppm,且每一个氨基酸均有二级碎片进行确证如图3C。 12345678910 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 Color code for signal intensity>2.1e+06>5.2e+05>1.3e+05>3.2e+04>7.8e+03 图3A.杂质组分1-6的鉴定结果;不同长度的条码代表覆盖氨基酸的数目和位置,不同颜色表示其在质谱中的响应,条码上的数字表示该肽段的色谱保留时间; 1234567 8 910 11 12 1314 15 16 17 18 19 20 21222324 25 26 27 28 Color code for signal intensity>8.8e+05>4.3e+05>2.1e+05>1.0e+05>5.0e+04 图3B.5.杂质组分7-11的鉴定结果;不同长度的条码代表覆盖氨基酸的数目和位置,不同颜色表示其在质谱中的响应,条码上的数字表示该肽段的色谱保留时间; F: FTMS+pESi d Full ms2 716.8670@hcd23.00[110.0000-2945.0000] TIC: 2.19e+008 Experimental (+4, w=1.8,r=35000, QExactive) 图3C.杂质A3-N28的一级同位素峰的分布,及其匹配到的二级碎片离子 此外, Orbitrap高分辨率质谱仪具有高灵敏度的优势,如在上一cycle中杂质未洗脱完全或存在异构体时,那么在下一组分中仍鉴定到同一杂质,因此需综合所有组分结果进行精确判定。 另外在对多肽药物纯化工艺和储存条件进行考察时,本实验亦建立了LC-MS直接分析方法,样品使用水复溶后,利用质谱前端六通阀对样品进行除盐,有效梯度为30min,三次技术重复,可高可信度的获得样品中氨基酸缺失类及修饰类杂质信息,如图4鉴定结果及其相对含量信息,为纯化工艺和储存条件的优化提供依据。 NO Peptide Sequence Modification ISDAAVD Acetylation 2 LKEKKEVVEEAEN None 33 ISDAAVDTS Acetylation 4 ISDAAVDTSS Acetylation 5 SDAAVDT Acetylation 6 TSSEITTKDLKEKKEVVEEAEN 2x 7 TSSEITTKDLKEKKEVVEEAEN None 8 VDTSSEITTKDLKEKKEVVEEAEN None 9 AVDTSSEITTKDLKEKKEVVEEAEN None 10 AAVDTSSEITTKDLKEKKEVVEEAEN 2x 11 AAVDTSSEITTKDLKEKKEVVEEAEN None 12 ISDAAVDTSSEITTKDLKEKKE 13SDAAVDTSSEITTKDLKEKKEVVEEAEN Acetvlation Acetylation 14SDAAVDTSSEITTKD Acetylation 15 SDAAVDTSSEITTKDLKEKKEVVEEAEN 2x 16 SDAAVDTSSEITTKDLKEKKEVVEEAEN None 17 SDAAVDTSSEITTKDLKEKKEV Acetylation 18 SDAAVDTSSEITTKDLKEK Acetylation 19 SDAAVDTSSEITTKDLKEKKEVVEEA Acetylation 20 DAAVDTSSEITTKDLKEKKEVVEEAEN Acetylation 21 SDAAVDTSSEITTKDLK Acetylation 主成分 Thymalfasin_new Color code for signal intensity>7.7e+06 >1.2e+06 >1.9e+05 >3.0e+044.7e+03 图4.将胸腺法新直接进入LC-MS分析,获得其中氨基酸缺失类杂质的定性和相对定量信息; ( 热线8008105118 电话400 6505118 www.thermofisher.com ) ( 仅用于研究目的。不可用于 诊 断目的。◎ 2 018 Thermo Fisher Scientific Inc. 保留 所 有权利。所有商标均为 Thermo Fisher Scientific Inc. 及其子公司的资产,除 非 另有指明 。 ) Orbitrap高分辨质谱仪具有高灵敏度、高分辨率、高准确度和高稳定性的优势性能,与液相色谱联用可实现对多肽药物氨基酸序列的确证、氨基酸修饰的定性和定量,多肽药物杂质的鉴定和定量,以及多肽药物的动力学研究。本实验采用在线多组分中心切割二维除盐方法,一次进样完成了多目标杂质的在线除盐,显著的改善了分析效率,与Orbitrap高分辨质谱联用,强强联合,提高了杂质鉴定的通量和准确度。 ( 参考文献 ) ( [1]陈松辉,李明,李红梅,等.合成多肽药物中相关结构杂质分析 综述 Review on Analysis of Re l ated Structure Impurities in Syn-thetic Peptide M edicines[J]. Advances in A n alytical Chemistry,2016, 6(03):43. ) ( [2] 程磊,唐洋明,殷果,等. HPLC法对胸腺法新及其制剂中杂质 检查[J].药物分析杂志,2013(11):1942-1947. ) ( [3] D’ hondt, Matthias, et al. "Related i mpurities in peptide me-dicines."Journal of pharmaceutical and biomedical analysis 101(2014):2-30. ) 根据美国药典(USP)定义,多肽药物指在不考虑工艺的条件下,氨基酸数目≤40属于多肽药物;当采用化学合成方法制备时,其多肽药物指氨基酸数目<100。多肽类药物的制备目前主要有化学合成、基因重组和从动植物中提取三种方法,其中固相多肽合成技术的产生极大推动了多肽药物的发展。多肽药物在合成和储存的过程中,容易形成结构相关杂质,杂质的类型主要分为两类,一类为固相合成工艺相关的杂质,如氨基酸的丢失、氨基酸插入、保护基残留、氧化/还原以及残留溶剂、试剂、无机杂质等;另一类来源多肽的降解,如β-消除反应、焦谷氨酸和琥珀酰亚胺的形成。许多结构相关杂质不但没有药物疗效,反而具有一定的毒副作用。欧盟药典规定需对含量在0.5%以上的相关结构杂质进行定性分析,对含量在1%以上的结构相关杂质进行定量分析并考察其毒副作用,美国药典也有类似规定[1][2],因此在多肽药物开发阶控制杂质的性质及含量至关重要。Orbitrap高分辨质谱仪具有高灵敏度、高分辨率、高准确度和高稳定性的优势性能,与液相色谱联用可实现对多肽药物氨基酸序列的确证、氨基酸修饰的定性和定量,多肽药物杂质的鉴定和定量,以及多肽药物的动力学研究。本实验采用在线多组分中心切割二维除盐方法,一次进样完成了多目标杂质的在线除盐,显著的改善了分析效率,与Orbitrap高分辨质谱联用,强强联合,提高了杂质鉴定的通量和准确度。
关闭-
1/4

-
2/4
还剩2页未读,是否继续阅读?
继续免费阅读全文产品配置单
赛默飞色谱与质谱为您提供《多肽药物中杂质鉴定检测方案(液相色谱仪)》,该方案主要用于生物药品药物研发中限度检查检测,参考标准《暂无》,《多肽药物中杂质鉴定检测方案(液相色谱仪)》用到的仪器有赛默飞UltiMate 3000快速分离四元系统液相色谱、赛默飞Q Exactive Focus LCMSMS 系统。
我要纠错
推荐专场
相关方案










 咨询
咨询
