细胞裂解液,腺相关病毒颗粒中病毒蛋白表达,病毒颗粒的电荷异质性检测方案(蛋白印迹仪)
检测样品 其他
检测项目 病毒蛋白表达,病毒颗粒的电荷异质性

 金牌会员
13 篇解决方案
金牌会员
13 篇解决方案
方案详情文
智能文字提取功能测试中
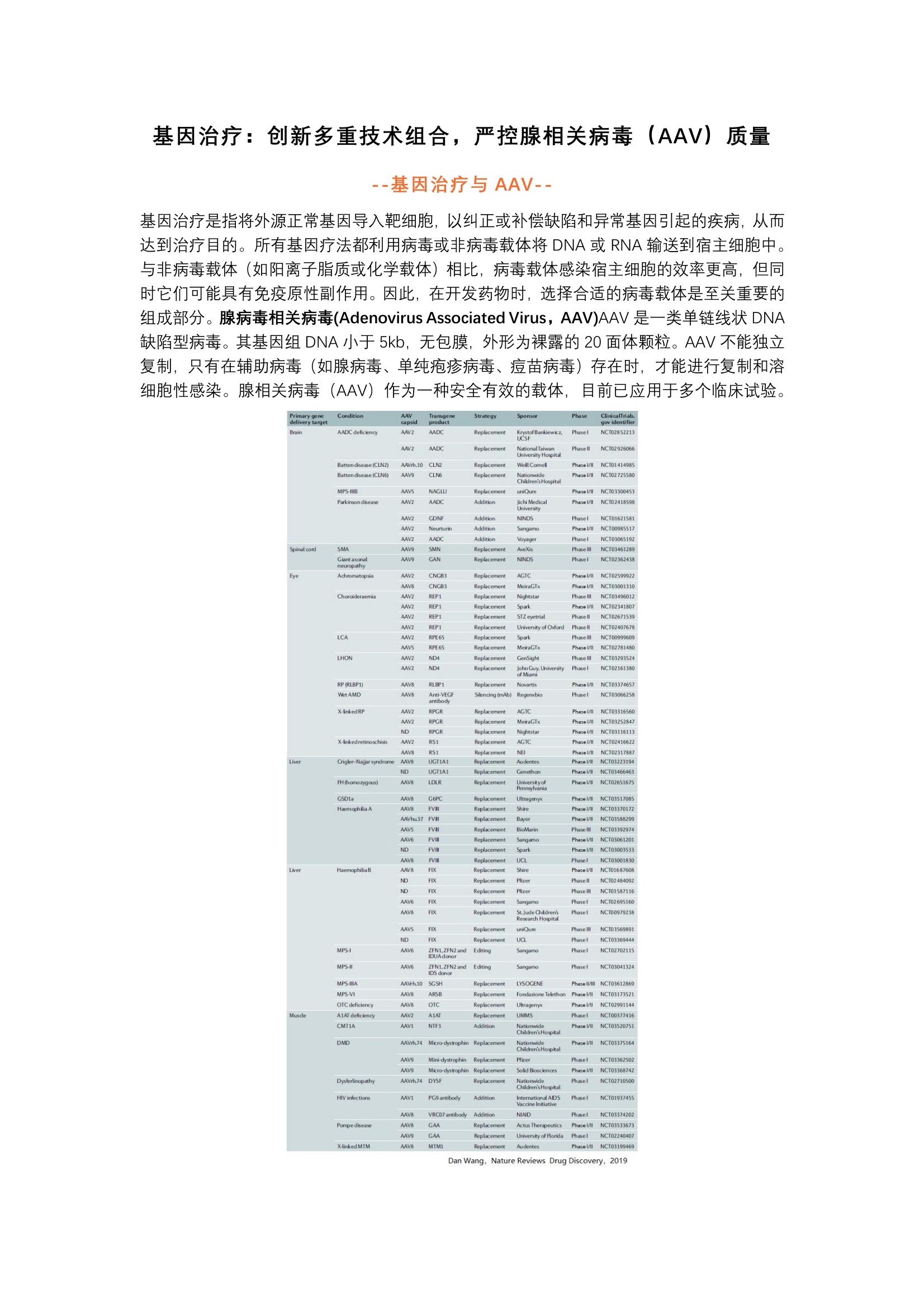
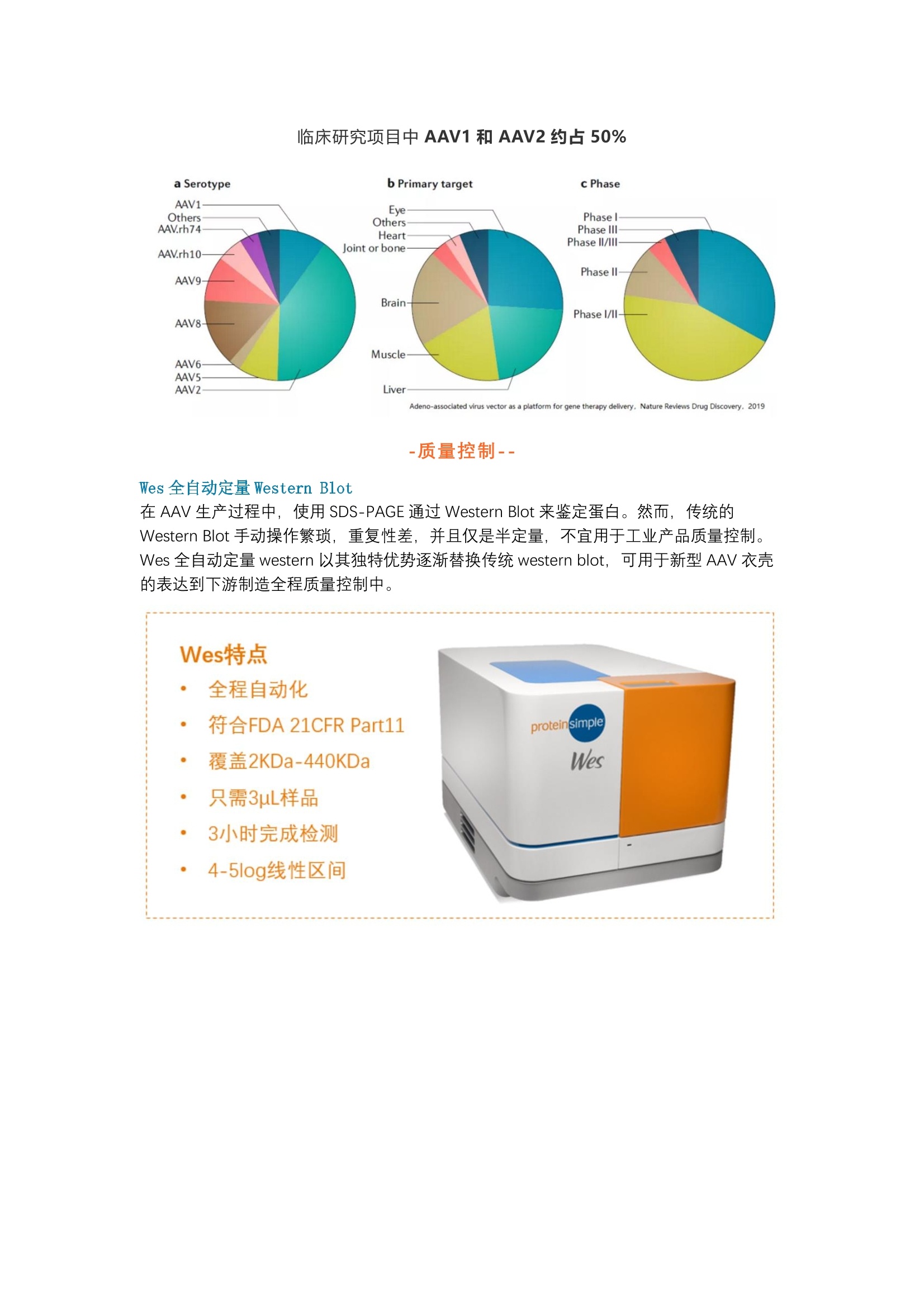
鉴定衣壳蛋白VP1/2/3 Inter-assay CV 基因治疗:创新多重技术组合,严控腺相关病毒(AAV) 质量 ·基因治疗与 AAV-- 基因治疗是指将外源正常基因导入靶细胞,以纠正或补偿缺陷和异常基因引起的疾病,从而达到治疗目的。所有基因疗法都利用病毒或非病毒载体将 DNA 或 RNA 输送到宿主细胞中。与非病毒载体(如阳离子脂质或化学载体)相比,病毒载体感染宿主细胞的效率更高,但同时它们可能具有免疫原性副作用。因此,在开发药物时,选择合适的病毒载体是至关重要的组成部分。腺病毒相关病毒(Adenovirus Associated Virus, AAV)AAV是一类单链线状 DNA缺陷型病毒。其基因组 DNA 小于 5kb, 无包膜,外形为裸露的20面体颗粒。AAV 不能独立复制,只有在辅助病毒(如腺病毒、单纯疱疹病毒、痘苗病毒)存在时,才能进行复制和溶细胞性感染。腺相关病毒(AAV) 作为一种安全有效的载体,目前已应用于多个临床试验。 Primary gene Condition AAV Transgene Strategy Sponsor Phase ClinicalTrials. Dan Wang, Nature Reviews Drug Discovery, 2019 临床研究项目中 AAV1和AAV2约占50% -质量控制-- Wes 全自动定量 Western Blot 在 AAV 生产过程中,使用SDS-PAGE 通过 Western Blot 来鉴定蛋白。然而,传统的Western Blot 手动操作繁琐,重复性差,并且仅是半定量,不宜用于工业产品质量控制。Wes 全自动定量 western 以其独特优势逐渐替换传统western blot,可用于新型 AAV 衣壳的表达到下游制造全程质量控制中。 FIGURE 1. (A) Immunodetection of VP1, VP2 and VP3 proteins during purification from whole-cell lysate. Detection was performed with an anti-AAVVP1/VP2/VP3 mouse monoclonal antibody. (B) Total protein detection of each fraction. Load: input material loaded onto the columns; flow-through: material not bound on columns; wash: wash buffer from columns; fractions: eluate fractions from columns; VR1616: ATCC purified referencematerial loaded as a positive control (low titer); cell lysate: HEK293 cell lysate (without virus); water: negative control. Sample dilutions are shown inbrackets.2筛选抗体1,000,000VP3 VP2 VP1800.000600,000Anti-AAV2VP1/VP2/VP3 mouse monoclonal400,000200,000030,000w 25,00020,00015,000Anti-AAV2VP1/VP2 mouse monoclonal10,0005,0000 30,00025,000 20.00015,000Anti-AAV2VP1 mouse monoclonal10,0005,0000 124066116180230MW (kDa)FIGURE 3. Antibody screen targeting VP1/VP2/P3 proteins (top panel),VP1/VP2 proteins (middle panel) and VP1 only (bottom panel).检测动态范围 FIGURE 4.Range of detection of the anti-AAVVP1/VP2/VP3mousemonoclonal antibody. (A) Lane view of VP1/VP2/VP3 detection of eachdilution. (B) Total peak area of VP1/VP2/VP3 by dilution factor. 将市售AAV2 (1x10" GC/mL, 33.8ug/mL)进行从1:8至1: 256的2X倍比稀释, Wes检测VP1/VP2/VP3。 Maurice 表征 AAV电荷异质性 与所有治疗药物一样,基因疗法,需要表征包装药物的递送载体电荷等。使用全柱成像毛细管等电聚焦电泳法((iclEF) 来表征 AAV 的电荷异质性,可以确保产品的稳定性和一致性。 Maurice 兼具 CE-SDS 和 iCIEF 双功能。两种功能均入选国家药典。 MauriceCE-SDS+iCIEF双功能效率为传统方法5倍自发荧光+紫外吸光度双模式自发荧光灵敏度为吸光度3-5倍免组装毛细管卡盒·方法入选国家药典 自发荧光和紫外吸光度比较 FIGURE 1. Apparent pl comparison of intact AAV2 and AAV6 particles. The intact AAV2 resolves as a single peak just below pl~9.0 (left)while the intact AAV6 resolves as 2 peaks at an apparent pl ~9.25 (right). Native fluorescence detection (bottom) was clearly more sensitivecompared to absorbance detection (top), making it possible to save precious sample when performing intact AAV analytics. Maurice 同时兼具紫外吸光度和自发荧光检测通道。与吸收检测相比,自发荧光的灵敏度高3-5倍,可以更好检测出 AAV 特征性异构体峰。因而自发荧光模式更适合 AAV 病毒电荷表征。 Intra-assay CV SAMPLE INTACTAAV2 AREA INTACT AAV6 AREA Injection1 47867 34711 Injection 2 43590 36932 Injection 3 47992 34636 Injection 4 46224.50 38318 Mean 1827.69 36149.25 %RSD 3.95 4.30 TABLE 1.1.Quantitative results from the quadruplicate injections ofintact AAV2 and AAV6 demonstrates the intra-assay reproducibilityof the intact AAV method.The results were very reproducible AAV2 和 AAV6 样品一式四份进样,检测 Intra-assay重现性(图2)。结果显示其高重现性: AAV2 和 AAV6的%RSD分别为3.95%和4.30%(表1)。 fluorescence exposure). AAV6样品三次独立实验,:每次实验三次重复,来检测Inter-assay 重现性(图3)。%RSD为6.6%(表2)。 变性 AAV 蛋白电荷表征 FIGURE 4. The denatured iclEF method for AAV2 is reproducible for both absorbance (left) and native fluorescence (right)detection within a run. Shown are overlays of three injections for both detection modes. Data generated with nativefluorescence detection had improved signal-to-noise ratios and baseline resolution compared to absorbance detection. AAV 病毒蛋白会进行几种翻译后修饰,包括糖基化和脱酰胺作用。应激引起的病毒蛋白脱酰胺作用可能导致载体活性,衣壳装配和转导效率降低。iclEF 方法通常用于监测由唾液酸化,糖基化和脱酰胺作用诱导的单克隆抗体的电荷异质性,因此对AAV 病毒蛋白也进行类似的评估。使用一式三份电泳图叠加使用吸光度和自发荧光检测法进行评估, AAV2 电荷变异体可以清晰分辨和重现(图4)。 灵敏度及线性 mL (left) and was detected with as little as 3x10" GC/mL AAV2 using native fluorescence detection. Strong linearity was also observed (right)across the titration range tested with an R? of 0.9956. 将变性的 AAV2 从一3x10”GC/mL 连续滴定至一3x10"GC/mL(图6)以建立方法的灵 敏度。该滴定范围内观察到很强的线性相关性, R²为0.9956。 监测 AAV 颗粒稳定性 FIGURE 7. Intact AAV6 analysis following incubation at varioustemperatures. After 10 minutes at 60 ℃, the AAV6 particle cannotbe observed and is no longer stable. The change in peak signatureafter stress-testing indicates Maurice can be used to monitor viralvector stability. 对完整的 AAV 样品进行温度压力测试,以确定是否可以使用 Maurice 监测病毒载体的稳定性或衣壳蛋白脱酰胺。AAV6 颗粒非常稳定,在37℃ 或 50C 下保持10分钟完整无缺。但是,当AAV6颗粒在60℃下10分钟时,不稳定。 监控AAV批间差 FIGURE 9. AAV6 lot-to-lot comparison. Five different lots of AAV6were analyzed using the intact method. All lots produced a similarprofile at pl~9.25, but only one lot had an additional peak at a lower pl. 利用 Maurice iclEF 天然荧光监测批次间变异,以鉴别病毒载体批间差别。五批不同的AAV6, 每批具有不同的基因组含量/mL (GC/mL), Maurice iclEF 自发荧光分析(图9)。 结果显示,所有五个批次在 pl一9.25左右均产生相似的峰形。但是,在一批中观察到了一个较低 pl 的附加峰,表明该样品与其他四批样品不同。 主要参考资料 1. Deamidation of amino acids on the surface of adeno-associated virus capsids leads tocharge heterogeneity and altered vector function, AR Giles, JJ Sims, KB Turner, L Govindasamy, MR Alvira, M Lock, JM Wilson, Mol Ther, 2018; 26(12):2848-2862. 2.Dan Wang, Phillip W. L. Tai and Guangping Gao,Adeno-associated virus vector as aplatform for gene therapy delivery, Nature Reviews Drug Discovery, 2019. 基因治疗是指将外源正常基因导入靶细胞,以纠正或补偿缺陷和异常基因引起的疾病,从而达到治疗目的。所有基因疗法都利用病毒或非病毒载体将DNA或RNA输送到宿主细胞中。与非病毒载体(如阳离子脂质或化学载体)相比,病毒载体感染宿主细胞的效率更高,但同时它们可能具有免疫原性副作用。因此,在开发药物时,选择合适的病毒载体是至关重要的组成部分。AAV是一类单链线状DNA缺陷型病毒。其基因组DNA小于5kb,无包膜,外形为裸露的20面体颗粒。AAV不能独立复制,只有在辅助病毒(如腺病毒、单纯疱疹病毒、痘苗病毒)存在时,才能进行复制和溶细胞性感染。腺相关病毒(AAV)作为一种安全有效的载体,目前已应用于多个临床试验。在AAV生产过程中,使用SDS-PAGE通过Western Blot来鉴定蛋白。然而,传统的Western Blot手动操作繁琐,重复性差,并且仅是半定量,不宜用于工业产品质量控制。Wes全自动定量western以其独特优势逐渐替换传统western blot,可用于新型AAV衣壳的表达到下游制造全程质量控制中。与所有治疗药物一样,基因疗法,需要表征包装药物的递送载体电荷等。使用全柱成像毛细管等电聚焦电泳法(icIEF)来表征AAV的电荷异质性,可以确保产品的稳定性和一致性。Maurice兼具CE-SDS和iCIEF双功能。
关闭-
1/7
-
2/7
还剩5页未读,是否继续阅读?
继续免费阅读全文产品配置单
ProteinSimple为您提供《细胞裂解液,腺相关病毒颗粒中病毒蛋白表达,病毒颗粒的电荷异质性检测方案(蛋白印迹仪)》,该方案主要用于其他中病毒蛋白表达,病毒颗粒的电荷异质性检测,参考标准《暂无》,《细胞裂解液,腺相关病毒颗粒中病毒蛋白表达,病毒颗粒的电荷异质性检测方案(蛋白印迹仪)》用到的仪器有Jess 全自动蛋白免疫印迹定量分析系统。
我要纠错
相关方案




 咨询
咨询

