磁性多壁碳纳米管固相萃取-气相色谱-质谱法检测水样中13种邻苯二甲酸酯类化合物
邻苯二甲酸酯类物质(Phthalic Acid Esters, PAEs)是广泛使用于塑料中的增塑剂,在聚氯乙烯中的添加量高达20 %~30 %[1]。它们在塑料中呈游离态,与塑料之间以氢键和范德华力联接[2],因而极易转移入大气、水、土壤、生物乃至人体,成为一种全球性的有机污染物[3]。PAEs具有类似雌激素的作用,干扰人体内正常的内分泌系统[4],并具有致癌、致畸、致突变性[5]。[F1] 因此,PAEs对环境的污染已经受到世界各国的普遍重视,世界上许多国家将其列入优先监测的黑名单[6]。美国环保署(EPA)将邻苯二甲酸二(2-乙基己基)酯(DEHP)等6种PAEs列为首选检测污染物[7],欧盟也将DEHP等6种PAEs认定为对人体和环境有害的物质[8]。我国地表水环境质量标准GB 3838-2002则将邻苯二甲酸二丁酯(DBP)和DEHP作为监测项目,并规定DBP不得超过3 μg/L,DEHP不得超过8 μg/L[9]。
目前,PAEs的检测方法主要有气相色谱法(Gas Chromatography, GC)[10][11]和高效液相色谱法(High Performance Liquid Chromatography, HPLC)[12][13]。由于PAEs不易溶于水,在水环境中的浓度一般只有10-9数量级,检测水中的这类物质必须使用预富集处理[14]。传统的液液萃取(LLE)富集方法使用有机溶剂一次或多次萃取PAEs,具有消耗溶剂量大,耗时长,费力,不易自动操作等缺点,而且大量的萃取液的浓缩又会给环境造成二次污染。[F2]
碳纳米管(Carbon Nanotubes, CNTs)是1991年发现的一种新型材料[15],因其独特的物理化学性质,已经迅速成为当前研究的热点[16]。CNTs是由石墨烯片卷成的无缝、中空的同轴圆柱体,可分为多壁碳纳米管(MWCNTs)和单壁碳纳米管(SWCNTs)两种,[F3] 由于具有纳米级别的中空管状结构、大的比表面积、表面官能团和疏水的表面,CNTs能强烈吸附某些重金属离子和有机化合物[17]。这一性质使得CNTs成为一种新的固相萃取(Solid Phase Extraction, SPE)吸附剂而广泛应用于分析领域[18]。研究发现,CNTs能选择性地吸附二恶英、苯、1,2-二氯苯和多环芳烃等具有苯环的化合物[16]。Cai等[18]以多壁碳纳米管(Multi-walled Carbon Nanotubes, MWCNTs)为SPE材料,结合高效液相色谱法,成功地分析水样中4种PAEs,发现其效果与C18、C8、PS-DVB等商业SPE吸附剂相当或更佳。
磁性碳纳米管是Fe3O4、γ-Fe2O3等具有磁性的纳米粒子沉积在CNTs上而形成的磁性复合材料。这种复合材料既具有磁性纳米粒子的铁磁性,又具有CNTs的优点,已经在材料[19]、生物[20-22]、医药[23]、环保[24,25]等各个领域显示了广阔的应用前景,然而,在分析领域却很少得到应用。
本文利用磁性MWCNTs具有磁性和强吸附性的特点,将其应用于水样中13种PAEs的富集,并结合气相色谱-质谱联用(GC-MS)技术进行分析检测。优化了萃取时间、水样pH值、解吸溶剂的种类、用量及解吸时间等实验条件,并将优化的实验条件用于实际水样的分析。本方法操作简便,省时,准确,灵敏,环保,适用于实际水样中PAEs的检测。
1 实验部分
1.1 仪器、试剂与材料
Shimadzu GCMS-QP2010 Plus 气质联用仪(日本岛津公司);ZHWY-200D多振幅高速轨道摇床(上海智城分析仪器制造有限公司);PB 203-N电子天平(上海梅特勒-托利多仪器有限公司);HH-S1恒温油浴锅(常州澳华仪器有限公司)。
邻苯二甲酸二丙基酯(DPrP,99.0%)、邻苯二甲酸二丁基酯(DBP,99.0%)、邻苯二甲酸二异丁基酯(DiBP,99.0%)、邻苯二甲酸二戊基酯(DPP,99.0%)、邻苯二甲酸二己基酯(DHxP,99.0%)、邻苯二甲酸二(2-乙基己基)酯(DEHP,99.0%)、邻苯二甲酸二苯基酯(DPhP,99.5%)、邻苯二甲酸二正辛基酯(DOP,97.5%)、邻苯二甲酸二环己基酯(DCHP,99.5%)、邻苯二甲酸丁基苄基酯(BBP,97.0%)、邻苯二甲酸二(丁氧基乙基)酯(DBEP,98.5%)、邻苯二甲酸二(乙氧基乙基)酯(DEEP,98.5%),邻苯二甲酸二异壬基酯(邻苯二甲酸二(3,5,5-三甲己基)酯,DiNP),均购自Dr. S. Ehernstorfer公司;MWCNTs(纯度>95 %,外径:40-60nm,长度:5-15 μm,比表面积:40-300 m2/g),购自深圳纳米科技有限公司;丙酮、甲醇、乙腈(HPLC),使用前重蒸;无水乙醇(A.R.);无水硫酸钠(A.R.),用前在马弗炉中350℃烧烤4h;FeCl3·6H2O(G.R.,99%);乙二醇(A.R.);三水合醋酸钠(A.R.);盐酸(A.R.)。实验用水为Mili-Q超纯水系统(Milipore,美国)纯化的纯净水。
1.2 标准溶液的配制
将13种PAEs标准品用丙酮配制成1.0 mg/mL的单标准储备液,保存于4℃的冰箱中,使用前将上述单标准储备液用丙酮稀释配制成100 μg/mL的混合标准使用液。
1.3 实验方法
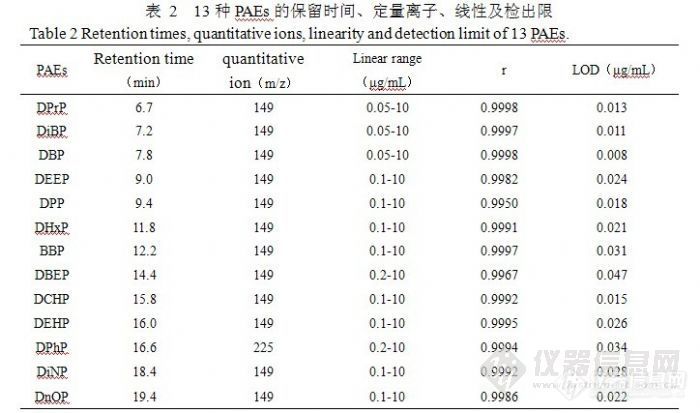
1.3.1 GC-MS分析 色谱柱:DB-5 MS毛细管柱(30 m×0.25 mm i.d.×0.25 μm);载气:He(>99.999%),柱流量为1.0 mL/min;进样口温度:260 ℃;不分流进样1 μL;柱升温程序:初始温度为80 ℃,保持1 min,以30 ℃/min升至235 ℃,保持11 min,再40 ℃/min升至300 ℃,保持5 min。溶剂延迟时间:5 min。离子源(EI源):70 eV,250 ℃;接口温度:280 ℃;检测器电压:0.89 kV。为了提高仪器分析的灵敏度,采用选择离子监测(SIM)模式。各目标分析物的保留时间和定量离子见表1。
1.3.2 磁性MWCNTs的合成 按照参考文献[20]方法合成磁性MWCNTs。具体过程如下:称取1.4 g FeCl3·6H2O和0.4 g MWCNTs于一100 mL洁净烧杯中,加入75 mL 乙二醇,用玻璃棒搅拌混匀,再加入3.6 g醋酸钠,搅拌溶解,在室温下放置30 min。将上述混合物转移到洁净聚四氟乙烯反应釜,置于密闭钢罐中,200 ℃油浴16 h。冷却后,将合成产品(磁性MWCNTs)转移到洁净烧杯中,依次用无水乙醇和超纯水清洗几次,再在烘箱中烘干(80 ℃),于真空干燥器内保存,备用。
1.3.3 分析水样中的PAEs 自来水样品取自作者所在的实验室,瓶装饮用水样品购自当地超市,湖水样品取自平湖(湖南汉寿县境内)小龙虾捕捞水域。自来水样品和瓶装饮用水样品直接取样分析,湖水样品过0.45 μm滤膜,去掉不溶物固体杂质后分析。分析过程如下:量取200 mL样品于250 mL容量瓶中,加入40 mg磁性MWCNTs,轻轻摇动,使磁性MWCNTs在水中分散。盖上塞子,放入摇床振摇(500 rpm)10 min后取出。将一块磁铁置于容量瓶底部,使磁性MWCNTs吸附到容量瓶底部,弃去水液。加入约10 mL超纯水,并将加入的超纯水和磁性MWCNTs全部转移到一20 mL具塞玻璃试管中。弃去超纯水,准确加入2 mL丙酮,盖上塞子,摇匀,静置5 min。用磁铁把磁性MWCNTs吸引到试管内壁,取出丙酮解吸液,用无水硫酸钠干燥,装入自动进样小瓶中,供GC/MS进样分析。
2.结果与讨论
2.1 磁性MWCNTs性质表征
合成的磁性MWCNTs为黑色粉末状固体,具有良好的磁性,能全部被磁铁吸引,并且在轻微的振摇时能均匀地分散在水中。这些特点与文献[26] 的描述相似。从透射电镜图(见图1)可以看到,Fe3O4磁性纳米粒子吸附在细长的MWCNTs的外表面上,结合成一种新的纳米材料。尽管超声处理会使Fe3O4纳米粒子从MWCNTs脱落(这一点与文献[26] 的描述不同),但剧烈的机械振摇不会破坏这两种纳米粒子的结合。通过操纵磁铁,很容易将合成的磁性MWCNTs聚集到容器内壁,以及将其从一个容器转移到另一个容器。因此,磁性MWCNTs能加快样品萃取和相分离速度,节省样品处理时间,简化实验操作。

图1 磁性碳纳米管的透射电镜图
Figure 1. TEM image of the magnetic MWCNTs
2.2 萃取条件的优化
将13种PAEs混合标样添加于空白超纯水样中(每种添加浓度为5 μg/L),用于实验条件的优化。本研究考察了萃取时间、水样pH值、解吸溶剂种类和用量及解吸时间等参数对萃取效果的影响。结果取3次重复实验的平均值。
2.2.1 萃取时间的优化 萃取时间对萃取效果的影响很大,图2显示了不同萃取时间各组分的回收率。从图2可知,各组分在萃取10 min时均达到满意回收率,继续延长萃取时间对提高回收率的贡献不大,因此,将萃取时间定为10 min。
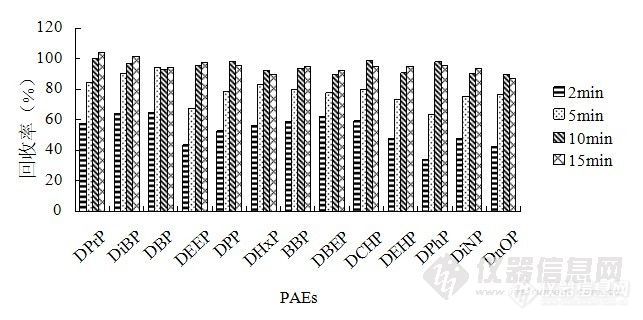
图2 萃取时间对回收率的影响。实验条件:解吸溶剂,2 mL丙酮;解吸时间,5 min;水样pH,7。
Figure 2 Effect of adsorption time on the extraction efficiency of PAEs. Experimental conditions: elute solvent,2 mL acetone; desorption time,5 min; pH of water sample, 7.
2.2.2 水样pH值的优化 水样pH值不仅能改变目标分析物的存在状态,而且能改变MWCNTs表面功能团的类型和密度,因而影响其对目标分析物的吸附量[27]。由于PAEs在pH5-7范围内稳定存在,本文仅考察了此pH范围(用盐酸调节)内的萃取效果。从图3可以看出,pH值为5-7时,磁性MWCNTs对PAEs的萃取效果没有明显差别。为简便起见,将pH=7用于其它条件的优化。
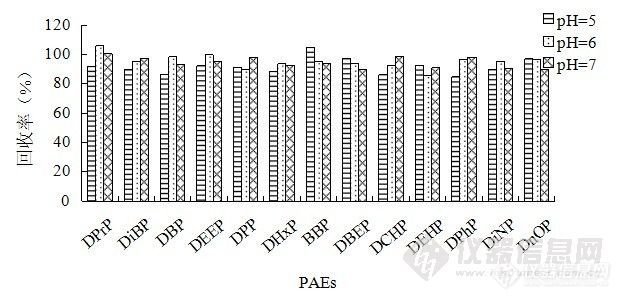
图3 水样pH值对回收率的影响。实验条件:萃取时间,10 min,解吸溶剂,2 mL丙酮,解吸时间,5 min。
Figure 3 Effect of pH of water sample on the extraction efficiency of PAEs. Experimental conditions: extraction time, 10 min; elute solvent, 2 mL acetone; desorption time, 5 min.
2.2.3 解吸溶剂的种类和用量及解吸时间的优化 解吸溶剂的种类及其用量也是影响萃取效果的关键因素。图4显示了丙酮、甲醇和乙腈3种不同溶剂的解吸效果。从图4可见,丙酮的解吸效果最好。因此,我们进一步优化了丙酮的用量(见图5)和解吸时间(见图6),最终选择2 mL丙酮作为解吸溶剂,解吸时间为5 min。
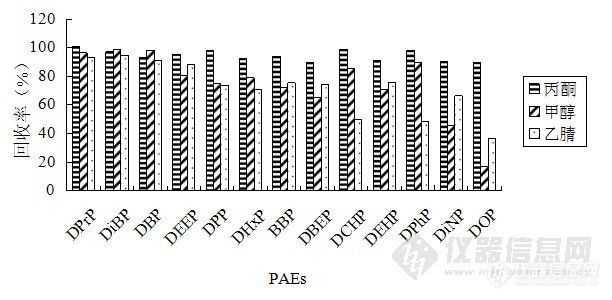
图4 不同解吸溶剂对回收率的影响。实验条件:萃取时间,10 min;水样pH,7;解吸溶剂用量,2 mL;解吸时间,5 min。
Figure 4 Effect of kind of elute solvent on the extraction efficiency of PAEs. Experimental conditions: extraction time, 10 min; pH of water sample, 7; volume of elute solvent, 2 mL ; desorption time,5 min.
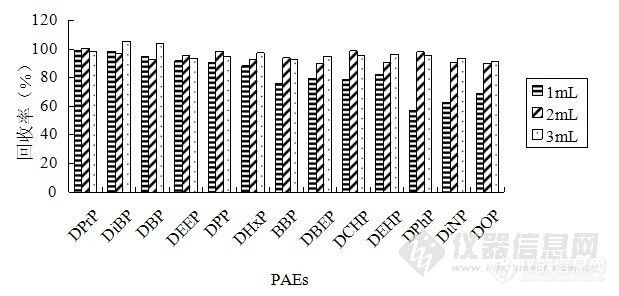
图5 解吸溶剂(丙酮)用量对回收率的影响。实验条件:萃取时间,10 min;水样pH,7;解吸时间,5 min。
Figure 5 Effect of volume of elute solvent(acetone)on the extraction efficiency of PAEs. Experimental conditions: extraction time, 10 min; pH of water sample, 7; desorption time,5 min.
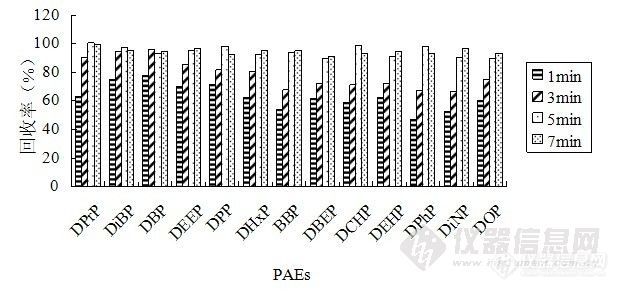
图6 解吸时间对回收率的影响。实验条件:萃取时间,10 min;水样pH,7;解吸溶剂,2 mL丙酮。
Figure 6 Effect of desorption time on the extraction efficiency of PAEs. Experimental conditions: extraction time, 10 min; pH of water sample, 7; elute solvent,2 mL acetone.
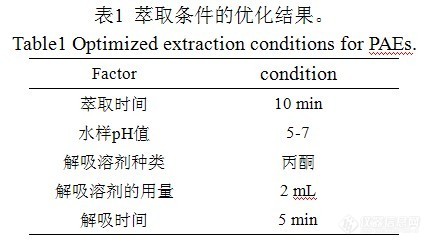
优化后的萃取条件见表1。在优化的条件下,PAEs各组分均达到满意的回收率(89.7%-100.5%)。
2.3 吸附容量
选择萃取效果最好的DBP来研究磁性MWCNTs的吸附容量。在空白超纯水中添加不同浓度的DBP,用上述优化的条件进行分析。结果发现,当添加水样中DBP的浓度达到0.8 μg/mL时,吸附量达到最大值,进一步增大DBP的浓度时,吸附量几乎保持恒定,因此,制备的磁性MWCNTs的吸附容量为4.0 mg/g(0.8 μg/mL×200 mL∕40 mg)。这表明磁性MWCNTs极易吸附PAEs,少量的磁性MWCNTs就能满足分析的需要。但磁性MWCNTs的用量越少,达到萃取平衡的时间越长。本文仅使用40 mg的磁性MWCNTs,在较短的时间(10 min)内就能完成萃取,达到较高的富集倍数(100倍)。
2.4 线性范围和方法的检测限
标准储备液用丙酮稀释成0.02-10 μg/mL范围的不同浓度,在1.3.1所述的条件下进样分析(标样色谱图见图7),根据标样浓度和色谱峰面积建立校准曲线,计算线性相关系数,结果见表2。从表2可见,所有组分的线性相关系数均大于等于0.9950,说明线性关系良好。以信噪比(S/N)为3确定各组分的仪器检测限(见表2)。方法的检测限结合样品处理的富集倍数(100倍)计算,结果为0.08-0.47 μg/L,表明本方法具有很高的灵敏度,可以满足实际检测的需要。
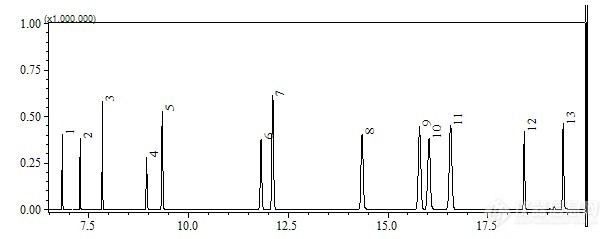
图7 PAEs标样的GC-MS色谱图
Figure 7 GC-MS chromatogram of 13 PAEs. (1-DPrP,2-DiBP,3-DBP,4-DEEP,5-DPP,6-DHxP,7-BBP,8-DBEP,9-DCHP,10-DEHP,111-DPhP,12-DiNP,13-DOP)
2.5 样品测定及方法的准确度和精密度
将优化后的方法应用于自来水、瓶装饮用水和湖水的分析,检测结果见表3。所有样品中均未检出13种PAEs。通过分析加标样品计算回收率和相对标准偏差(结果见表3),回收率范围为84.5%-107.5%,标准偏差范围为1.9%-12.8%,说明方法具有较高的准确度和精密度。
表3 实际样品的检测结果及添加回收率与精密度。
Table 3 Analysis results of real samples, recovery and precision of method.
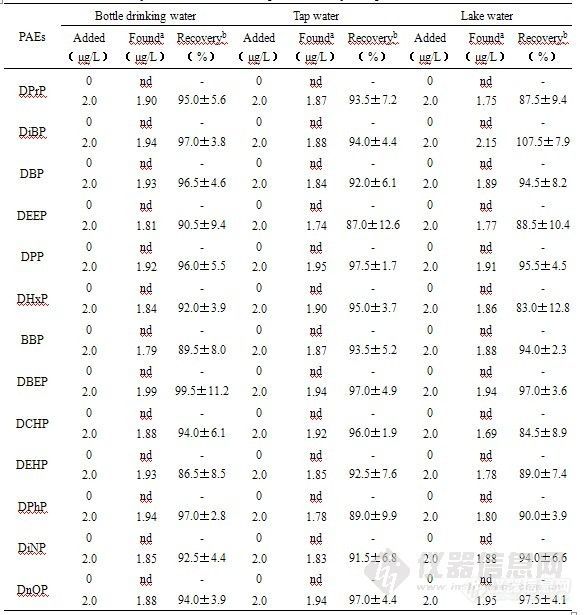
a Mean for three detections.
b Mean and standard deviation for three detections; nd: not detected.
3. 结论
本文成功地将磁性MWCNTs应用于水样中PAEs的萃取,并结合GC-MS进行分析。本方法操作简单、快速、省溶剂、污染小,结果准确可靠,可用于实际样品中PAEs的检测。
参考文献
[1] Hu X Z, Zhang K R, Sun J H, et al. Chinese Journal of Health Laboratory Technology(胡晓字,张克荣,孙俊红,等. 中国卫生检验杂志), 2003, 13(1): 9
[2] Fang L P, Niu Z Y, Cai F, et al. Journal of Analytical Science(房丽萍,牛增元,蔡发,等. 分析科学学报), 2005, 21(6): 687
[3] Li X, Zhong M, Xu S F, et al. J Chromatogr A, 2006, 1135(1): 101
[4] Lin X T, Wang X Y, Ren R. Environmental Pollution & Control(林兴桃,王晓逸,任仁. 环境污染与防治), 2003, 25(1): 268
[5] Amir S, Hafidi M, Merlina G, et al. Porc Bio, 2005, 40: 2183
[6] Qi W Q, Sun Z G. Determination of trace organic pollutants. Beijing: Chemical Industry Press (齐文启,孙宗光.痕量有机污染物的检测. 北京: 化学工业出版社), 2001
[7] Mo C H, Cai Q Y, Wu Q T, et al. China Environmental Science(莫测辉,蔡全英,吴启堂,等. 中国环境科学), 2001, 21(4): 362
[8] Chen R Y, Wang J P. Eco-textiles and green dye. Beijing: China Textile & Apparel Press(陈荣沂,王建平.生态纺织品与环保染料. 北京: 中国纺织出版社), 2002
[9] Chinese Research Academy of Environmental Science. Environmental quality standards for surface water. Beijing: China Environmental Science Press(中国环境科学研究院.地表水环境质量标准.北京: 中国环境科学出版社), 2002
[10] C astillo M, Barcelo D, Pereira A S, et al. Trends Anal. Chem., 1999, 18 (1): 26
[11] Michele D C, Alessia P, Giampiero S,et al. Food Chem. 2008, 111(3): 771
[12] Nour Kayali, Fernando G, Tamayoa, et al. Talanta. 2006, 69: 1095
[13] Lin Z P, Michael G Ikonomou, Jing H W, et al. Environ. Sci. Technol., 2003, 37: 2100
[14] Zhang Y, Zhou M, Ma M G, et al. Environmental Protection of Chemical Industry(张媛,周敏,马明广,等. 化工环保), 2006, 26(6): 525
[15] Iijima S. Nature, 1991, 354: 56
[16] Ren X M, Chen C L, Masaaki Nagatsu, et al. Chem. Eng. J., 2010: 1
[17] Zhao H X, Wang L P, Qiu Y M, et al. Anal. Chim. Acta., 2007, 586: 399
[18] Cai Y Q, Jiang G B, Liu J F, et al. Anal. Chim. Acta..2003, 494: 149
[19] Deng Z F, Yenilmez E, Leu J, et al. Appl. Phys. Lett., 2004, 85(25): 6263
[20] Hu P, Huang C Z, Li Y F, et al. Anal.Chem., 2008, 80(5): 1819
[21] Qu S, Huang F, Chen G, et al. Electrochem. Commun., 2007, 9(12): 2812
[22] Gao C, Li W W, Morimoto H, et al. Phys. Chem. B, 2006, 110: 7213
[23] Tan F Y, Fan X B, Zhang G L, et al. Mater. Lett., 2007, 61(8-9): 1805
[24] Deng Y H, Deng C H, Yang D, et al. Chem. Commun., 2005: 5548
[25] Jin J, Li R, Wang H L, et al. Chem. Commun., 2007: 386
[26] Gabriel Morales Cid, Agnes Fekete, Bartolome M, et al. Anal. Chem., 2010, 82 (7): 2743
[27] Peng X J, Li Y H, Luan Z K, et al. Chem. Phys. Lett., 2003, 376(1-2): 154











