本篇内容与大家分享的是植物性食品中代森锰锌的实验,对实验中遇到的问题进行了分析,强化实验过程的细节,提高自身科研水平,共同改进实验过程。本文重点对此实验提PH值 ,PH不准确会导致整个实验没有效果。
,PH不准确会导致整个实验没有效果。
摘要:本方法研究了植物性食品中代森锰锌残留量的LC/MS/MS方法,利用碱性乙二胺四乙酸二钠提取,甲酯化反应后,经HLB固相萃取柱净化后上机检测。标准曲线线性良好,相关系数r2>0.999,样品回收率89.65%~93.46%,相对偏差RSD<6%。
1前言
代森锰锌是乙撑二硫代氨基甲酸酯类杀菌剂,主要应用于防治果树、蔬菜、花卉及其它经济作物中藻菌纲和半知菌类引起的霜霉病、斑病、赤霉病等。由于代森锰锌的应用十分广泛,并且主要杂质和分解产物乙撑硫脲(ETU)具有致癌、致畸、致突变作用,因此引起广泛关注。代森锰锌难溶于水且不溶于大多数有机溶剂,只能采用间接方法测定。近年来,对代森锰锌残留方法的研究集中在甲基化后检测其衍生物亚乙基-1,2-双二硫代氨基甲酸甲酯(EBDC-dimethyl)。
本研究采用碘甲烷为甲基化试剂,建立了代森锰锌在植物性食品中残留分析的检测方法,利用超高效液相色谱-串联质谱(UPLC-MS /MS) 在多反应离子监测模式下进行检测。本方法有效地去除了干扰,提高了灵敏度,定性与定量分析准确。本方法简便快捷,易操作,能够满足苹果中代森锰锌的残留量的快速检测和确证的要求。
2实验部分
2.1 仪器与试剂
1290 infinity II超高效液相色谱仪(美国Agilent公司);6460 Triple Quad LC/MS(美国Agilent公司);Visiprep 24 TM Dl固相萃取装置(美国Supelco visiprep公司); XW-80A漩涡混合器(中国上海沪西);L400离心机(中国湖南湘仪);HLB固相萃取柱3cc 60 mg(美国 Waters公司)。
甲醇和乙腈(HPLC级,德国Merck公司);甲酸(HPLC级,中国上海安普);滤膜(PTFE Hydrophilic 0.22μm,中国上海安普);一级水(蒸馏水)。氢氧化钠();L-半胱氨酸;四丁基硫酸氢铵;盐酸;碘甲烷。
2.2 实验方法
2.2.1 标准溶液的配制
称取50.0 g L-半胱胺酸盐,50.0 g乙二胺四乙酸二钠,用800 mL水溶解。用氢氧化钠溶液调节pH 10,用水定容至1000mL。称取10.00 mg代森锰锌标准品,用L-半胱氨酸和乙二胺四乙酸二钠溶液溶解,定容至10mL,作为储备液置于4℃冷藏保存。用L-半胱氨酸和乙二胺四乙酸二钠溶稀释成10 mg/L的工作液置于4℃冷藏保存。
2.2.3 样品处理
精确称量5.00g样品于50mL离心管,加入20mL L-半胱氨酸及乙二胺四乙酸二钠溶液,超声振荡15min,加入10mL二氯甲烷,混匀,离心3min。取上清液于50mL离心管中,加入2mL 0.4moL四丁基硫酸氢铵溶液,用pH计调节pH 7.5-7.7,加入100μL碘甲烷,放置20 min后,离心5min,备用。
用5mL甲醇和5mL水平衡活化HLB净化柱后,取1/2提取液上样,用5mL水淋洗,抽干。然后用10 mL甲醇溶液洗脱,接收洗脱液,旋蒸至近干。加入2mL乙腈+0.1%甲酸水(1+1)涡旋定容。过0.22μm滤膜,待测。
2.3液相色谱-串联质谱条件
2.3.1 液相条件
色谱柱: Agilent Eclipse Plus C18 RRHD (2.1 mm×100 mm, 1.8 μm);流动相:0.1%甲酸水溶液(A),乙腈(B)。流速: 0.30 mL/min;柱温:40 ℃;进样量:2 μL。
2.3.2 质谱条件
ESI 正模式;Gas Temp: 325℃;Gas Flow: 10 L/min;Nebulizer : 45psi;Sheath Gas Tem: 350 ℃;Sheath Gas flow: 11 L/min。
3.结果与分析
3.1 质谱条件的优化
将代森锰锌配制成浓度为1mg/L的标准品,使用两通连接液相色谱与质谱,连续进样几次后,确定其母离子、子离子。MRM方式下所选择的目标分析物特征离子见表1。
| Compound | Precursor Ion(m/z) | Product Ion
(m/z) | Dwell
times/ms | Fragmentor
voltage/V | Collision energy/eV | Cell Accelerator Voltage/V |
| Mancozeb | 241 | 193 | 20 | 81 | 1 | 3 |
| | 241 | 134 | 20 | 81 | 21 | 3 |
| | 241 | 117 | 20 | 81 | 8 | 3 |
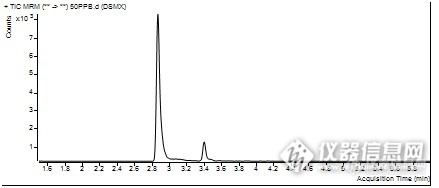
有机相的浓度对于待测物的影响较大,用乙腈和甲酸水作为流动相。随着乙腈浓度的增大,分离时间变短,分离效果较好。通过优化,确定以表2的方式作为梯度洗脱条件,流动相A为0.1%甲酸水,流动相B为乙腈。目标物标准溶液(50 ug/L)的总离子流图和提取离子色谱图见图1。
表2梯度洗脱条件
Table 2Conditions of gradient elution
| 时间/min | 流动相A/% | 流动相B/% |
| 0.00 | 60 | 40 |
| 1.00 | 60 | 40 |
| 3.00 | 10 | 90 |
| 4.00 | 10 | 90 |
| 4.01 | 60 | 40 |
| 5.00 | 60 | 40 |
3.3 线性回归方程
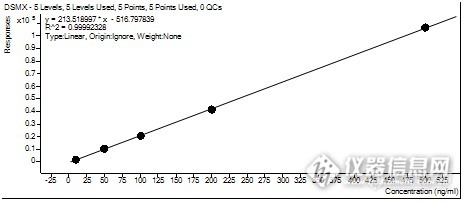
将标准溶液稀释成浓度为10、50、100、200、500 μg/L溶液,按以上条件进行分析,记录色谱图。以标准溶液浓度为横坐标,峰面积为纵坐标进行线性分析,得到代森锰锌的标准曲线方程Y=213.518997*x-516.797839,r2>0.999(如图2)。由样品前处理回收率和稀释倍数关系,定量限(LOD,S/N=10)100 ug/kg,检出限(LOD,S/N=3)为10ug/kg。 呈线性了
呈线性了
实验过程中出现过许多问题,提取液的配制不准确(PH值一定要准确)、pH调节范围不合适造成衍生不完全,这些问题的出现造成许多不必要实验,在以后对待类似实验时提供了借鉴的意义,同时也完善方法开发思路,与大家共勉。


 ,PH不准确会导致整个实验没有效果。
,PH不准确会导致整个实验没有效果。
 呈线性了
呈线性了