

氯化镁是一种无机物,化学式MgCl2,分子量为95.211,沸点1412 ℃,呈无色片状晶体,微溶于丙酮,溶于水、乙醇、甲醇、吡啶。
1、固化剂;营养强化剂;呈味剂(与硫酸镁、食盐、磷酸氢钙、硫酸钙等合用);日本清酒等的助酵剂;除水剂(用于鱼糕,用量0.05%~0.1%);组织改进剂(与聚磷酸盐类合用,作为鱼糜制品的弹性增强剂)。因苦味较强,常用量小于0.1%;
2、小麦粉处理剂;面团质量改进剂;氧化剂;鱼肉罐头改质剂;麦芽糖化处理剂。
3、以超微粉碎技术处理的大豆全粉为原料,利用氯化镁和谷氨酰胺转氨酶(glutamine transaminase,TG)制备大豆全粉凝胶。全豆豆乳分别冷却至25、15、5 ℃添加氯化镁和TG时,随着冷却温度的降低凝胶强度逐渐变大、 凝胶破裂距离变大,不同冷却温度对凝胶强度和破裂距离影响差异显著。[1]
4、经含氯化镁的漂洗液漂洗鱼糜后,硬度和白度随氯化镁浓度的增加逐渐增大,其凝胶特性较用清水和 0.15% NaCl 漂洗的鱼糜凝胶得到不同程度的提高。综合各项指标,浓度为 2.5 mmol / L 氯化镁漂洗液对鲢鱼鱼糜凝胶性能提升最大。[2]
5、KCl、CaCl2 和 MgCl2 部分替代 NaCl 腌制对风鸡样品中理化指标( pH、质构、TVBN 值、水分含量以及感官特性) 具有一定的影响。从感官评定的结果可以看出,当 45% 的 NaCl 被替代时,样品的色泽、香气、质地和咸味等感官特性与对照组无显著差异。所以,合理选择 KCl、CaCl2 和 MgCl2 的替代比,将有利于降低传统钠盐的使用量。[3]
6、在氯化镁浓度为0.4%(w/w)、谷氨酰胺转氨酶浓度为7U/g(蛋白质)时,全豆盐卤充填豆腐成型完好,凝胶强度最大达到221g,是传统内酯充填豆腐的2.2倍;持水率比传统内酯充填豆腐略小,为70%。在低剪切力阶段,全豆豆浆的粘度远大于传统豆浆,在全豆盐卤充填豆腐形成过程中,与传统内酯充填豆腐类似,储藏模量G′值迅速上升,但全豆盐卤充填豆腐G′值最终达到3020Pa,而传统内酯充填豆腐G′值最终仅为1300Pa。[4]
7、分别利用氯化镁、石膏和氯化镁、瓜尔胶复配凝固剂制作豆腐,瓜尔胶降低了氯化镁制作 豆腐的硬度,但复配凝固剂制作的豆腐和石膏豆腐有相似的质构特性,红外光谱对三种豆腐粉末 测定的结果表明:三种凝固剂对豆腐中蛋白的二级结构并没有影响;在 37 ℃下研究三种凝固剂 对豆浆黏度变化的影响,发现瓜尔胶提高了凝固过程第一阶段的速率,但降低了第二阶段凝固过 程的速率。瓜尔胶通过改变豆浆的凝固速率影响了豆腐的凝胶结构和质构特性[5]
项目 | 指标 | |
氯化镁,w/% | 以MgCl·6H2O计 | 99.0 |
以MgCl计 | 46.4 | |
钙(Ca),w/% | 0.10 | |
硫酸盐(以SO4 计),w/% | 0.40 | |
水不溶物,w/% | 0.10 | |
色度/黑曾 | 30 | |
铅(Pb)/(mg/kg) | 1 | |
砷(As)/(mg/kg) | 0.5 | |
铵(NH4)/(mg/kg) | 50 | |
1 方法提要
用三乙醇胺掩蔽少量三价铁、三价铝和二价锰等离子,在pH为10时,以铬黑T作指示剂,用乙二胺四乙酸二钠标准滴定溶液滴定钙镁含量,从中减去钙含量,计算出氯化镁含量。
2 试剂和材料
盐酸溶液:1+1、三乙醇胺溶液:1+3、氨-氯化铵缓冲溶液(甲)(pH≈10)、硝酸银溶液:10g/L、 乙二胺四乙酸二钠标准滴定溶液:c(EDTA)=0.02mol/L、 铬黑T指示剂。
称取约10g试样,精确至0.0002g,置于250mL烧杯中,用20mL水溶解。加1mL盐酸溶液,加热至沸,并微沸1min~2min,冷却后转移至250mL容量瓶中,用水稀释至刻度,摇匀,此溶液为试验溶液A。保留此溶液用于氯化镁含量、钙含量的测定。
移取25.00mL试验溶液A,置于250mL容量瓶中,用水稀释至刻度,摇匀。移取25.00mL上述溶液,置于250mL锥形瓶中,加入50mL水、5mL三乙醇胺溶液、10mL氨氯化铵缓冲溶液甲和0.1g铬黑T指示剂,用乙二胺四乙酸二钠标准滴定溶液滴定至溶液由紫红色变为纯蓝色。
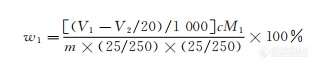
式中:
V1———滴定试验溶液所消耗的乙二胺四乙酸二钠标准滴定溶液体积的数值,单位为毫升(mL);
V1———滴定钙所消耗的乙二胺四乙酸二钠标准滴定溶液体积的数值,单位为毫升(mL);
c———乙二胺四乙酸二钠标准滴定溶液浓度的准确数值,单位为摩尔每升(mol/L);
m———试料的质量的数值,单位为克(g);
M1———六水氯化镁(MgCl·6H2O)的摩尔质量的数值,单位为克每摩尔(g/mol)(M1=203.3)。
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.2%。
1 试剂和材料
2 仪器和设备
3分析步骤
钙含量以钙(Ca)的质量分数w3计,数值以%表示,按公式(A.3)计算:

式中:
V2———滴定试验溶液所消耗的乙二胺四乙酸二钠标准滴定溶液体积的数值,单位为毫升(mL);
c ———乙二胺四乙酸二钠标准滴定溶液浓度的准确数值,单位为摩尔每升(mol/L);
m ———试料的质量的数值,单位为克(g);
M———钙(Ca)摩尔质量的数值,单位为克每摩尔(g/mol)(M=40.01)。
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.02%。
高温炉:能控制温度850℃±50℃。
称取约25g试样,精确至0.01g,加适量水溶解,加2mL盐酸溶液,置于电炉上加热至沸,并保持微沸1min~2min。冷却后转移至250mL容量瓶中,用水稀释至刻度,摇匀。用中速定性滤纸干过滤,弃去初滤液20mL。滤液作为试验溶液B。
移取25.00mL试验溶液B,置于250mL烧杯中,加水至50mL,加1mL盐酸溶液,在电炉上加热煮沸,在搅拌下滴加5mL氯化钡溶液,滴加时间约为1min。继续搅拌并微沸2min~3min,然后盖上表面皿,保持微沸5min。取下静置过夜。用慢速定量滤纸过滤,用淀帚擦拭烧杯壁,用温水洗净烧杯和沉淀,洗涤至无氯离子为止(取5mL洗涤液,加1mL硝酸溶液,用硝酸银溶液检验)。 将沉淀连同滤纸转移至已于800℃±50℃下灼烧至质量恒定的瓷坩埚中,在电炉上灰化后,置于高温炉中,于800℃±50℃灼烧至质量恒定。
硫酸盐含量以硫酸根(SO4)的质量分数w4计,数值以%表示,按公式计算:
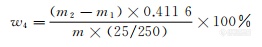
式中:
m2 ———坩埚和沉淀的质量的数值,单位为克(g);
m1 ———空坩埚的质量的数值,单位为克(g);
0.4116———硫酸钡换算成硫酸根的系数;
m ———试料的质量的数值,单位为克(g)。
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.05%。
硝酸溶液:1+4、硝酸银溶液:17g/L。
3分析步骤
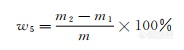
式中:
m1———玻璃砂坩埚质量的数值,单位为克(g);
m2———水不溶物和玻璃砂坩埚质量的数值,单位为克(g);
m ———试料的质量的数值,单位为克(g)。
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.02%。
比色管:容积50mL。
3 分析步骤
移取3.00mL500黑曾单位铂钴标准溶液,置于比色管中,用水稀释至刻度。
称取50.00g±0.01g试样,置于100mL烧杯中,加约40mL水溶解。转移至比色管中,用水稀释至刻度,摇匀,放置40min消除气泡。将试样溶液比色管与标准溶液比色管置于白色背景下,沿比色管轴线方向用目测比较,试样溶液所产生的色度不得大于标准溶液所产生的色度。
移取1.00mL铅标准溶液,置于150mL烧杯中,用盐酸溶液调节溶液的pH 为1.0~1.5(用精密pH 试纸检验)。将溶液移入分液漏斗中,用水稀释至约200mL。加入2mL吡咯烷二硫代氨基甲酸铵(APDC)溶液,摇匀。用三氯甲烷萃取两次,每次加入20mL,将萃取液(即有机相)收集于50mL烧杯中,在通风橱中用水浴加热蒸发至干。在残余物中加入3mL硝酸,加热近干。加入0.5mL硝酸和10mL水,加热至剩余液体体积为3mL~5mL,移入10mL容量瓶中,用水稀释至刻度。
称取10.00g±0.01g试样,置于150mL烧杯中,加入30mL水,加入10mL盐酸溶液,盖上表面皿并加热至沸,沸腾5min。冷却,用氢氧化钠溶液调节pH 值为1.0~1.5(用精密pH 试纸检验)。然后按上一步中从“将溶液移入分液漏斗中……”开始操作。
选用空气乙炔火焰,于283.3nm波长处,用水调零,使用原子吸收分光光度计测定铅标准测定溶 液和试验溶液的吸光度。
称取2.00g±0.01g试样,置于250mL烧杯中,加50mL水,加入10mL盐酸,作为试验溶液。
限量标准溶液的配制:移取 1.00 mL 砷标准溶液[1 mL 溶液含砷(As)0.001 mg],以下按 GB/T5009.76—2003中第11章进行测定。
纳氏试剂、氢氧化钠溶液:100g/L、酒石酸钾钠(KNaC4H4O6·4H2O)溶液:500g/L、铵标准溶液:1.00mL溶液含铵(NH4)0.02mg:用移液管移取2.00mL按 HG/T3696.2配制的铵标准溶液,用水稀释至100mL,摇匀。该溶液现用现配、无铵蒸馏水:按 HG/T3696.3进行制备,本试验所有试剂均用无铵蒸馏水配制。
移取0.00mL、0.50mL、1.00mL、1.50mL、2.
00mL铵标准溶液,分别置于50mL比色管中,加入1mL酒石酸钾钠溶液,摇匀。加2mL纳氏试剂,摇匀,用水稀释至刻度,摇匀。放置15min,于分光光度计上,在420nm处,使用1cm比色皿,以水调零测量其吸光度。
从每个标准溶液的吸光度中减去试剂空白溶液的吸光度,以铵的质量(mg)为横坐标,对应的吸光度为纵坐标,绘制工作曲线。
称取约5g试样,精确至0.01g,置于150mL 烧杯,加水溶解。转移至250mL 容量瓶中,加50mL氢氧化钠溶液,加水稀释至刻度,摇匀,静置2h。
移取20.00mL上层清液,置于50mL比色管中,加1mL酒石酸钾钠溶液,摇匀。加2mL纳氏试剂,摇匀,用水稀释至刻度,摇匀。放置15min,于分光光度计上,在420nm处,使用1cm比色皿,以水调零测量其吸光度。从工作曲线上查出试验溶液中铵的质量。
铵含量以铵(NH4)的质量分数w6 计,数值以 mg/kg表示,按公式计算:
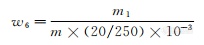
式中:
m1———从标准曲线上查得铵质量的数值,单位为毫克(mg);
m ———试料的质量的数值,单位为克(g)。
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于10mg/kg。
参考文献:
[1] 李君,康昕,蒲雪丽,崔怀田,王胜男,宋虹,朱丹实,刘贺.不同冷却温度添加氯化镁和谷氨酰胺转氨酶对大豆全粉凝胶流变性质的影响[J].食品科学,2021,42(08):17-21.
[2] 余永名,李晓丽,刘宇彤,仪淑敏,李钰金,李学鹏,徐永霞,励建荣.漂洗液中氯化镁浓度对鲢鱼鱼糜凝胶特性的影响[J].食品工业科技,2016,37(07):322-327+337.
[3] 林静,刘斌,李松林.氯化钾、氯化钙和氯化镁部分替代食盐腌制对风鸡品质影响的研究[J].食品工业科技,2016,37(03):105-109.
[4] 吴超义,夏晓凤,成玉梁,霍建冶,钱和.以氯化镁为凝固剂的全豆充填豆腐质构与流变特性研究[J].食品工业科技,2015,36(06):143-146+152.
[5] 李蒙,陈复生,杨宏顺,王萌蕾,赖少娟.氯化镁瓜尔胶复合凝固剂对豆腐凝固过程影响[J].粮食与油脂,2014,27(04):30-33.
[6] GB 25584-2010, 食品安全国家标准 食品添加剂 氯化镁.