-
+关注
私聊
-

yhl-87_
第11楼2009/11/09
气相色谱手性分离 (12)
二.对 Chirasil-Val 聚硅氧烷链的改性
早在 1966 年 Gil-Av 等就用涂在玻璃毛细管柱上的 N-三氟乙酰基-L-异赖氨酸戊酯作手性固定液分离消旋的N-三氟乙酰基氨基酸酯,1977 年Frank 制备出二甲基硅氧烷和(2-羰丙基)甲基硅氧烷的共聚物固定相 Chirasil-Val,这一固定相具有很好的分离氨基酸对映异构体的性能,并成为很有名的商品手性柱。
但是 Chirasil-Val 也有不尽如人意的地方,Koppenboefer 研究发现用Chirasil-Val 分离蛋白质水解得到关键的 20 个氨基酸对映体中,有 8 个对映体(Val,Gly,Thr,α-IIe, IIe,Ser,Pro,和Leo)分离不够好,改变柱温不能改善分离状况,必须调整固定相的极性。调整固定相的极性的办法是,1。合成具有固定结构的聚硅氧烷共聚物,即带不同烷基侧链的聚硅氧烷和带甲基(2-羧丙基)聚硅氧的共聚物。2。把L-缬氨酸叔丁基酰胺基团甲基(2-羧丙基)聚硅氧结合在一起,成为具有手性分离的固定相。1995年 Koppenboefer 发现在主链中二甲基硅氧烷链段和带有 L-缬氨酸叔丁基酰胺基团的硅氧烷链段比例进行了研究,此比例等于 7 的情况下分离效果最好。合成的路线如图 12-1所示:
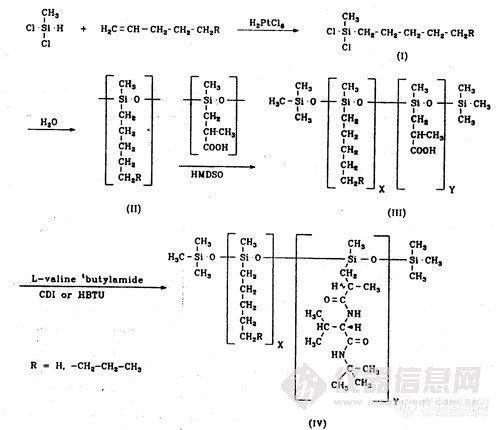
图 12-1 Koppenboefer 合成改性 Chirasil-Val 路线
这种固定相制备的色谱柱分离 20 种氨基酸对映体的色谱如图 12-2所示。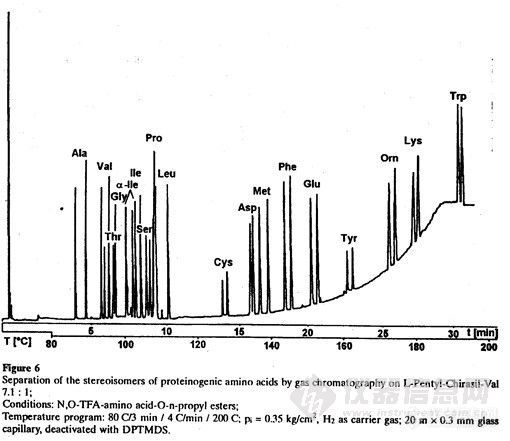
图 12-2 Koppenboefer的色谱柱分离 20 种氨基酸对映体的色谱如图
文献:
1.B. Koppenboefer,et ak.,Chromatographia,1995,40(11/12):718
2. B. Koppenboefer,et ak.,J.Chromatogr.A,1995,699:215
-
+关注
私聊
-

yhl-87_
第12楼2009/11/09
气相色谱手性分离 (13)
用“Chirasil-Val 商品柱做手性氨基酸的 ee-值
1978年合成了聚合物手性固定液,即把L-缬氨酸-特丁酰胺接枝到聚硅氧烷上,商品名“Chirasil-Val”(“Chirasil-Val” 4 )(见图 13-1) 是 80 年代使用很多的分离手性氨基酸的固定相,具有左旋或右旋Chirasil-Va(L- and D-ChirasilVal ),以适应用于不同对映体的过量测定,可以用于多肽水解后用结晶法制备左旋或右旋氨基酸纯品中杂质对映体的测定。例如在左旋亮氨酸中可以测定出低达 0.04% 含量的右旋亮氨酸(以三氟乙酰基亮氨酸-O-甲基酯),如图13-2 中所显示的情况。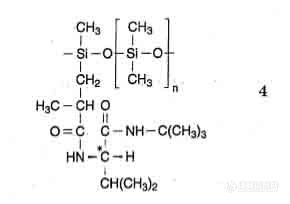
图 13-1 商品手性 gc 固定相“Chirasil-Val” 4 的结构
图 13-2 左旋三氟乙酰基亮氨酸-O-甲基酯杂质在左旋和右旋 Chirasil-Va 4 固定相上分析的色谱图。
左面的色谱是在 20m x 0.25 mm ID.弹性石英毛细管柱,柱温 95 ℃,氢载气(0.3 bar),分流比为100:1
左面的色谱是在 20m x 0.25 mm ID.弹性石英毛细管柱,柱温 110 ℃,氢载气(0.4 bar),分流比为100:1
-
+关注
私聊
-

yhl-87_
第13楼2009/11/09
气相色谱手性分离 (14)
氨基酸杯芳烃接枝聚硅氧烷手性固定相(1)
把手性 L-缬氨酸特-丁基酰胺键合到间苯二酚杯[4]芳烃环状结构的 8 个羟基上,形成一种高度定向排列的超分子结构。间苯二酚杯[4]芳烃是由间苯二酚和 1-十一烯醇得到,把这种杯芳烃通过四个间隔基单元键合到聚二甲基硅氧烷上,得到 Chirasil-Calix 7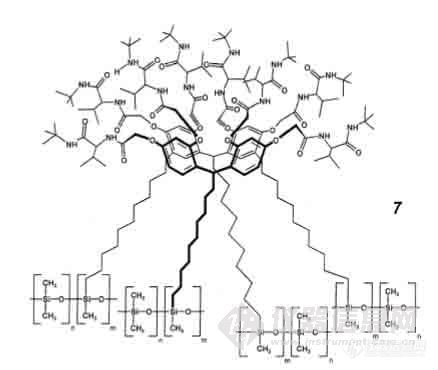
J. Pfeiffer, V. Schurig, J. Chromatogr. A ,1999,840:145.
令人惊奇的是手性选择剂几乎是环状结构定向彼此并列紧密地排列着,与并Chirasilof Val 4 不能够明显地提高其选择性,而芳香族氨基酸衍生物也没有表现出有利与形成包含型超分子化合物的倾向。合成的这种带有手性胺侧链的杯[4]芳烃用作手性固定相,用于分离手性氨基酸、醇和胺有专门的报道。(N. Iki, F. Narumi, T. Suzuki, A. Sugawara, S. Miyano, Chem. Lett. ,1998 :1065.;
F. Narumi, N. Iki, T. Suzuki, T. Onodera, S. Miyano, Enantiomer 2000,5: 83.)
(文献:Jens Pfeiffer, Volker Schurig,J. Chromatogr.A,1999,840:145)
-
+关注
私聊
-

yhl-87_
第14楼2009/11/09
气相色谱手性分离 (15)
氨基酸杯芳烃接枝聚硅氧烷手性固定相(2)——Chirasil-Calix 7 的合成
上一讲提到由间苯二酚和 1-十一醇得到的杯芳烃通过四个间隔基单元键合到聚二甲基硅氧烷上,形成手性固定相 Chirasil-Calix 7 ,这种固定相的合成路线如图 15-1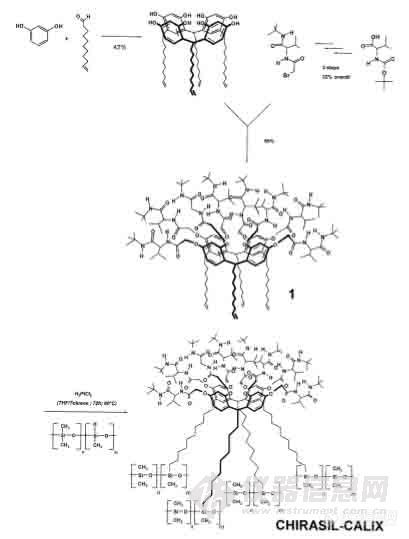
图 15-1 CHIRASIL-CALIX 手性固定相
合成这一固定相时,首先把间苯二酚和1-十一烯醇缩合制备成间苯二酚杯[4]芳烃,然后把手性L-缬氨酸特-丁基酰胺键合到间苯二酚杯[4]芳烃环状结构的 8 个羟基上,形成一个具有手性中心的环状排列结构1 (图 15-1)。把间苯二酚杯[4]芳烃(1)用聚硅氧烷稀释涂渍成色谱柱。或者把间苯二酚杯[4]芳烃(1)通过它的四个端烯基,用铂催化硅-氢加成到含氢硅氧烷的链上,形成键合的聚硅氧烷手性固定液Chirasil-Calix。
(文献:Jens Pfeiffer, Volker Schurig,J. Chromatogr.A,1999,840:145)
-
+关注
私聊
-

yhl-87_
第15楼2009/11/09
气相色谱手性分离 (16)
氨基酸杯芳烃接枝聚硅氧烷手性固定相(3)——Chirasil-Calix 7 的性能
使用Chirasil-Calix 7 (上两讲所阐述的键和到聚硅氧烷链上的GC手性固定液)和未键合只把手性L-缬氨酸特-丁基酰胺键合到间苯二酚杯[4]芳烃溶解到OV-1701中作毛细管色谱柱的固定相,比较它们的分离性能。
把上述两种固定液涂渍到20 m x 0.25 mm I.D 弹性石英毛细管柱上,在涂渍以前先把弹性石英毛细管柱在 260 ℃ 通小的氢气流下处理两天,把Chirasil-Calix 的 0.25% 乙醚溶液以静态法涂渍到处理过的弹性石英毛细管柱上,形成膜厚为0.25 µm 的毛细管柱,之后,在100 ℃,130 ℃,160℃下通气流老化各 4 小时,最后在160℃ 下再老化16 小时。
实验用样品的胺基和羧基按下述方法进行衍生化为N(O,S)-三氟乙酰基氨基酸甲酯:
: 把 10 mg 外消旋氨基酸在 1 ml 4 mol 盐酸加 2 ml 甲醇溶液中于 40 ℃ 下加热 1 小时,等溶液干涸后把残渣溶解在 1 ml 二氯甲烷中,加入三氟乙酸酐 0.25 ml 在室温下反应 1 小时,在反应溶液上面通入干燥的小氮气流。把多余的三氟乙酸酐吹走,把残留物溶解在 1 ml 二氯甲烷中。
使用手性 L-缬氨酸特-丁基酰胺键合间苯二酚杯[4]芳烃溶解到 OV-1701 中涂渍的毛细管柱,其柱效很差,对N(O,S)-三氟乙酰基氨基酸甲酯没有手性分离能力。而把 15% (w/w) 的L-缬氨酸特-丁基酰胺键合间苯二酚杯[4]芳烃接枝到含有 10% Si–H 基的二甲基硅氧烷上,制备出 Chirasil-Calix 型的色谱柱,分离17 个 D,L N(O ,S)-TFA 氨基酸甲酯的保留数据列于表 16-1中。
表 16-1 17 个 D,L N(O ,S)-TFA 氨基酸甲酯在Chirasil-Calix 7 上的保留数据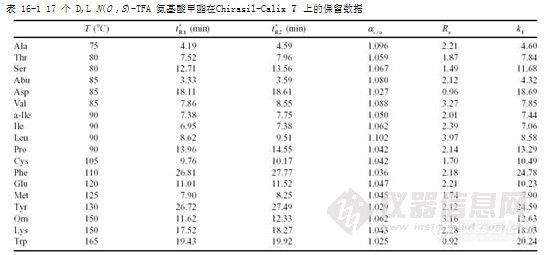
色谱柱:20 m x 0.25mm 弹性石英毛细管柱,涂渍 Chirasil-Calix 7 膜厚 0.25 µm,分流比1:100, 载气 0,45 bar,氢气。死时间 tM=1.01 min
(文献:Jens Pfeiffer, Volker Schurig,J. Chromatogr.A,1999,840:145)
-
+关注
私聊
-

yhl-87_
第16楼2009/11/09
气相色谱手性分离 (17)
氨基酸杯芳烃接枝聚硅氧烷手性固定相(4)——Chirasil-Calix 7 的应用
使用 20 m x 0.25mm 弹性石英毛细管柱,涂渍 Chirasil-Calix 7 固定相可以同时把蛋白质水解后的一些氨基酸对映提得到很好的分离,如图 17-1 就是分离蛋白质水解后的 D,L N(O,S)-TFA 氨基酸甲基酯的色谱。
图 17-1 Chirasil-Calix 7 色谱柱分离白蛋质水解后的 D,L N(O,S)-TFA 氨基酸甲基酯的色谱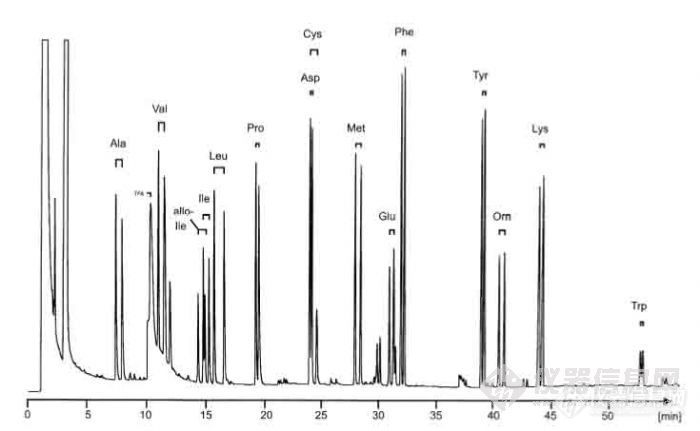
图 17-2 是分离挥发性氨基酸的 N-TFA-2-氨基丁酸甲酯的色谱。使用这一固定相不同于 Chirasil-Val (GC 手性分离讲座 6)的分离情况,对脯氨酸的分离很好,而对天冬氨酸和色氨酸的分离不够好。对酪氨酸鸟氨酸在Chirasil-Val 上具有近似的分离因子,而在 Chirasil-Calix 色谱柱上鸟氨酸比酪氨酸分离度好的多。一个令人意外的是含芳香基的氨基酸在Chirasil-Calix 色谱柱上分离情况没有改善,甚至有所下降。这一点从相近流出的 Glu/Phe (谷氨酸/苯丙氨酸)和Tyr/Orn(酪氨酸/鸟氨酸)可以明显地看出。因此没有出现预期的超分子作用发生。

图 17-2 Chirasil-Calix 7 色谱柱分挥发性的N-TFA-2-氨基丁酸甲酯的色谱
(文献:Jens Pfeiffer, Volker Schurig,J. Chromatogr.A,1999,840:145)
-
+关注
私聊
-

yhl-87_
第17楼2009/11/09
气相色谱手性分离 (18)
氨基酸杯芳烃接枝聚硅氧烷手性固定相和杯芳烃固定液的比较
前两讲的实验说明使用氨基酸杯芳烃接枝聚硅氧烷手性固定相可以很好地分离手性化合物,从第17讲的内容说明,尽管杯芳烃具有很好的可形成超分子的结构,但是对含芳香基的氨基酸对映提的分离并没有起作用,起手性分离作用的是杯芳烃上的氨基酸。下面试看一个只有杯芳烃的GC 固定液的分离能力,我们曾合成了下面结构的杯芳烃: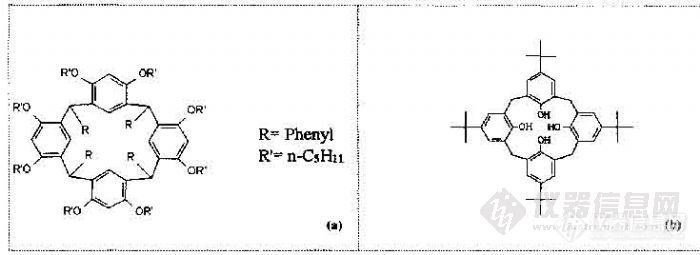
把这类固定也涂渍成弹性石英毛细管柱,可以很好地分离各种位置异构体,如甲酚、二甲酚、二甲萘的异构体,如图 18-1 和图 18-2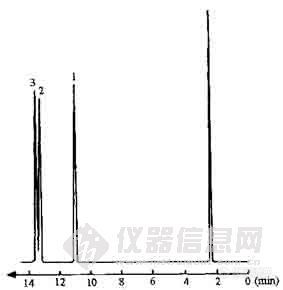
图 18-1 21.5 m x 0.25mm 涂渍杯芳烃的色谱柱分离甲酚异构体
1——邻甲酚, 2——对甲酚 3——间甲酚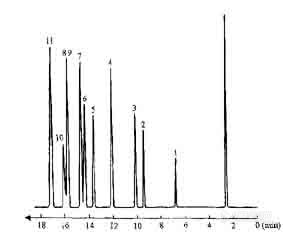
图 18-2 21.5 m x 0.25mm 涂渍杯芳烃的色谱柱分离二甲萘异构体
1——萘,2——2-甲萘,3——1-甲萘,4——联苯,5——2,6-二甲萘
6——1,7-二甲萘,7——1,6-二甲萘,8,9——1,4-和2,3-二甲萘,
10——1,5-二甲萘,11——1,2-二甲萘
但是这一固定液对各种手性莸构体却没有分离能力。
(文献:Hanbang Zhang,et al.,J. Chromatogr.A,1997,787: 161-169)
-
+关注
私聊
-

yhl-87_
第18楼2009/11/09
气相色谱手性分离 (19)
基于金属配合物的手性气相色谱固定液(1)
1977 年 Schurig 使用二羰基铑(I)-3-三氟碳乙酰-(1R)-樟脑酸盐配合物(dicar-
bonyl rhodium(I)-3-trifiuoroacetyl-(1R)-camphorate)(见图 19-1)溶于角鯊烷做手性固定液,用于分离 3-甲基环戊烷对映体,这种方法叫做配位作用气相色谱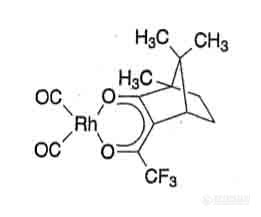
图 19-1 二羰基铑(I)-3-三氟碳乙酰-(1R)-樟脑酸盐配合物(1R)
(V. Schurig, Angew. Chem Int. Ed. Engl.,1977,16 :110.)。这一研究开始于1969年(V. Schurig, E. Gil-Av, J. Chem. Soc. D, Chem. Commun,1971:650.),但是没有获得满意的结果,这一次的研究获得了成功。3-甲基环戊烷对映体的对映体的结构如图 19-2 中左上方的图,下面的图是使用 200 m x 0.5mm 不锈钢毛细管柱涂渍混合固定液(在角鲨烷中溶解 0.04 mol 1R)分离3-甲基环戊烷对映体的色谱,柱温为 22 ℃,载气为氮气,对映体之间的分离因子为 1.025,箭头所指处是单独使用角鲨烷做固定液时3-甲基环戊烷的峰,分离所用的参比物(Ref)是甲基环己烷。(V.Schurig, J. Chromatogr. A, 2002,965:315)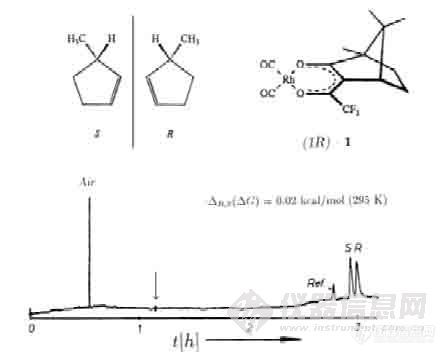
图 19-2 3-甲基环戊烷对映体的分离图
-
+关注
私聊
-

yhl-87_
第19楼2009/11/09
气相色谱手性分离 (20)
基于金属配合物的手性气相色谱固定液(2)
上一讲讲到本 1977 年 Schurig 使用二羰基铑(I)-3-三氟碳乙酰-(1R)-樟脑酸盐配合物做手性气相色谱固定相,开辟了配合作用气相色谱。过渡金属所形成的二羰基配合物从二羰基铑扩展到全氟酰化萜烯二酮的锰(II)、钴(II)和镍(II)的化合物,如图 20-1的结构式。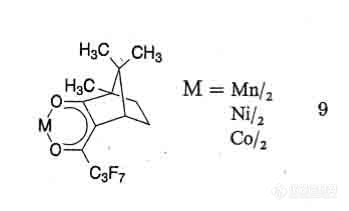
图 20-1 全氟酰化萜烯二酮的锰(II)、钴(II)和镍(II)化合物
下面图 20-2 是使用结构式中金属原子为镍的化合物(镍(II)二[3-(七氟丁酰基)-10-亚乙基)(1S)-樟脑化合物)做固定液,制成玻璃毛细管柱,分离三个手性中心顺反异构体(第二丁基过氧化丁二烯(sec-butyloxirane)得到的色谱,固定液0.125 mol 溶于OC-101中,涂渍成 25 m x 0.25mm ID 的色谱柱,柱温为 90 ℃。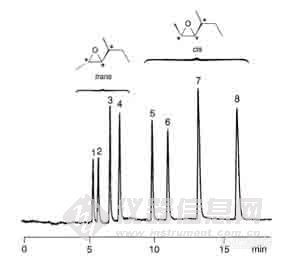
图 20-2 配合作用色谱分离顺反异构体的色谱
-
+关注
私聊
-

yhl-87_
第20楼2009/11/09
气相色谱手性分离 (21)
金属配合作用气相色谱的原理概述
在气相色谱中使用金属络合物作固定相是 1955年 Bradford等在聚乙二醇中加如硝酸银分离链烯首次报道的。上世纪 70 年代 Schurig 开创的配合作用气相色谱,是用金属配合物作气相色谱固定液,它的原理是基于溶质的孤对电子与金属配合物固定液的电子空轨道之间的配位作用而进行分离的。就像烯烃 π 键上的电子进入银离子上的电子空轨道那样。在溶质与金属络合物形成三元配合物时,由于配位键对空间、张力及电子效应的显著灵敏性,以及溶质与金属配位作用的多样性,使其对一定空间结构的位置异构体具有选择性,并且由于手性金属络合物与具有电子给体性质的溶质间可形成 1:1的非对映体配合物,使其对光学异构体也具有手性识别作用,因而配合作用气相色谱是一种分离选择性很有特色的色谱分离方法,并且溶质与金属离子配位通常不需要衍生化,这使得配合作用气相色谱的使用极为方便。
此外,溶质分子与金属配合物形成三元配合物的稳定性不仅依赖中心离子的价态、电子结构、离子半径以及中心离子和配体重叠轨道的空间安排;而且也受配体的碱性以及配体通过中心离子的电子转移效应等诸多因素影响,这使得配合作用气相色谱分离过程的可控制性颇为灵活。
在配合作用气相色谱中使用何种类型的金属配合物作固定液分离效果最好,还没有一定的规律,但除了气相色谱固定液要求的热稳定性和低熔点外,还要保证配合物中金属阳离子至少有一个空的成键轨道可用于额外的配位,以及要保证溶质分子与金属配合物的配位作用快速而且可逆。目前已研究过的金属络合物固定液主要有普通金属配合物、光活性的手性金属配合物以及金属液晶类配合物等三类。
(史雪岩等,分析化学,2000,28(1):118)