-
+关注
私聊
-

yhl-87_
第31楼2009/11/09
电化学分析法(32)—恒电流库仑滴定法
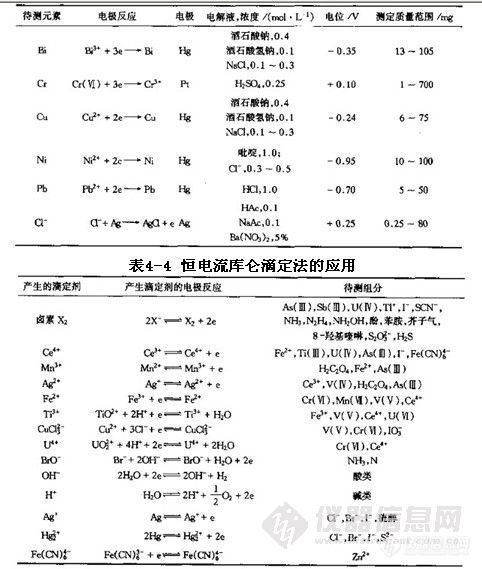
4.5 恒电流库仑滴定法
恒电流库仑滴定法与滴定分析基本相同,其不同在于滴定剂不是由滴定管加入,而是在恒电流下对一种辅助剂进行电解,在电解池内部的工作电极上产生一种能与待测组分迅速定量反应的物质(滴定剂),反应完全时,用指示剂或其他方法指示终点。根据消耗的总电量(电流乘以电解时间),用法拉第电解定律计算被测组分的量。维持100%的电解电流效率以及有准确指示终点的方法是保证测定准确度的关键。
例如,电解 Fe2+溶液,Fe2+在阳极上氧化成Fe3+,开始电解时的电流效率可达100%,随着电解的进行,阳极表面附近Fe3+浓度不断增加,Fe2+浓度不断降低,阳极电位逐渐向正方向移动,最后可能Fe2+还未全部氧化,阳极电位已达到了其他物质的分解电位,则阳极上即有其他物质发生氧化,使电解Fe2+的电流效率低于100%,产生测量误差。
若加入过量的 Ce3+作为辅助剂,Fe2+就能以恒定电流进行电解。电解开始时,Fe2+在阳极上氧化,阳极电位越来越正,当到达Ce3+的分解电位时,Ce3+开始氧化析出Ce4+,与溶液中未反应的Fe2+ 发生的反应如下
Ce4+ + Fe2+ = Ce3+ + Fe3+
从此反应可知,电解Ce3+所消耗的电量与单纯电解 Fe2+时所消耗的电量完全相等。由于溶液中Ce3+始终是过量的,相对稳定了阳极电位,避免了其他副反应的发生,保证了电解的电流效率为100%。
库仑滴定的装置如图4-3a所示。电解时,恒电流数值可由恒电流器读出。电停表作为计时器。如图4-3b所示,库仑池的工作电极是电解产生滴定剂的电极;辅助电极浸在另一种电解质中,下段用多孔陶瓷管与试液隔开,防止电极产物对工作电极反应或对滴定产生干扰。工作电极和辅助电极分别作为电解池的阳极或阴极;参比电极和指示电极与终点指示器相连,用以指示滴定终点。用指示剂指示终点时不需要参比电极和指示电极。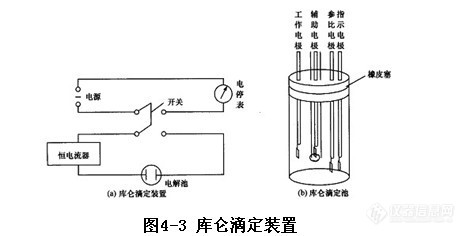
库仑滴定法由于不需要配制标准溶液或使用基准物质,可以避免由于标准溶液的不准确引进的测定误差。因所用滴定剂由电解产生,边产生边滴定,一些不稳定的物质如Cl2、Br2、Cu+、Mn(Ⅲ)、Ag(Ⅱ)等都可作为库仑滴定剂,大大扩大了分析范围,广泛用于酸碱、沉淀、配位及氧化还原滴定中,还可以测定微量或痕量组分,并可实现自动化分析。库仑滴定法由于测定的物理量是电流及时间,均易测准,是一种准确而灵敏的分析方法,RSD约为0.5%,若用计算机控制,灵敏度、准确度会更高。
-
+关注
私聊
-

yhl-87_
第33楼2009/11/09
电化学分析法(34)—经典(直流)极谱法
5 极谱分析法 (Polarography)
自从1922年捷克和斯洛伐克的海洛夫斯基(J.Heyrovsky)首创极谱学以来,极谱分析已由经典极谱、导数极谱发展到单扫描极谱、交流极谱、方波极谱、脉冲极谱、半积分和半微分极谱法等,使极谱分析的灵敏度和分辨率有了很大的提高。这些方法在矿石及有色金属分析中已得到了普遍的应用。
5.1 经典(直流)极谱法
经典极谱法又称直流极谱法或恒电位极谱法,是由一个滴汞电极和一个参比电极插入待测试液中组成电解池,以直流电压(0.1~0.2V/min)施加于电解池上进行电解,再根据电解过程中所得到的电流(i)~电位(E)曲线进行分析。其基本装置如图5-1所示。采用的指示电极—滴汞电极是一个面积很小的极化电极,汞是通过内径约为0.5~0.08mm的厚壁毛细管均匀下滴,在蒸馏水中滴落时间约3~5s。参比电极用一个相对来说面积比较大,电位稳定的非极化电极,常用的有饱和甘汞电极、银-氯化银(Ag-AgCl)电极、银汞电极、石墨电极和汞层电极等。电流是用检流计、记录仪、示波器等记录。在电解池上加上一定的直流电压并逐渐增加,当它达到溶液中待测离子的分解电压后,待测离子在滴汞电极上迅速地还原且产生相应的电流,随着外加电压的继续增加,电解加速,电流增加(此时滴汞电极称为去极化,在滴汞电极上起反应的物质称为去极剂),直至受扩散控制的离子到达电极表面时立即被还原而处于扩散平衡状态为止,此时电流不再增加,而形成极限扩散电流,从而得到典型的极谱电流(i)~电位(E)曲线,即极化曲线称为极谱波,如图5-2所示,该图为镉离子极谱图。极谱波的波高即极限扩散电流,它与待测离子的浓度成正比,这是极谱定量分析的基础。利用各种离子的氧化还原电位不同,即i~E曲线中点所对应的电位(半波电位E1/2)的不同可作定性的依据。
扩散电流可用依尔科维奇(Ilkovic)方程式表示: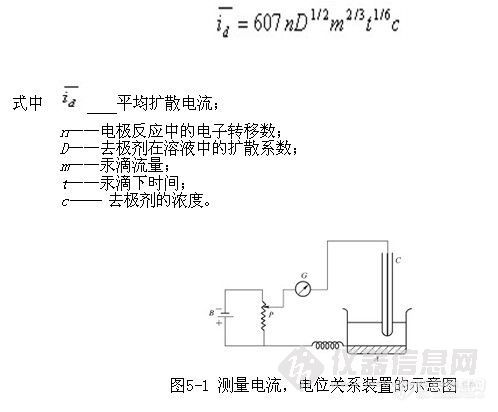
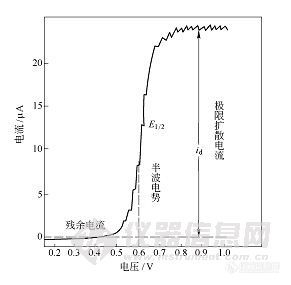
图5-2 镉离子极谱图
待测物质(去极剂)的浓度是影响扩散电流的主要因素,其他如汞柱高度、毛细管的大小、溶液组分及温度等也都是影响扩散电流的因素。在极谱测定过程中,应该保持汞柱高度不变,温度变化控制在士0.5℃。
经典极谱法适合于浓度为10-5~10-2mol/L物质的测定,相对误差约为2%~5%。其分辨率为100mV,当准确测量后波的波高时,前波元素与后波元素的最大浓度比不得超过10:1。
-
+关注
私聊
-

yhl-87_
第34楼2009/11/09
电化学分析法(35)—单扫描极谱法
5.2 单扫描极谱法
单扫描极谱法又称线性变电位极谱法(简称示波极谱法),是指在滴汞电极的一滴汞的生长末期增加一次电压扫描,用阴极射线示波器来显示其所得的电流(i)~电位(E)曲线的极谱法。它与经典极谱相似,是根据电压线性扫描的伏安曲线来进行分析的。所不同的是,经典极谱在获得i~E曲线的过程中,电压扫描速度慢(一般是0.2V/min),以至在一滴汞的生命期间,滴汞电极的电位保持恒定,电流只随电极的面积变化,极化曲线是在许多滴汞的周期内获得的,属于恒电位极谱法;而单扫描极谱是以线性脉冲(通常为锯齿波)加在一滴汞的生长后期,扫描速度很快(一般是0.25V/s),在测量电流时,电极的面积几乎不变,电流随电位的改变而变化。因此,整个极化曲线在一个汞滴上可以全部得到。i~E曲线记录的时间少至2s,一般用示波器观察极谱图。其特点是在一滴汞的生命期间,滴汞电极的电位不是恒定的,而是随着时间变化的,电极电位是时间的线性函数,属于变电位极谱法。
单扫描极谱的i~E曲线与经典极谱不同,它呈峰形(如图5-3)。峰电流(ip)的大小与被测物质的浓度成正比,据此进行定量分析。峰电位(Ep)是被测物质的特征量,与被测物质的浓度无关,据此可进行定性分析。单扫描极谱曲线出现的峰状,是由于加在滴汞电极上的电压变化速度很快,当达到待测物质的分解电压时,该物质在电极上迅速还原,产生很大的电流,随后由于电极附近待测物质的浓度急剧降低,扩散层厚度随之逐渐增大,直到扩散平衡,电流又下降到取决于扩散控制的值。对于在电极上呈可逆反应的离子,所得ip较大,峰形较尖锐;而电极过程呈不可逆反应的离子,所得ip较小,甚至无峰。

图5-3 Pb2+在3mol/L HCl-1mol/L NaCl中的示波极谱图
ip-峰电流;id-极化电流;ab-基线;de-波尾;c-波峰
对于可逆极谱波来说,单扫描极谱峰电流与被测物质(去极剂)浓度成正比,且符合如下关系式:
ip = kn3/2D1/2υ1/2Ac
式中ip---峰电流,A;
k---复杂的常数,其值在25℃时为2.69×105;
n---电极反应中的电子转移数;
D---去极剂在溶液中的扩散系数,cm2/s;
υ---电压改变的速率,V/s;
A---电极面积,cm2;
c---去极剂浓度,mol/cm3;
公式表明ip ∝ c,这是定量分析的依据。同时,ip∝υ1/2,由于单扫描极谱的扫描速率比经典极谱快得多,所以ip比经典极谱中的极限扩散电流要大得多。对可逆体系来说,灵敏度比经典极谱提高了三个数量级。但扫描速率不能太快,太快的扫描速率会降低信噪比,不利于提高灵敏度。
单扫描极谱有很多优点,主要是再现性好、灵敏度高(可测至10-7mol/L)、在荧光屏上记录的瞬间电流可立刻读数,使极谱的测定快速;对某些电极反应不灵敏的离子可以用来减少其干扰,如氧在电极上的反应不可逆,因此在一些单扫描极谱分析中不需要预先除氧。一般说来,凡是经典极谱上能得到极谱波的物质亦能用单扫描极谱法测定。当测定某些金属离子,由于电极反应的可逆性差,或存在大量先还原物质致使单扫描极谱波波形欠佳时,使用导数示波极谱法往往能得到清晰的波形,提高测量的精确度和重现性。
-
+关注
私聊
-

yhl-87_
第35楼2009/11/09
电化学分析法(36)—交流、方波、脉冲极谱法
5.3 交流、方波、脉冲极谱法
A 交流极谱法
此法是将一个小振幅(几毫伏至几十毫伏)低频(≤100Hz)的正弦电压叠加在直流极谱的直流电压上面,通过测量电解池的交流电流来确定电解池中被测定物质的浓度的方法。交流极谱波具有导数曲线的形状,为一峰形波。交流极谱比经典极谱分辨率好,两峰相差40mV即可分开,氧的干扰较小,但不能提高分析灵敏度。
B 方波极谱法(Squarewave polarography)
此法是将一个低频率小振幅(一般≤50mV)的方形波电压叠加在直流极谱的直流电压上面,并在方波电压改变方向前的一瞬间记录通过电解池的交流电流成分的极谱方法。方波极谱波与交流极谱波图形相像,都是具有导数极谱曲线形状的峰形波,峰电流正比于待测物质的浓度,这是方波极谱作为定量分析的依据。而方波极谱优于交流极谱的是它能够消除或减少双电层电容电流的影响,从而提高了测定灵敏度。
方波极谱的特点是分辨率好、灵敏度高。对于可逆体系,灵敏度可达5×10-8mol/L。前还原电流影响小,在5×104倍先还原物质存在下,它仍可测定微量后还原物质。因此,该法在痕量分析中有着广泛的应用,如已广泛用于合金、钢铁材料、矿石、水样、食物、肥料等物料的分析。
-
+关注
私聊
-

yhl-87_
第36楼2009/11/09
电化学分析法(37)—脉冲极谱法
C 脉冲极谱法 (Pulse polarography)
此法是在一个缓慢改变的直流电压上面,在滴汞电极每一汞滴后期的某一时刻,叠加上一个方形脉冲电压,并在脉冲结束前的一定时间范围内,测量通过电解池的脉冲电流的极谱方法。根据所加脉冲电压的方式不同,可分为常规脉冲极谱(简称脉冲极谱)和微分脉冲极谱两种。这两种脉冲极谱的区别如图5-4所示。微分脉冲极谱是在每一汞滴增长到一定时刻(如1s或2s),在直流线性扫描电压上叠加一个2~100mV的脉冲电压,每次加入等幅脉冲,脉冲持续时间为40~80ms,比方波极谱(一般为几毫秒)的长。由于在脉冲后期测量电解电流,使得电容电流和毛细管噪声电流得以充分衰减。因为此法是测量电极上电位改变ΔE后的电流的改变Δi,所以得出类似于导数曲线的峰形波。对于常规脉冲极谱来说,所加电压为阶梯形脉冲,脉冲幅度随时间呈线性增加,时间间隔与微分脉冲极谱一样,由于此法是测量电极上的扩散电流平台的电流值,所以得到的图形类似于经典极谱波的图形。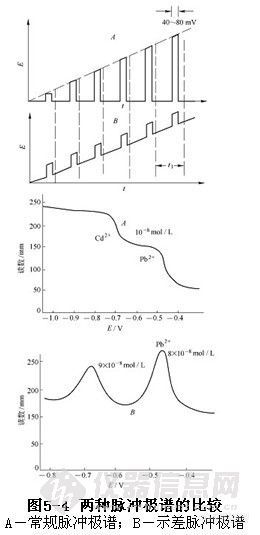
脉冲极谱具有灵敏度高,选择性好和支持电解质用量少等优点。脉冲极谱测定法对于呈可逆反应和不可逆反应的物质的检出浓度分别可达10-8mol/L和5×10-8mol/L,特别是对于呈不可逆电极反应的物质的测定灵敏度比方波极谱测定灵敏度提高了约100倍。采用微分脉冲极谱法,分辨率高,因为波呈峰形,前还原物质允许量可达5000:1,能分辨峰电位相差25mV的两种物质。另外,由于脉冲极谱中的脉冲电压持续的时间较长,相应地允许电解池的内阻要大一些,这就可以使用较低浓度的支持电解质(允许10-2~10-3mol/L),从而减少支持电解质中杂质的干扰。
-
+关注
私聊
-

yhl-87_
第37楼2009/11/09
电化学分析法(38)—催化极谱法
5.4催化极谱法
催化极谱法是利用极谱催化波以提高极谱分析灵敏度和选择性的一种分析方法。极谱催化波是指在进行电极反应的同时有电催化反应或化学催化反应而形成的特别灵敏的极谱波。
A 平行催化波
平行催化波是指去极剂的电极反应与反应产物的化学反应平行进行,而化学反应再生出的去极剂又在电极上还原,形成催化循环所产生的极谱波。它属于动力波的一种,极谱电流是受与电极反应平行的化学反应速率的控制,比去极剂的扩散电流大得多,从而提高了测定的灵敏度。此化学反应的速度越快,所得到的催化电流也越大,极谱分析的灵敏度也越高。平行催化波的反应过程可以下式表示:
式中A为去极剂,B为电极还原反应的产物,Z为氧化剂。由于化学反应再生了A,使在电极反应中所消耗的A又在化学反应中得以补偿,其浓度在最终溶液中基本不变。实际上产生催化电流所消耗的物质不是A,而是化学反应中的氧化剂Z。从此意义上看,可以把A称为催化剂。此外,催化体系中常存在络合剂。选择适当的络合剂,使金属离子以络离子的形式还原,电极过程可逆。当平行催化波发生时,若电极上或电极过程不存在吸附现象,波形与经典极谱波相同;当金属络离子等在滴汞电极上有吸附现象时,即使在经典极谱仪上也出现峰形催化波,往往使分析灵敏度比极谱扩散波高出几个数量级。催化电流与去极剂(催化剂)的浓度,在一定范围内呈线性关系。铂、钨、钒、铌、锡等元素均可在一些体系中产生平行催化波,利用该波可以测定这些微量元素。在经典极谱仪上可测离子浓度达10-6~10-8mol/L,甚至10-9~10-10mol/L。
-
+关注
私聊
-

yhl-87_
第38楼2009/11/09
电化学分析法(39)—催化氢波
B 催化氢波
氢离子在滴汞电极上还原的氢波称为正常氢波。由于在汞电极上析出氢的电极反应速度很慢,所以具有很大的超电位,而氢离子一般在-1.2V左右才能在滴汞电极上还原。催化氢波就是指在酸性或缓冲溶液中某些痕量物质(催化剂)的存在能减低氢的超电位,使氢离子比正常氢波在较正的电位下放电还原所产生的极谱波。由于其催化剂在滴汞电极上往往有吸附现象,使催化氢波的波形经常呈峰状。在一定浓度范围内,催化剂与催化电流呈线性关系。因此氢的催化波可以作为测定催化剂(浓度低至10-6~10-10mol/L)的灵敏方法。
C 络合吸附波
络合吸附波是指某些金属的络合物吸附于电极表面,所产生的灵敏的极谱波。它不同于一般的络合物极谱波,也不同于有机化合物的单纯吸附波,而是同时具有络合和吸附两种特性的波,并有增加电流的作用。与普通极谱波相比,其灵敏度的提高主要是由于吸附特性。吸附一方面起到富集去极剂的作用,另一方面也起了催化(即加速电极过程)的作用。这类波通常在单扫示波极谱仪上测定,其优点是极化速度快,吸附效果明显,有灵敏的波峰,特别是其导数波有尖锐的峰形,有利于提高分辨率。在一定浓度范围内,峰电流与金属离子的浓度成正比。能与金属离子形成络合物吸附波的有机络合剂有茜素络合剂、偶氮染料、三苯甲烷染料、氢醌染料和铜铁试剂以及8-羟基喹琳、四环素等抗菌素等类。一些重金属(如镉、铅、铋、铜等)离子,稀有稀散元素(如镓、铟、铀、钍)以及稀土元素、碱土元素等均能形成灵敏的络合吸附波。这类催化波已广泛应用于矿石分析中的微量金属离子的测定。
-
+关注
私聊
-

yhl-87_
第39楼2009/11/09
电化学分析法(40)—阳极溶出伏安法
6 溶出伏安法 (Voltammetry)
6.1 阳极溶出伏安法
极谱法和伏安法的区别在于极化电极的不同。极谱法使用的是滴汞电极或其他表面周期性更新的液体电极;而伏安法使用的是固体电极或表面静止的电极,如悬汞电极、汞膜电极(银基、玻璃碳等)、铂、金、银电极、微电极、化学修饰电极等。其中化学修饰电极已有专著出版[1,2]。阳极溶出伏安法又称反向溶出伏安法,是指被测定的物质在一定电位条件下电解一定的时间,于电极上进行电还原浓集,然后施加反向电压,使浓集在微电极上的物质再氧化溶出。溶出伏安图呈峰状波,其形状与单扫极谱图相似。溶出峰电流通常在一定范围内与被测物质的浓度成正比。此外,还有阴极溶出伏安法,它与阳极溶出伏安法不同的是浓集过程为电氧化,其溶出过程是电还原,微量S2-、Cl-、Br-、I-等阴离子的测定均有相应的阴极溶出伏安法。阳极溶出伏安法包括预电解浓集(电积)和溶出两个过程。浓集过程就是控制阴极电位电解,一般情况下,电位控制在比被测离子的半波电位负300~400mV范围内,使被测金属离子在工作电极上析出,在电极表面形成汞齐或难溶物,因此浓集应在充分搅拌的情况下进行。当搅拌速度、电极面积、溶液体积等保持恒定的条件时,控制电积的时间就成为影响灵敏度高低的主要因素。对悬汞电极来说,电积时间大约是:5min,10-6~10-7mol/L;15min,10-8mol/L;60min,10-10mol/L。电积时间一般是在几秒至几分钟的范围内,随着电积时间的增长,测定灵敏度提高,但电积时间过长会降低准确度;对含量特别低的成分,作较长时间的电积也是必要的。溶出过程是伏安测定过程,即极化电压按一定的速率(一般在20mV/s以上)向阳极方向线性地变化,使电积在工作电极上的被测金属溶出,产生阳极氧化电流,得到i-E溶出伏安图。溶出峰电流除了受待测物质浓度的影响之外,还受到电极的性质和表面积、电积时间、搅拌速度、扫描速率以及溶液体系(包括溶液的粘度、被测离子的扩散系数、电荷数)等因素的影响。阳极溶出伏安法是目前灵敏度很高而成本又比较低的痕量分析方法,其灵敏度可与无火焰原子吸收光谱媲美,而成本却远远低于后者。溶出过程可以使用经典极谱仪、单扫描示波极谱仪、方波极谱仪、脉冲极谱仪等各种极谱仪,所得的溶出峰电流比所用的相应极谱仪的阴极还原波峰电流灵敏2~4个数量级。阳极溶出法的测定范围在10-6~10-11mol/L,检出极限可达10-12mol/L,它能同时测定几种含量在10-9,甚至 10-12范围内的元素。目前已有30多种元素能进行阳极溶出分析,十几种元素可作阴极溶出分析,其中铬、钼、锰、铁、钴、铊、铅等元素既可作阳极也可作阴极溶出分析。
-
+关注
私聊
-

yhl-87_
第40楼2009/11/09
电化学分析法(41)—半微分溶出伏安法
6.2 半微分溶出伏安法
半微分溶出伏安法是一种对电解池电流进行后置处理的新极谱法。它是通过改善波形来提高灵敏度和分辨率。新极谱法包括(1)半积分电分析法,系记录电流的半积分m和电压E的关系曲线;(2)半微分电分析法,系记录电流的半微分e和电压E的关系曲线;(3)1.5次微分和2.5次微分极谱法,系记录电流的1.5次微分e或2.5次微分e"和电压E的关系曲线。以上统称为新极谱法,其灵敏度和分辨能力近于脉冲极谱法,且具有许多优点:仪器结构远比示差脉冲极谱仪简单、廉价,记录速度快,尤其适用于快速分析和快速电极反应的研究,在底液中的支持电解质浓度很低,甚至不存在的情况下,也可以进行测定等。
半微分阳极溶出伏安法是指将被测定的金属离子经过电解浓集于悬汞电极、汞膜电极或圆盘电极,然后测定氧化电流的半微分量(e)的方法。同样,1.5次微分或2.5次微分阳极溶出伏安法是记录氧化电流的1.5次微分量(e)或2.5次微分量(e")。在电极面积及其转动的角速度、预电解时间、电压扫描速率、溶液的粘度等条件固定情况下,e(或e,或e")与被测定物质的浓度成正比,这种关系是定量分析的基础。随着微分阶次的增加,峰形逐步尖锐,有利于提高分辨能力。在同一扫描速率(特别是速率较快)情况下,随着微分阶次的增加,峰高也大幅度地增加,因此这种方法有利于提高灵敏度。此法灵敏度高,其最低检出限可达10-12;分辨能力好,允许存在大量前还原物质;适用于快速扫描;仪器装置比较简单。