-
+关注
私聊
-

nphfm2009
第23楼2013/08/06
 应助达人
应助达人请问这个图说明了什么问题,怎么看这个图啊
不同pH值下不都是铬酸根离子吗,并没有重铬酸根离子的存在啊,
还有“要点:加入盐酸后,溶液务必呈酸性(PH=<1),(加热煮沸除碳酸根、亚硫酸根、硫离子,因为在酸性条件下,铬酸钡溶解生成的铬酸根,变重铬酸钾根后,会还原亚硫酸根和硫离子自身变成三价铬离子,导致溶液中有过多的钡离子,虽然硫酸根能沉淀完全,但到后续氨性条件下,本应释放出的铬酸根又部分复合成铬酸钡,使测定结果偏低,此外,较多的碳酸根也会缓慢地少量地转化铬酸钡,释放出铬酸根来,又使结果偏高。”
老师,对这些怎么理解啊,反应一定要再酸性条件下,那铬酸根岂不是变为重铬酸根了???老化验工(zlhuang0132) 发表: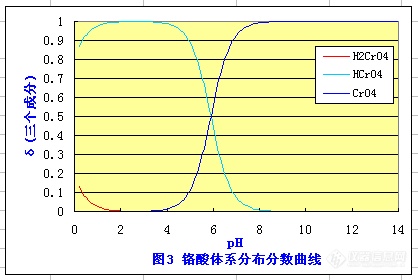
这是它们转化的分布分数
-
+关注
私聊
-

老化验工
第24楼2013/08/06
(1)这是三种含铬酸根的分布分数随PH值变化的曲线图,在任何PH值下,三个分布分数值之和为1,各值在0-1之间变化,分布分数值也就是某种成分浓度在三者浓度之和中所占的比例(重铬酸根不在此浓度和中,因为它是另外的酸根体系:重铬酸根了)。
该图说明在任何指定的PH值下,谁占的浓度比例是多少,这个比例乘总浓度(此总浓度不含重铬酸根)就是该成分的平衡浓度。
(2)对于弱酸、弱碱而言,PH不同,电离程度不同,因而各成分所占的比例不同,分布分数就是一组定量表示它们的分配及转化的化学参数(在分析化学酸碱滴定一章中有详细介绍)。并不是所有PH值下都是铬酸根!正如铵盐本来是以铵根存在NH4+,但如果你不断地加氢氧化钠调整铵盐溶液的PH值,则随着PH值的升高,从PH5以后,铵根浓度会降低,氨浓度会增大,如果你调到PH9.26,则铵与氨各点一半,调到12以上,几乎全变成氨了,这是平衡移动的原因,而分布分数则可以定量描述平衡移动的状态。
重铬酸是强酸,几乎不存在重铬酸和重铬酸氢根,因为它完全电离成重铬酸根了,因而没有分布分数曲线(只能画出一条重铬酸根等于1的水平线,其他质子化的二酸根视为0)。
(3)这个方法的原理是,用重铬酸钡来定量转化试液中的硫酸根,若在中性或微酸性,重铬酸钡转化成硫酸钡的过程是漫长的,可能是不定量的,但若先让铬酸钡因强酸化而溶解,则酸性释放出大量的钡离子后,少量的硫酸根就能完全沉淀,然后再调PH值至碱性,剩余的钡离子与全部重铬酸根重新转化成的铬酸根再沉淀,就可留下部分铬酸根不能沉淀了(因为原来与之匹配的钡离子被硫酸根用掉了),这部分不沉淀的铬酸根就是我们要测量的部分,它们的量与硫酸根的量“等摩尔数”。
在PH=<1,可以保证所有的铬酸钡都能溶解。
这个置换测定法的原理比较复杂,需要综合考虑。nphfm2009(nphfm2009) 发表:请问这个图说明了什么问题,怎么看这个图啊
不同pH值下不都是铬酸根离子吗,并没有重铬酸根离子的存在啊,
还有“要点:加入盐酸后,溶液务必呈酸性(PH=<1),(加热煮沸除碳酸根、亚硫酸根、硫离子,因为在酸性条件下,铬酸钡溶解生成的铬酸根,变重铬酸钾根后,会还原亚硫酸根和硫离子自身变成三价铬离子,导致溶液中有过多的钡离子,虽然硫酸根能沉淀完全,但到后续氨性条件下,本应释放出的铬酸根又部分复合成铬酸钡,使测定结果偏低,此外,较多的碳酸根也会缓慢地少量地转化铬酸钡,释放出铬酸根来,又使结果偏高。”
老师,对这些怎么理解啊,反应一定要再酸性条件下,那铬酸根岂不是变为重铬酸根了???


