
方案摘要
方案下载| 应用领域 | 制药/生物制药 |
| 检测样本 | 其他 |
| 检测项目 | |
| 参考标准 | SFDA 2010版GMP |
针对车间冻干机灭菌要求,使其符合2010版GMP规范,现采用气化过氧化氢灭菌技术对洁净舱体进行灭菌。 购置1台博医康(BIOCOOL)TL-V100型汽化过氧化氢灭菌器,用于车间冻干机灭菌。进行完TL-V100型汽化过氧化氢灭菌的确认后,需达到预期无菌要求。
针对车间冻干机灭菌要求,使其符合2010版GMP规范,现采用气化过氧化氢灭菌技术对洁净舱体进行灭菌。
购置1台博医康(BIOCOOL)TL-V100型汽化过氧化氢灭菌器,用于车间冻干机灭菌。进行完TL-V100型汽化过氧化氢灭菌的确认后,需达到预期无菌要求。
本方案适用车间冻干机灭菌的冻干机灭菌。
整个冻干机内部灭菌中使用过氧化氢气体作为灭菌剂,对冻干机内的空气及暴露的物体硬表面进行灭菌操作,整个过程中使用TL-V100型汽化过氧化氢发生器以及35%过氧化氢溶液,对冻干机进行相关的灭菌操作。通过针对性的灭菌过程及相应的灭菌过程参数进行灭菌,确认冻干机内部区域及物品的暴露硬质外表面过氧化氢气体的分布均匀性并达到6个对数以上的广谱杀灭效果,对细菌芽孢、霉菌等微生物达到较好的杀灭效果。
本方案旨在证明针对冻干机进行的过氧化氢气体灭菌达到了预期的灭菌效果,即灭菌空间气体分布均匀性好、达到6个对数的芽孢杀灭效率(嗜热脂肪芽孢杆菌Geobacillus stearothermophilus,ATCC #12980)。
本设计方案遵循SFDA2010版GMP、PDA TR34等技术要求。
本设计方案仅适用于车间冻干机的灭菌。
本设计方案是根据用户需求标准起草。
◈EPA——Material Demand Studies:Materials Sorption of Vaporized Hydrogen Peroxide
◈房间内空气及物品细菌数量调查与对策[J].中国护理杂志,2001,36(1):50-51
◈GB 22216-2008 食品添加剂 —— 过氧化氢
◈灭菌技术规范 中华人民共和国卫生部
◈AAMI TIR 17 附录E
◈NHSRC building Decontamination Alternatives(实用建筑物灭菌技术)
◈2010年版药典 附录XVII 灭菌法
◈YY/T0567.5-2011医疗保健产品的无菌加工——在线灭菌
◈SFDA 2010版GMP
◈GAMP 5
◈汽化过氧化氢气体发生器(TL-V100):1台 外形尺寸:( L×W×H) 320mm×270mm×400mm
◈数据在线打印系统:1套 (标配)
◈无线平板控制系统:1套(选配)
◈过氧化氢浓度检测系统:1套(选配)
◈温湿度检测系统:1套(标配)
◈数据USB输出模块:1套(标配)
◈过氧化氢残留检测器:1套(选配)
◈审计追踪:1套(标配)
TL-V100型汽化过氧化氢气体发生器是将浓度为35%食品级过氧化氢溶液,通过汽化器汽化成过氧化氢蒸汽,将过氧化氢蒸汽输送到密闭空间内进行灭菌,具体原理图如下:
TL-V100系列工作原理图
汽化过氧化氢发生器是将浓度为35%的H2O2溶液(即双氧水),通过汽化器汽化成过氧化氢蒸汽,并通过喷头直接喷射到密闭空间或通过管道循环对密闭舱体进行灭菌灭菌的设备。
TL-V100汽化过氧化氢发生器的工作过程分三个阶段:
调节阶段:将过氧化氢溶液注入汽化器汽化成过氧化氢蒸汽,并通过风机输入到密闭空间内,直至达到预期的浓度;
灭菌阶段:继续输入过氧化氢蒸汽,并保持预期的浓度;
排残阶段:停止输入过氧化氢蒸汽,通过使密闭空间内的排风系统,将过氧化氢蒸汽循排出,直至密闭空间内的过氧化氢浓度降至允许的范围内。(注:如客户选配过氧化氢除残模块,可进行自动除残,直至密闭空间内的过氧化氢浓度降至允许的范围内)
5.1.1 基本结构描述
(1)外观
TL-V100型汽化过氧化氢气体发生器整体采用304不锈钢喷塑工艺,整体视觉良好并易于清洁。主操作面采用智能控制程序对TL-V100型汽化过氧化氢气体发生器进行模块化控制,.可选配无线平板远程控制,同时在设备底部设置有万向脚轮,背面设有拉杆便于在房间内部移动。
设备外部进出气管路均采用标准型接口进行,进风口/出风口均采用标准型DN32快装接口,易于拆装、更换方便。

TL-V100汽化过氧化氢发生器整体示意图
(2)单片机控制:
运行参数实时显示;
阶段之间自动切换;
外形尺寸:(长×宽×高)320mm×270mm×400mm
重量:20kg
5.1.3公用介质参数
电源:AC220±22V 50Hz±1Hz;
5.1.4性能特点
功率:1800W
空气流量:大于48m3/h
注射速率:1~10g/min
汽化温度:≤135℃
载气过滤效率:99.9999%
灭菌剂:35%食品级过氧化氢溶液
灭菌容积:≤200m³
灭菌效力:对嗜热脂肪芽孢杆菌的杀灭能力达到106
洁净度:灭菌后,保证洁净室内的无菌环境;
分布均匀性测试:通过化学指示剂进行密闭空间内部布点,确保内部VHPS良好的分布均匀性;
工作方式:连续工作
5.1.5使用环境
灭菌环境温度:≥ 20℃
相对湿度:≤40% RH
空间密闭性良好
5.1.6安全
设备外表面温度较高的部位设置有明显的警示标识;
过氧化氢溶液更换处有明显的警示说明;
控制系统能够抵抗手持无线电设备和设备周围1米范围内的手机信号干扰。
主要成分过氧化氢35%,具有广谱杀菌能力,对细菌、真菌、放线菌、芽孢、病毒等都有显著效果。适用于制药、生物技术、医学产品生产、实验室等等,分解后不会产生任何有害残留,只有水和氧气。
2H 2O2=2H2O + O2↑
通过使用空间残留检测仪,采用对过氧化氢敏感的检测仪,在1小时除残后,可验证过氧化氢残留量。OSHA(职业安全与健康标准)要求过氧化氢残留小于1ppm。
嗜热脂肪芽孢菌片(芽孢数10的6次方以上)
【产品说明】
本品符合 2020 新版《药典》,采用 Geobacillus stearothermophils (ATCC 12980)作为指示菌,由芽孢钢片、恢复培养基、灭菌管构成。当灭菌合格,经培养指示剂颜色保持紫色不变;不合格,则指示剂颜色由紫色变为黄色。
【使用范围】
适用于汽化过氧化氢空间灭菌效果监测。
【使用方法】
1.在指定位置纸面朝上放置芽孢菌片袋,进行灭菌。(或从菌片袋中取出芽孢钢片,可让钢片放置在平皿内,将其暴露于各个灭菌位点,进行灭菌,灭菌后立即盖上无菌皿盖。)
2.灭菌处理后,将菌片袋(平皿)移至超净工作台,在无菌条件下,用无菌镊子从菌片袋(平皿)里取出芽孢钢片,放入同批次配套培养基中(镊子使用前置于酒精灯外焰处灼烧 2-3s,并遵循一次一消原则,保证镊子无菌)。
3.将培养基瓶盖拧紧后,插入常规恒温培养箱内,在 55~60℃温度间培养 24 小时。
4.阳性对照:从未经过灭菌处理的芽孢菌片袋中取出芽孢菌片放入培养基中,同时进行培养。每次培养时都必须使用阳性对照。
【结果判定】
1.培养 24 小时后观察,培养液颜色由紫色变成黄色, 说明灭菌不完全, 请重新进行灭菌。
2.若培养液颜色保持紫色不变, ,则可判断灭菌完全。
3.只有对照管生物指示剂的培养液颜色必定由紫色变成黄色呈阳性,其生物学检测结果才算有效。
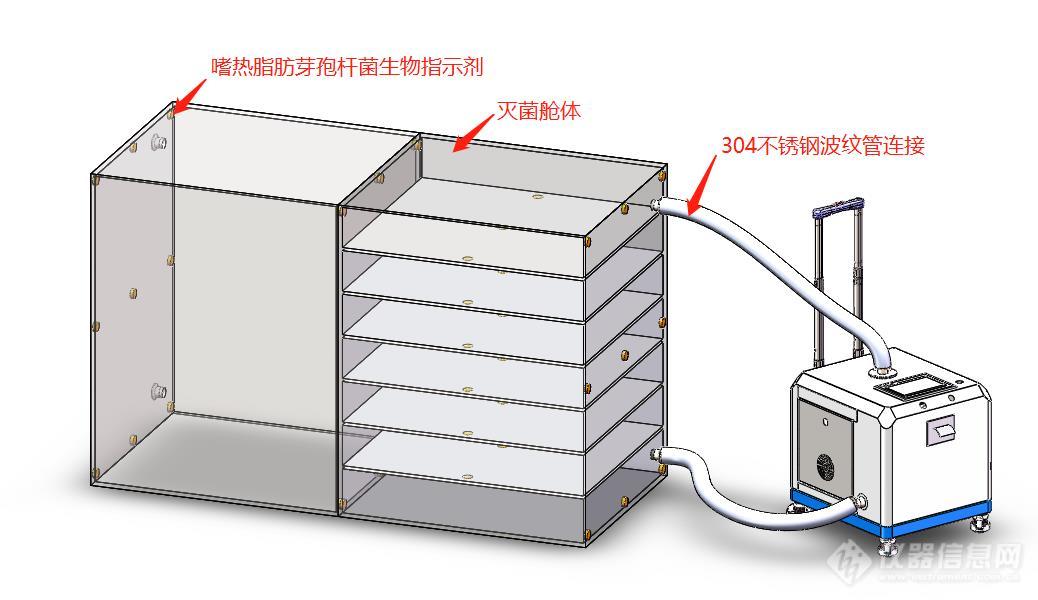
舱体的灭菌采用管道循环灭菌方式。设备安放示意图如下:
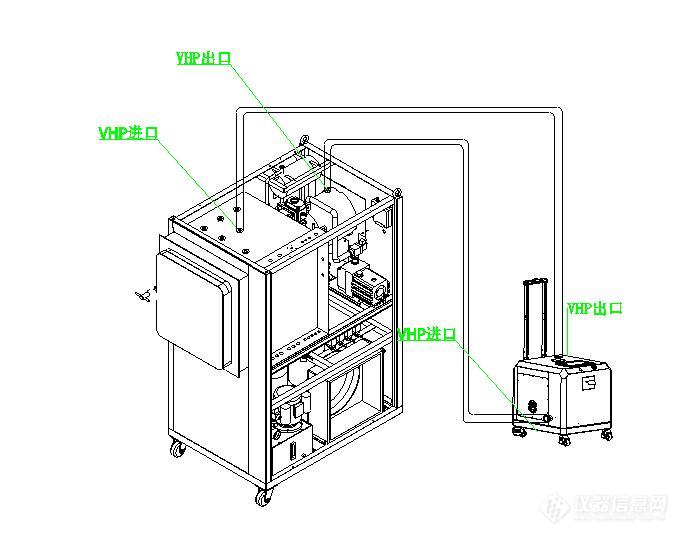
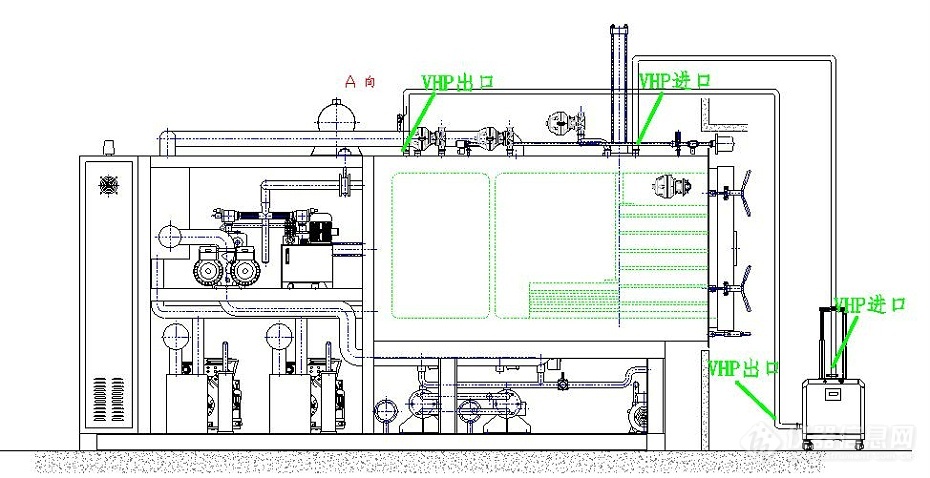
7.2.1 准备阶段
检查设备运行环境及设备电源等各部正常;
将设备推入灭菌设备旁( 设备上下延伸管路对接冻干机的进出口位置)
检查发生器储液瓶中过氧化氢溶液,佩戴护目镜和橡胶手套等必要的防护后向储液瓶内倒入足量的过氧化氢溶液。
连接TL-V100汽化过氧化氢发生器电源,打开电源开关 。
7.2.2 自动运行阶段
7.2.2.1 调节阶段
将过氧化氢溶液注入汽化器汽化成过氧化氢蒸汽,并喷射到冻干机内部,直至达到预期的浓度要求;
调节阶段结束后,设备自动进入灭菌阶段;
7.2.2.2 灭菌阶段
自动调节加药量,继续向冻干机内部注入过氧化氢蒸汽,并保持预期浓度;
灭菌阶段结束后,设备自动进入除残阶段;
7.2.2.3 静置阶段
加药完毕后,静置约1 小时,使过氧化氢灭菌气体与空气及物体表面充分接触,保证灭菌效果;
7.2.2.4 排残阶段
灭菌结束后,房间的排气系统进行排残,直至过氧化氢浓度低于1ppm;(或选配过氧化氢除残模块,可进行自动除残,直至密闭空间内的过氧化氢浓度低于1ppm)
排残结束后移除过氧化氢发生器及相关辅助设施。
使用的过氧化氢溶液为35%食品级过氧化氢溶液,否则可能会影响灭菌效果;
更换储液瓶中的过氧化氢溶液时必须佩戴防护手套和护目镜,避免过氧化氢溶液飞溅到皮肤和眼睛上,造成不必要的伤害;
汽化过氧化氢气体发生器处于通电运行状态或运行停止后不久,出风口和排气口连接装置及连接管路温度较高,严禁触摸。
过氧化氢发生器开启灭菌过程中严禁点击【停止】、【启动】等按键,严格按照操作规程进行操作。
备注:实验前准备项目
物品 | 数量 | |
1 | 220V电源 | 若干 |
2 | 插座 | 若干 |
3 | 密封胶条 | 若干 |
4 | 250ml量筒 | 1个 |
5 | 1000或2000ml量筒 | 1个 |
6 | 5L烧杯 | 1个 |
7 | 漏斗 | 1个 |
8 | 手套 | 若干 |
9 | 洁净服 | 若干 |
10 | 无菌空平皿 | 15个(实际数量略多于芽孢条放置点数量) |
11 | 恒温培养箱 | 1个(55-60摄氏度细菌培养箱) |
1、常规检测:
使用TL-V100汽化过氧化氢灭菌系统进行舱体灭菌不需您改变任何的常规检测方法和步骤。通常都是使用如接触平板法或擦拭法进行表面检测和其它的空气检测方法如沉降法。
生物指示剂菌种信息:Namsa Bacillus atrophaeus(ATCC 9372)
2、使用孢子条验证实验(参考做法):
使用器具:无菌平皿15个,无菌镊子, TSB干粉培养基。
3、培养基无需配制:
3.1 设计孢子条放置位置,给无菌平皿编号。
3.2(此过程无菌操作)在开始灭菌之前把孢子条字体一面朝上放在无菌平皿内,放在指定位置,打开平皿盖。
3.3 开始喷雾灭菌---消毒结束。
3.4(此过程无菌操作)收集各个位置的孢子条,盖上平皿盖。
3.5 在实验室工作台内把平皿内的孢子条包装打开用无菌镊子夹入无菌的装有TSB无菌培养基的管内,摇晃几下使孢子条完全浸在培养基内。
3.6 将阳性对照孢子条放入培养基内培养。
4、培养方法:
50-55摄氏度温箱培养,24,48小时后分别观察。
空白对照,阳性对照,和样本观察培养基是否变浑浊,变黄。下图为参照图: 芽孢条培养结果
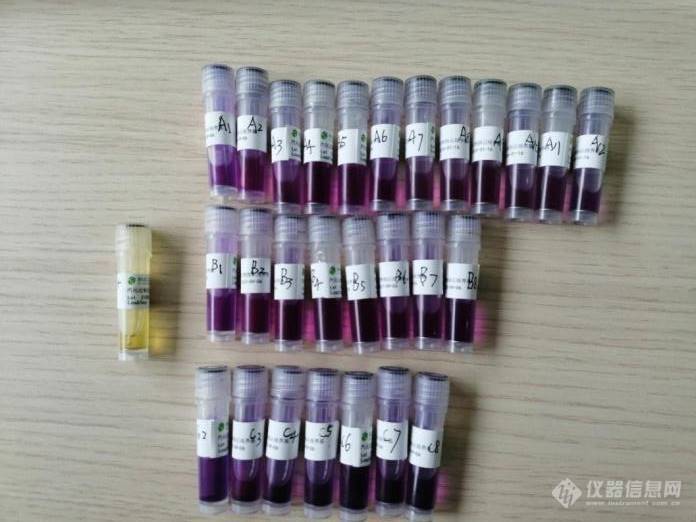


高均匀度氧化铝微球的制备
实验室中试冻干最佳解决方案
全功能型中试冻干机
博医康BIOCOOL-T系列“冰芯”冻干机
BIOVAC品牌直联旋片真空泵
博医康非标冻干机系统服务
博医康Smart冻干智能系统
博医康程序降温仪BIOCOOL smart-3
博医康程序降温仪BIOCOOL smart-2
博医康程序降温仪BIOCOOL smart-1
博医康真空冷冻离心浓缩仪FastDry-4
博医康真空冷冻离心浓缩仪FastDry-4E
博医康真空冷冻离心浓缩仪FastDry-3
博医康真空冷冻离心浓缩仪FastDry-3E
博医康真空冷冻离心浓缩仪FastDry-2
博医康真空冷冻离心浓缩仪FastDry-2E
博医康真空冷冻离心浓缩仪FastDry-1
博医康真空冷冻离心浓缩仪FastDry-1E

关注

拨打电话

留言咨询