氨基柱可在正相、反相、弱阴离子交换和 HILIC 模式下使用。其出厂时保存在纯异丙醇溶剂中,对不同的使用模式我们给出如下建议:
运行参数:
1. pH 范围:2.0-7.0
2.压力:ACE NH2 不得超过 4000psi(275bar);
ACE Excel NH2 不得超过 15000psi(1000bar)
3.柱温:不得超过 60°C
样品溶液的制备:
1.如可以的话,用流动相来溶解或稀释样品;如不可以,请先检查溶解后的样品在流动相中的溶解度;
2.进样前需使用 0.45 或 0.22μm 的滤膜过滤样品;
3.具有强酸或强碱性的样品,应将 pH 调节到色谱柱范围内再进样;
4.含蛋白样品要预先去除蛋白质,避免对氨基柱使用醛类和酮类化合物。
分析还原糖使用前后注意事项(特别重要):
保存好的 ACE NH2 柱(包括新柱),每次拿出来用于分析还原糖(异头物)之前,应按下列步骤进行操作来去除硅胶表面的质子,以便在开始分析之前获得最佳的峰形。
1.乙腈/水(7:3),冲洗 20 倍柱体积;
2.乙腈/水(7:3),加 0.1% v/v 氨水溶液(氨水溶液浓度约 32%),冲洗 50 倍柱体积;
3.乙腈/水(7:3),冲洗 20 倍柱体积;
冲洗前: 冲洗后:
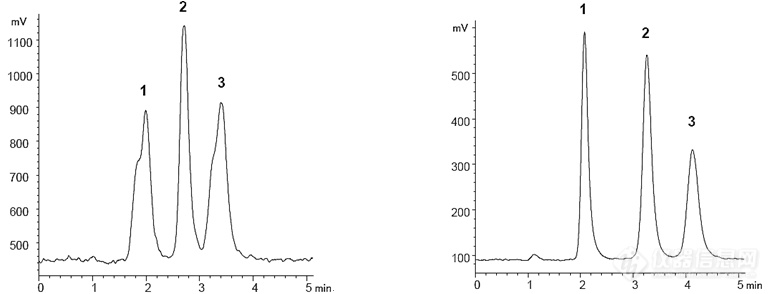
图 1. ACE 5μm NH2(50 x 2.1mm),用含有 0.1% v/v NH3 的乙腈/水(75:25)冲洗前后的糖分析对比图。
0.21mL/min, 35℃,RID. 峰 1=果糖,峰 2=蔗糖,峰 3=乳糖.
ACE NH2 柱长期保存条件:
为了最大程度上延长色谱柱使用寿命,使用后先用乙腈/水(1:1)冲洗 20 倍柱体积,再用 100%异丙醇冲洗 20 倍柱体积,然后取下柱子塞紧柱堵头放置。
正相条件下使用:
1.使用前:提前将系统管路内溶剂正确替换至将要使用的正相流动相,避免盐析出、溶剂不互溶等问题,再连接色谱柱,用流动相冲洗至少 10 倍柱体积,将封存溶剂替换掉,待基线平稳后进样;
2.使用后:适当增大流动相中的强洗脱溶剂比例进行清洗,最后保存在异丙醇或正己烷中;
3.再生:依次用 10 倍柱体积的氯仿、异丙醇、二氯甲烷、流动相分别进行冲洗(如有压力高的现象, 可按此程序进行反冲色谱柱);
反相、弱阴离子交换或 HILIC 条件下使用:
1.使用前:如色谱柱正保存在正相溶剂中,使用反相方法,必须先用两通连接系统和管路,用异丙醇冲洗,除去其中的乙腈、甲醇或水等。然后,再连接色谱柱,用至少 20 倍柱体积的异丙醇低流速冲洗过渡(一般对 250*4.6mm 色谱柱,0.5mL/min,需至少 3 小时;其它规格色谱柱请相应放大或缩小流速及时间),以除去正相保存溶液;再用至少 10 倍柱体积水/乙腈或甲醇(95:5)冲洗(不含缓冲盐的流动相可省去),最后用流动相平衡好即可使用。如色谱柱正保存在反相溶剂中,更换流动相时请确保新流动相与柱子原保存溶液可互溶,并不会导致盐析出。此步骤非常重要,如果没有充分过渡,会对柱效及保留时间等产生影响;
2.使用后:先用 95%水/有机相冲洗至少 10 倍柱体积,除去所用缓冲盐(不含缓冲盐的流动相可省去),再用 95%有机相/水冲洗至少 10 倍柱体积并保存。短期不用的话,可保存在反相溶剂中;若长期不用,用异丙醇保存。
3.再生:如正常清洗无效果并伴有压力升高的现象,可参照使用后清洗程序对色谱柱进行反冲;如果依然没有效果,可再用异丙醇低流速反冲。
色谱柱测试:
测试混标:咖啡因(140μg/mL)、尿嘧啶(85μg/mL)、尿苷(280μg/mL)混标溶剂:乙腈-水(90:10)
液相条件:见包装内测试报告进样量:2μL
第二届药物杂质分析分离学术研讨会即将召开
核苷酸专用柱是什么柱?菲罗门为您解答
HPLC和LC/MS 缓冲液选择指南:为什么要控制PH值?
【菲罗门】维生素HPLC分析知多少?
相关产品

关注

拨打电话

留言咨询