应用背景
免疫疗法是现代癌症治疗的关键组成部分,一些疗法已成功地应用于恶性肿瘤,但存在的非普适性及多副作用等问题仍未较好解决。RNA设计和递送的进步正在引领RNA免疫治疗的新时代,对癌症免疫学理解的实质性进步、个性化癌症抗原的识别以及RNA递送载体性能的优化,都将在下一代免疫治疗中发挥核心作用。
用于癌症疫苗的mRNA纳米颗粒
唯一获得批准的癌症疫苗是Sipuleucel-T,这是一种用于前列腺癌的自体树突状细胞疗法,于2010年获得批准,但由于其成本高且临床疗效不尽如人意,并未获得广泛使用。
下一代mRNA癌症疫苗的改进
mRNA癌症疫苗的改进可分为三个方向:1.增加可治疗的患者数量;2.提高RNA-LNPs的效力;3.提高其耐受性。
为解决第一个问题,需要更好地了解如何为更广泛的癌症患者设计抗原。以低突变负担癌症来讲,新抗原数量较少,可能需要额外的工具来改进抗原设计,神经网络和深度学习技术的进步,可利用多个数据源为抗原设计做出最佳预测。
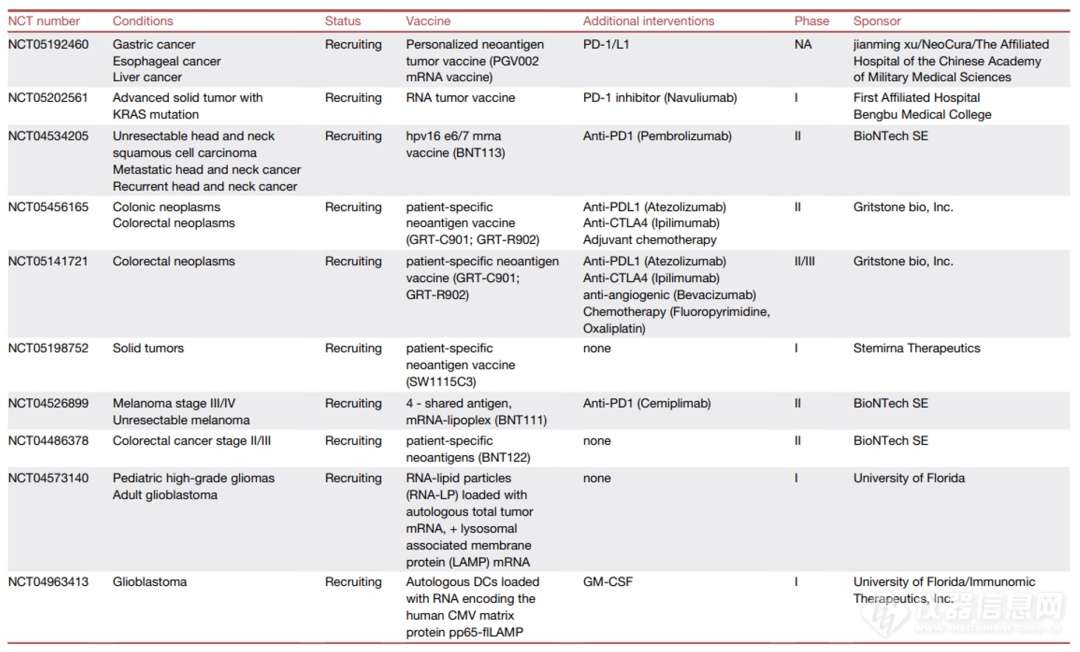
针对第二个问题,可电离脂质的开发虽然增加了mRNA的递送,但只有一小部分给药的mRNA被抗原呈递细胞(APCs)处理。将mRNA疫苗靶向具有MHC-I交叉呈递和CD8 T细胞活化能力的淋巴器官APCs,可能提高疫苗效力。例如BNT111,目前正处于黑色素瘤的II期临床试验中(见表1),并取得了良好的早期结果,该药物利用一种带负电荷的配方,可促进巨噬细胞和树突状APCs的特异性摄取。除了基于电荷的靶向,与LNP表面的配体偶联(例如,抗CD11c或DEC205抗体)也可以改善APC靶向,这些都可作为增强低RNA剂量下免疫反应的改进方向。
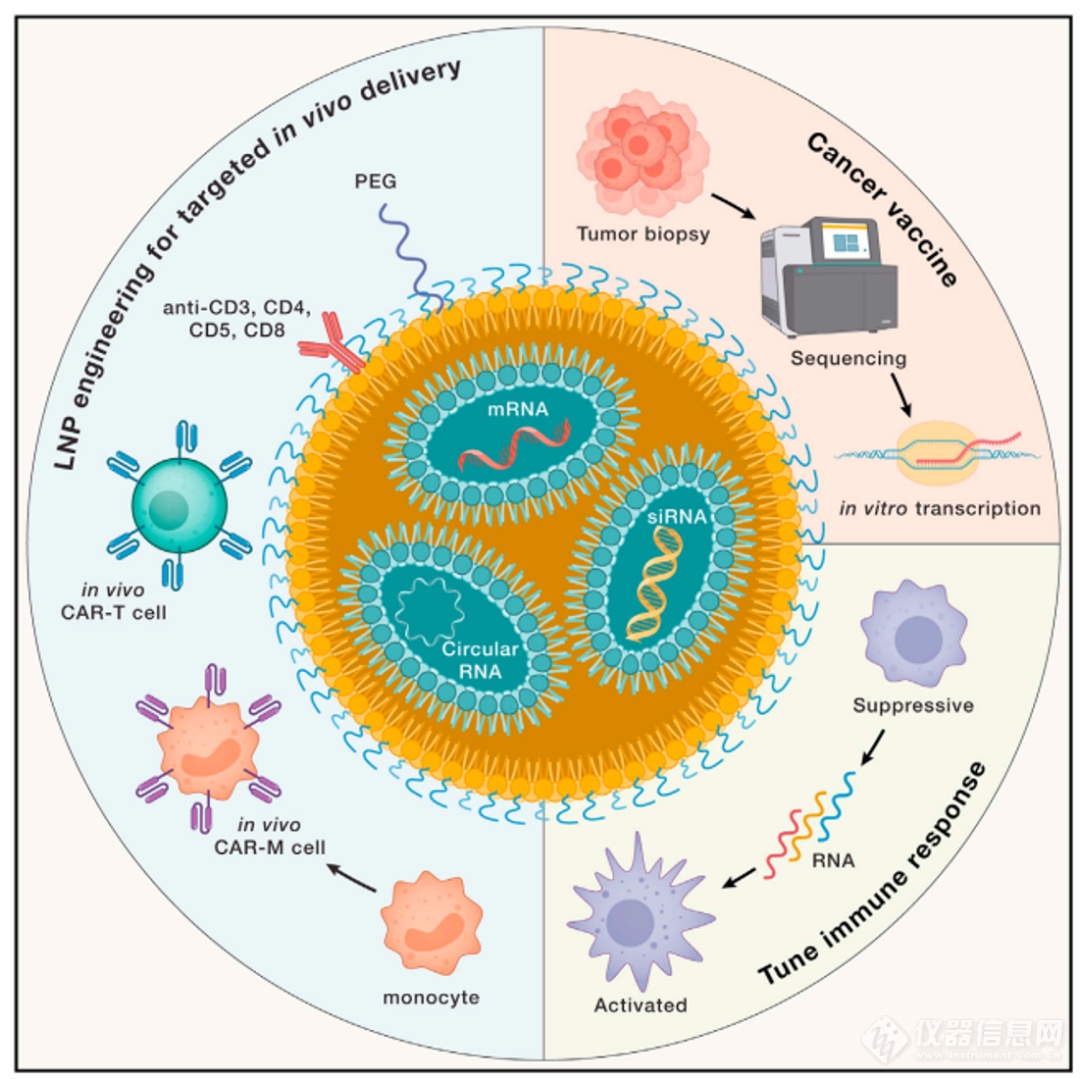
图1. RNA脂质纳米颗粒(LNPs)是模块化的工具,可精确地调整免疫反应
靶向RNA递送用于体内CAR治疗
体内RNA递送到T细胞是一种有吸引力的方法。即将CAR-mRNA封装到细胞类型特异性(即T细胞)的纳米颗粒中(图1)。这种基于mRNA-LNP的体内CAR-T生成除了具有时间和成本优势外,还可能带来治疗和安全性方面的好处。mRNA-LNP递送减轻了与现有CAR-T疗法中使用的慢病毒载体相关的插入突变的担忧。此外,mRNA表达的短暂性可以通过给药调节CAR-T水平,与已批准的疗法相比,这可能会降低毒性。
CAR-T应用中最大的挑战是增加LNP的特异性。关于T细胞表面受体配体(例如,针对CD3/4/5/8的抗体)结合到mRNA-LNPs上的潜在T细胞靶向已经得到了证明。在临床前,靶向抗体的共价吸附和静电吸附都已成功使用。提高偶联效率、控制配体的实际取向、设计更精确的靶向配体工程,都能提高LNP的效力。
将体内CAR疗法扩展到T细胞之外
与局部给药相比,全身输注使用更高剂量的RNA-LNPs之前需要免疫抑制,这是一个未被充分认识的挑战,因为免疫疗法需要具备一定的免疫功能。因此,对静脉注射RNA-LNPs有严重不良反应的患者可能无法接受这些治疗。
结论
免疫疗法的巨大成功表明,免疫系统仍然是我们对抗癌症最有力的工具之一。开发普适性的免疫药物,惠及更多的患者是所有研究人员、临床医生的共同努力目标。RNA疗法具有靶向特定基因、诱导免疫激活的固有能力,且易于通过靶向纳米颗粒在体内传递。尽管开发安全高效的RNA递送系统仍面临挑战,但相信,RNA纳米递送终将成为下一代免疫疗法的重要组成部分。
在生物3D打印中计算机辅助设计的作用
锘海LS18显微镜助力揭示脑-脂肪回路在慢性应激所致抑郁症和胰岛素抵抗中的作用
Thy1转基因小鼠样本不同分辨率成像解析案例
锘海组织三维成像技术助力解析小鼠半月板内血管分布特征

相关产品

关注

拨打电话

留言咨询