什么是自发荧光?
自发荧光即细胞发出的荧光,是由于某些生物结构(如线粒体和溶酶体等),在光下会发出荧光这一自然规律所造成的。大部分的荧光来自NADH、核黄素和黄素辅酶1。自发荧光是流式细胞术所面临的一个挑战,较高水平的自发荧光会干扰相关阳性群体的分辨率。
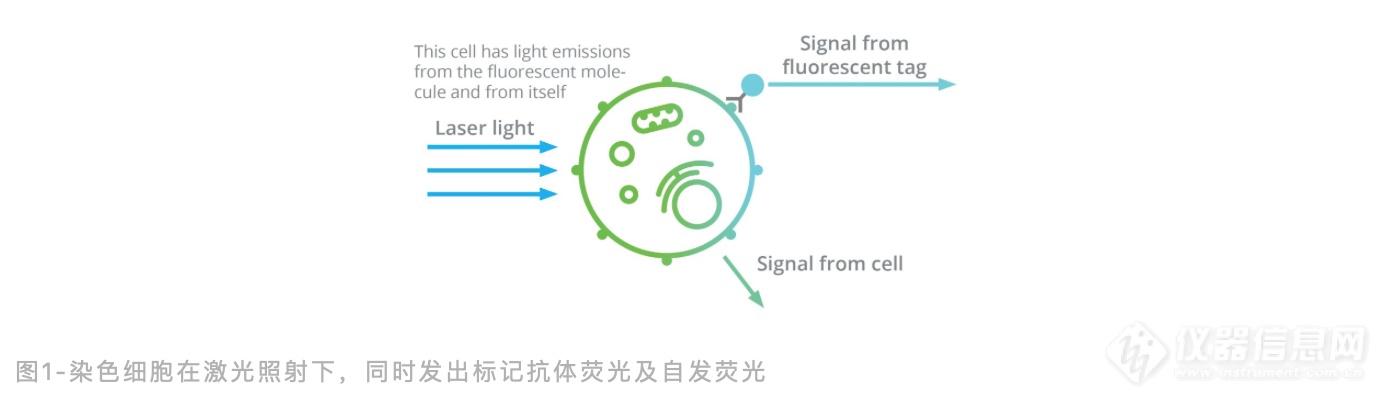
当使用的荧光分子比细胞发出的自发荧光亮很多的时候,自发荧光不会造成太大的影响;但当自发荧光与荧光分子发出的光量接近时,流式细胞实验就会受到很大的干扰。

改善高自发荧光样品的数据质量
Cytek Aurora 和 Northern Lights的全光谱检测和分析技术,可以实现自发荧光去除,使进一步提高数据的清晰度成为可能。某些样本类型,如酵母菌和肿瘤样本,存在较高的自发荧光,基于这些样本开展的流式细胞实验,是具有高度挑战性的。Cytek光谱流式细胞仪独特的光学检测系统,能够对未染色的细胞发出的自发荧光进行检测并获得其全光谱特征。配套SpectroFlo 软件的解析算法,在需要的情况下,可以将这些自荧光光谱作为一个单独的参数,从荧光数据中剔除出去。
利用Cytek光谱流式检测高自发荧光样品的应用实例
PrimeFlow™ RNA 检测
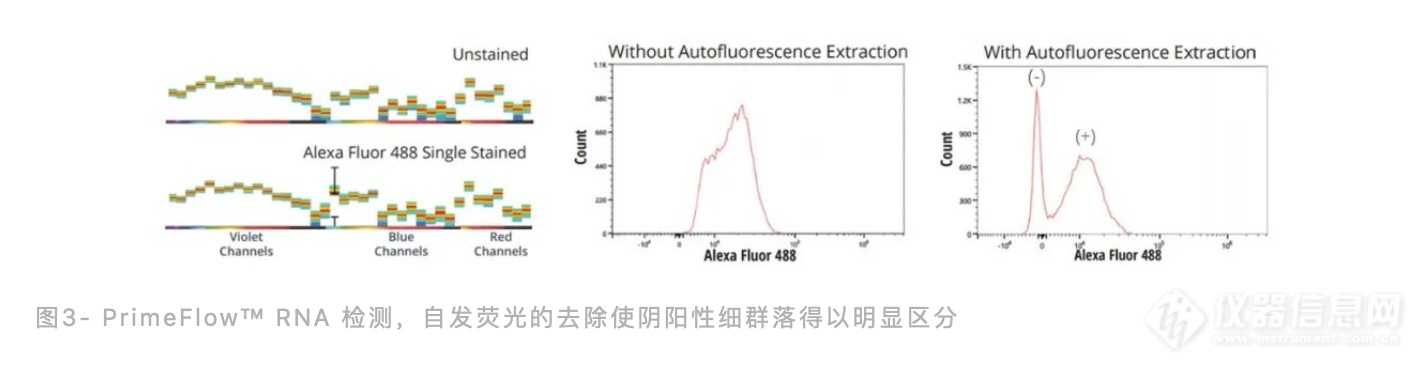
对人U937细胞进行PrimeFlow™RNA检测。通过一系列的杂交步骤,用Alexa Fluor®488荧光染料,对这些细胞HMBS基因的mRNA进行标记,HMBS是一种低表达基因(~10个拷贝/细胞)。在Cytek Aurora上对样品进行检测,使用SpectroFlo®软件进行分析,采用两种不同的策略,一种去除自发荧光,另一种不去除。
未染色和用Alexa Fluor®488标记的细胞在Aurora上获取后,发现两者荧光光谱很相似,重叠严重(图3左)。由于细胞的高自发荧光,阳性和阴性信号的分界是模糊的。去除自发荧光后,两个细胞群体的分辨率被大大提高了(图3右)。
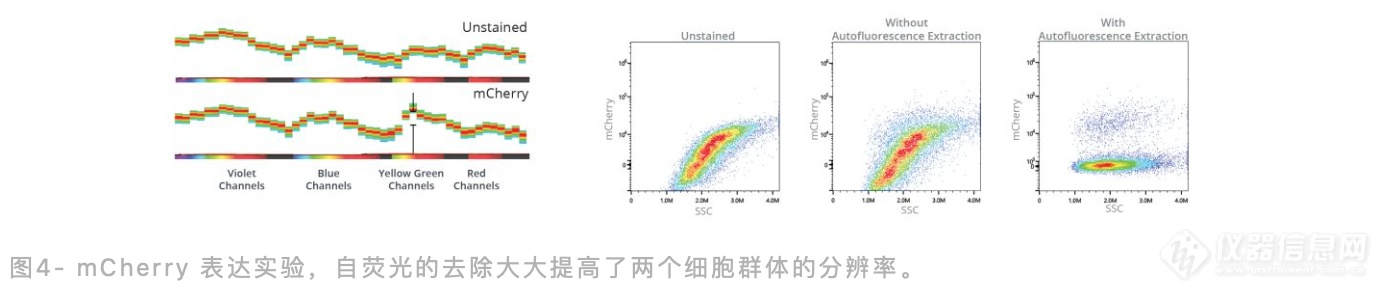
HeLa细胞的 mCherry 表达
用携带mCherry报告基因的CRISPR-Cas9靶载体转化HeLa细胞。mCherry的表达受敲入基因的内源性启动子驱动。感染后32小时收集细胞,用Cytek Aurora 流式细胞仪(四激光配置-V,B,YG,R)进行检测分析,评估mCherry荧光蛋白的整合情况。未染色的和携带mCherry的细胞发出的光谱在黄绿色通道中表现出差异。当不去除自发荧光时,阴性和阳性细胞几乎无法区分;去除自发荧光后,阳性细胞的分辨率被大大提高(图4)。(样品由EMBL (欧洲分子生物学实验室)流式细胞仪和细胞分选部门的Malte Paulsen提供)
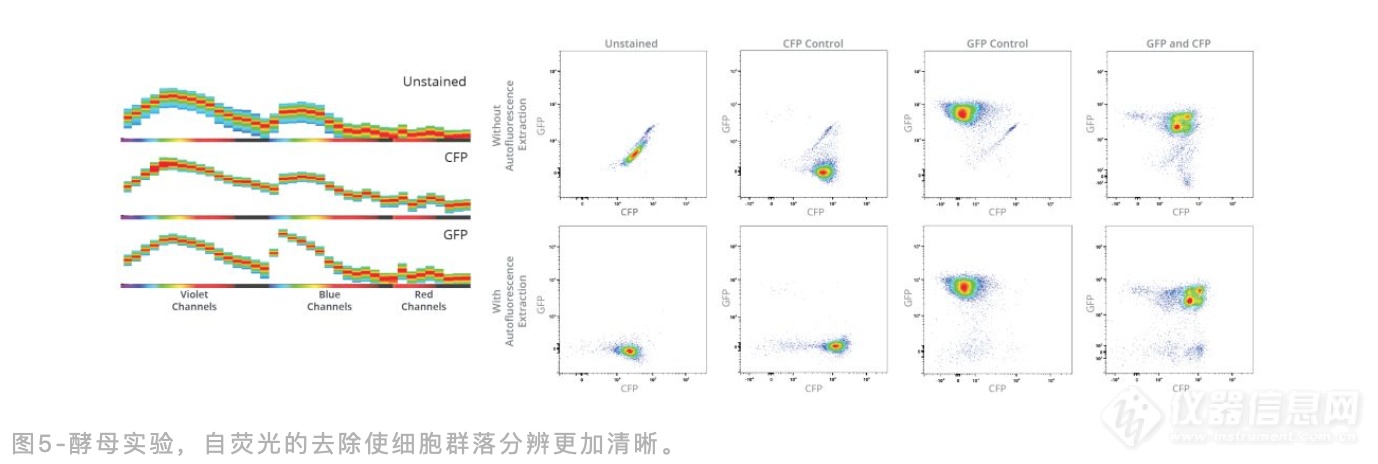
酵母的CFP和GFP 数据
如Thacker等人在参考文献2中所述,构建携带荧光蛋白报告基团的酿酒酵母菌株,以研究减数分裂的分离模式。在科罗拉多州立大学的Lucas Argueso实验室,使用四分体分离方法分离了分别表达CFP或GFP的对照菌株。这些菌株会在孢子形成时持续性地表达其中一种荧光蛋白。由于酿酒酵母的孢子拥有细胞壁、质膜和子囊(容纳孢子的囊),因此酵母有大量的自发荧光。在Cytek Aurora 流式细胞仪(三激光配置)上获取这些酵母样本,鉴别他们的自发荧光光谱特征,并对去除和不去除自发荧光的情况都进行了分析。全光谱特征和解析后结果的比较如图5所示,可以看到去除自发荧光后,细胞群落的分辨率的得到了很大的改善。
参考文献
1. Aubin, JE: Autofluorescence of viable cultured mammalian cells. JHistochem Cytochem 27:36–43, 1979.3
2. Thacker, D., Lam, I., Knop, M., & Keeney, S. (2011, October). Exploiting spore-autonomous fluorescent protein expression to quantify meiotic chromosome behaviors in Saccharomyces cerevisiae. Retrieved from https://www.ncbi.nlm.nih.gov/pubmed/21840861
装机量增加147台!Cytek Biosciences Q2营收4660万美元
全光谱自发荧光分选功能首发,解锁海洋生物免疫指纹密码
Cytek® Amnis® ImageStream®X Mk II流式图像交互,领略NF-κB 核转
高质量数据新标准,Cytek谱写45色全光谱流式方案二重奏(分析+分选)

相关产品

关注

拨打电话

留言咨询