
微生物抗生素耐药抵抗是当前全球性医疗问题,传统微生物耐药鉴定耗时过长,临床反馈时间滞后。为解决这一难题,我们引入了一种拉曼光谱结合重水标记(Raman - D2O)的方法,能快速检测微生物耐药性,辅助临床用药。
检测原理

在抗生素压力下,耐药菌的代谢活性远高于敏感菌。通过向培养环境中添加重水(D2O),对抗生素胁迫下的活性微生物群体进行标记,再利用拉曼光谱在单细胞层面检测微生物群体中的同位素峰(C - D),从而确定微生物的药敏结果[1]。
该方法基于免培养策略,可在 3 - 6 小时内得出结果。


检测流程

01
重水与抗菌剂孵育
制备菌液,设置实验组(NC)、阴性对照组(N)和阳性对照组(P),先进行抗菌剂孵育,然后将抗菌剂孵育后的NC和P组样品加入重水,N组样品加入无菌水进行孵育,随后清洗和制片。
02
拉曼光谱检测最小抑菌浓度
将制好片的BioRaman Chip拉曼芯片置于共聚焦拉曼光谱仪上,采集单细胞拉曼光谱。
03
肉汤稀释法 MIC 检测对照
采用肉汤稀释法检测微生物最小抑菌浓度(MIC),与拉曼检测结果进行比较。
04
数据分析
对拉曼光谱数据进行前处理,计算 CD ratio,确定拉曼 MIC 预测值。

检测结果

在重水与活性微生物孵育过程中,D2O中的D元素可以通过一些途径被吸收转化到细胞内的生物质中。因此微生物体内的D积累情况可以反映出其活性,可利用拉曼光谱检测通过CD比值(CD ratio = CD/(CD+CH))来表征。其中CH表示C-H 伸缩震动,体现在拉曼光谱中为2040-2300 cm-1处的光谱峰,CD表示同位素替代的C-D震动,体现在拉曼光谱中为2800-3100 cm-1处的光谱峰(Fig.1A)。
肉汤稀释法MIC的测定结果由肉眼确定,拉曼光谱法MIC由重水峰的决定(Fig.1B)。将大肠杆菌肉汤稀释法MIC结果与拉曼光谱MIC结果比较,如Fig.1C所示。大肠杆菌的MIC每种药物做了8个浓度梯度,每个梯度2倍稀释,图中绿色线框对应的浓度为肉汤稀释法检测得到的MIC,定义为肉眼可见澄清培养基的抗菌剂浓度。图中空白位置为未设置药物浓度梯度,橙色填充为Raman检测C-D峰的高于阈值,蓝色填充为Raman检测C-D峰低于阈值,对应的MIC值定为药物浓度从小到大顺序下,Raman检测平均值第一个小于阈值的抗菌剂浓度(Fig.1C红色线框)。由图Fig.1C可知,肉汤稀释法测得的MIC浓度与Raman-D2O标记测得的MIC浓度基本一致,差异结果在左右一个梯度之内,该误差可以接受[2],因此表明基于拉曼光谱法的药敏检测具有可行性。
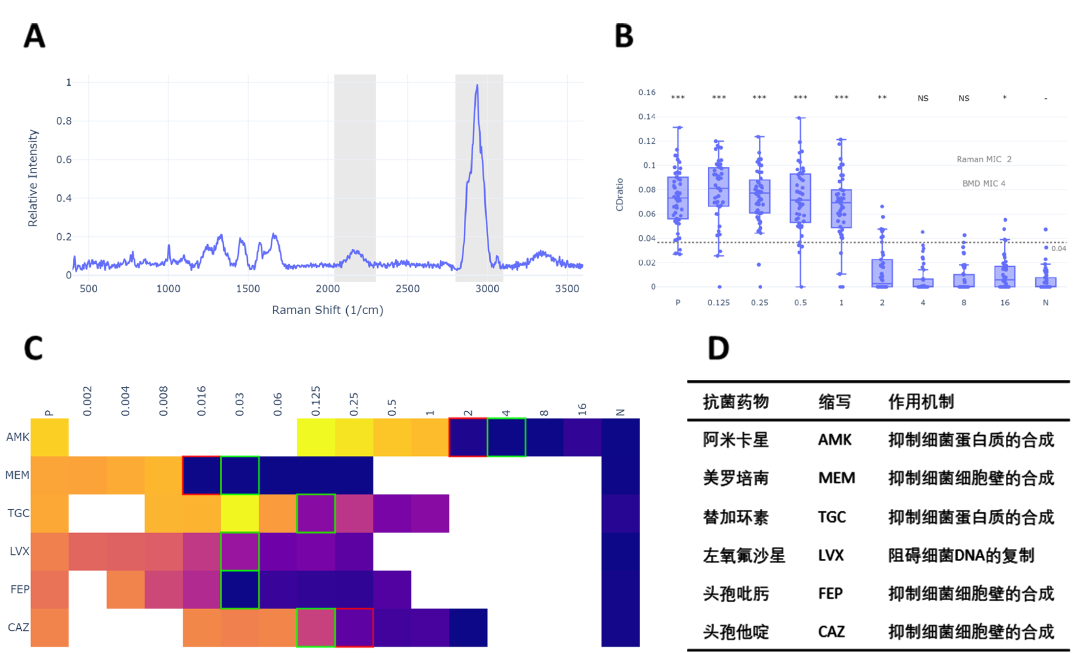
Fig1. 大肠杆菌(E.coli ATCC25922)不同药物药敏结果
A)单个重水标记微生物的拉曼光谱。其中横坐标为拉曼相对波数,纵坐标为相对强度。灰色色块对应的区域依次为C-D、C-H;B)以阿米卡星为例,大肠杆菌在不同浓度下的CD ratio分布。灰色虚线表示阈值,用于MIC判定;C)大肠杆菌对于不同药物Raman-D2O法的MIC判定以及肉汤稀释法的MIC结果比较。其中红色线框表示Raman-MIC结果,绿色线框则表示肉汤稀释法结果;D)药物缩写对应药物名称及作用机制

应用优势

快速高效
病原菌耐药检测时间缩短至6小时以内,使得临床当天用药成为可能。
非破坏性
无需破坏细菌细胞即可进行检测,保留了样品的完整性。
高灵敏度与准确性
拉曼光谱检测结果与普通肉汤稀释法基本一致,具有较高的可靠性和应用价值。

[1] Yi, X. et al. Development of a Fast Raman-Assisted Antibiotic Susceptibility Test (FRAST) for the Antibiotic Resistance Analysis of Clinical Urine and Blood Samples. Anal. Chem. 93, 5098–5106 (2021).
[2] Jorgensen, J. H. & Ferraro, M. J. Antimicrobial susceptibility testing: a review of general principles and contemporary practices. Clin Infect Dis 49, 1749–1755 (2009).





END


往期推荐

2024-03-13

2024-03-15

2024-03-21
2024-03-25
金秋硕果,科研同行丨记长光辰英的南京土壤所之行
S3000的科研之旅:探索生命的每一段意义
显微拉曼光谱技术在颗粒物检测中推本溯源
共聚焦荧光成像与单细胞分选技术联用,揭示肠道菌群的分裂模式及种属分类
相关产品

关注

拨打电话

留言咨询