

了解不同肠道细菌在体内的过程和活性,有助于理解微生物功能及其与宿主的相互作用。尽管人们对肠道菌群复杂功能的认识进展迅速,但直接研究单个细胞的体内微生物活性和过程仍然具有挑战性。
有研究团队提出了一种综合策略,将共聚焦荧光成像技术与单细胞分选和测序相结合,对共聚焦下呈现特异荧光信息的感兴趣细菌进行直接分选和测序,无需体外培养即可同时获得单细菌基因信息和生长分裂表型信息。鉴于这一方法的普适性,其有望成为各类复杂细菌体系研究中一种重要的通用策略。
该策略首先利用能够代谢标记肽聚糖的D型氨基酸荧光探针(FDAA)作为工具,通过使用红绿两种FDAA探针对小鼠进行序贯灌胃,在体标记后获得带有双色荧光的肠道菌群(两种颜色在细菌上的分布可反映其分裂情况)。然后将样品加到带有坐标信息(可进行定位)和特殊涂层(用于激光弹射分选)的芯片上,风干后进行共聚焦成像并记录感兴趣细菌的位置。之后将芯片转移到单细胞分选仪,把相应细菌挑选到无菌管内,破壁后利用MDA进行DNA扩增,用于后续的16S rDNA和全基因组测序分析。作者将这一方法命名为FLCiSS(combining fluorescent probe labeling and confocal imaging with single-cell sorting and sequencing)(图1)。
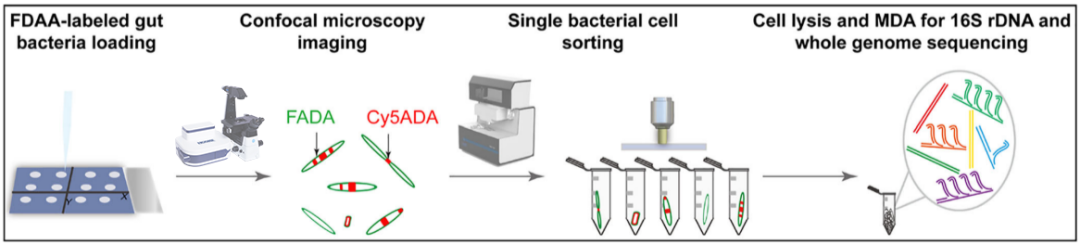
为了确定FLCiSS的实用性,研究者首先在人工细菌群落中测试了该方案,该细菌群落包含一株大肠杆菌(K12)和一株枯草芽孢杆菌(CICC 23659),分别用FADA和Cy5ADA预标记。基于荧光信息,每种细菌分选30个单细胞并进行全基因组扩增和测序。FLCiSS在单细胞水平上鉴定大肠杆菌和枯草芽孢杆菌的成功率分别为73.3%(22/30)和33.3%(10/30),这与最近单细菌测序研究中报道的一些最佳比率相当。综合这些数据,证明了FLCiSS在提供单个细菌的荧光标记数据和分类鉴定方面的可行性。
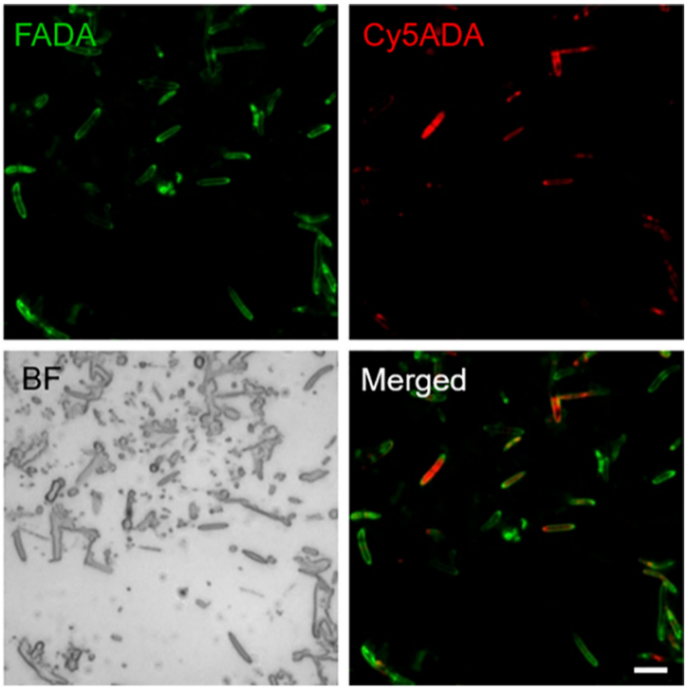
按上述方法共选择了210个细胞进行成像,同种生长模式的细胞进行单细胞分选,并经MDA扩增,成功扩增90个单细胞样品。对其中59份样品进行16S rDNA进行测序,确定各样品的分类群;其中48个样品得到NCBI的鉴定,另外11个样品无法被分类,疑似为过去研究中未培养的细菌类型。
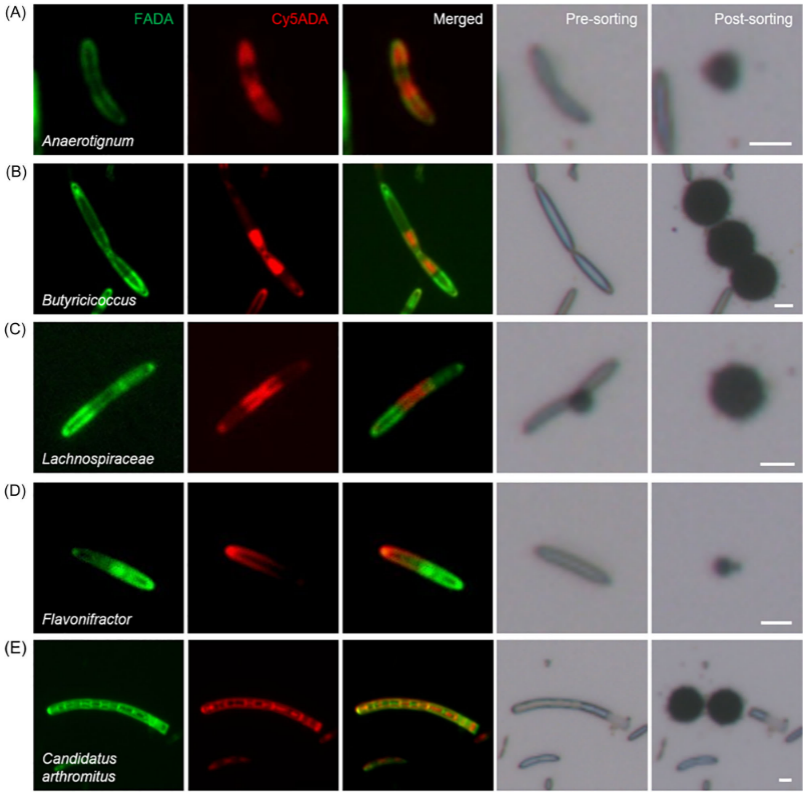
为观察细菌细胞生长状态,多色荧光探针染色是必要的。生物样品的荧光成像,一般要求添加防淬灭剂进行封片处理,并配合高NA的油镜,以达到清晰成像。而在本研究中,由于后续分选实验不能进行封片操作,也无法使用油镜,因此对成像设备的性能要求更高。且多色荧光探针标记肠道微生物的方法在过去仅止步于通过荧光成像确定生长模式。






而基于LIFT技术的PRECI SCS微生物单细胞分选仪实现了肠道微生物的“所见即所得”,使得不同的生长模式与微生物物种及基因信息对应起来,加深了我们对肠道菌群异质性的理解,进一步揭开了肠道微生物的神秘面纱。



往期推荐

2024-08-23
2024-08-23

2023-05-17

2022-04-20

金秋硕果,科研同行丨记长光辰英的南京土壤所之行
S3000的科研之旅:探索生命的每一段意义
显微拉曼光谱技术在颗粒物检测中推本溯源
拉曼光谱丨细菌免培养药敏检测新工具
相关产品

关注

拨打电话

留言咨询