
方案摘要
方案下载| 应用领域 | 其他 |
| 检测样本 | 其他 |
| 检测项目 | |
| 参考标准 | 【文献解读】随机光学重建显微镜助力线粒体动力学的STORM成像(申请试拍) |
【文献解读】随机光学重建显微镜助力线粒体动力学的STORM成像(申请试拍)

随机光学重建显微镜(STORM)可应用于超微线粒体结构的可视化。本文作者开发了一种新的策略来捕获线粒体动态使用压缩传感STORM算法以下的原始数据预处理的噪声校正的主成分分析和K因子图像分解。使用STORM显微镜与邻近二硫醇蛋白质靶向探针,可视化线粒体动力学是可实现的空间和时间分辨率为45 nm和0.8 s,值得注意的是,动态线粒体微管收缩〜 746 nm在1.2 s的监测。标记的缀合物被观察为分布在线粒体外膜上的簇(半径,~90 nm),据我们所知尚未报道。这种策略是有前途的定量分析细胞内的行为低于光学衍射极限。
荧光显微镜被广泛用于研究活细胞中的单个线粒体。然而,使用常规光学显微镜成像线粒体亚结构受到光学衍射极限的限制。由于超分辨率成像的出现,使超细结构可视化已成为可能。
在这项工作中,研究者进行了STORM成像的活细胞中的线粒体动力学,并进行了定量分析的目标下STORM超分辨率显微镜。一种新的荧光标记适合于STORM成像的开发选择性地标记VDPs的外线粒体膜上的简单的共培养与细胞。同时,研究者采用了一个温和的照明激光功率,以获得尽可能多的单帧发射极定位,并减少光漂白和光毒性。STORM成像的时间分辨率可以通过降低激光功率和提高CCD帧频来实现。为了避免背景噪声的干扰,噪声校正的主成分分析(NC-PCA)和K因子图像分解的组合被开发来处理原始数据之前,使用CSSTORM算法重建。使用这种策略,研究者实现了线粒体动力学的STORM成像,包括融合,分裂和线粒体微管化。此外,在STORM成像下,通过层次聚类分析定量评估线粒体外膜上的VDP分布。

Cy 5荧光染料是STORM显微镜的理想的光闪烁候选者,并且1,3,2-二硫砷杂环戊烷是用于VDPs共价结合的有用单元。哌嗪间隔基用作连接基(图1A)。根据先前描述的方案16制备荧光探针1。在将其应用于细胞成像之前,研究了1的光谱性质。首先,乙醇中的探针1在649 nm处显示最大吸收,摩尔消光系数为2。1 ± 0.3 × 105和670 nm处的发射最大值(图1B)。还在水溶液中检测了相同的参数,获得了相似的结果。与罗丹明B相比,在乙醇中获得0.28的荧光量子产率,在水溶液中获得0.18的荧光量子产率。此外,使用自制的dSTORM系统研究了1的单个分子的光闪烁行为。在不存在成像缓冲液和硫醇7,17的情况下,将1的样品直接用激光束(656 nm,0.8kW·cm 2)照射,以显示具有高光子数(约100 nm)的显著的光闪烁荧光。3000个光子/像素)和低的开关占空比(约0.001)。0.0013)。在合适的开关频率下,光闪烁的持续时间持续超过900秒,而“开启”状态的平均光闪烁周期约为88.2ms(图1C-F)。
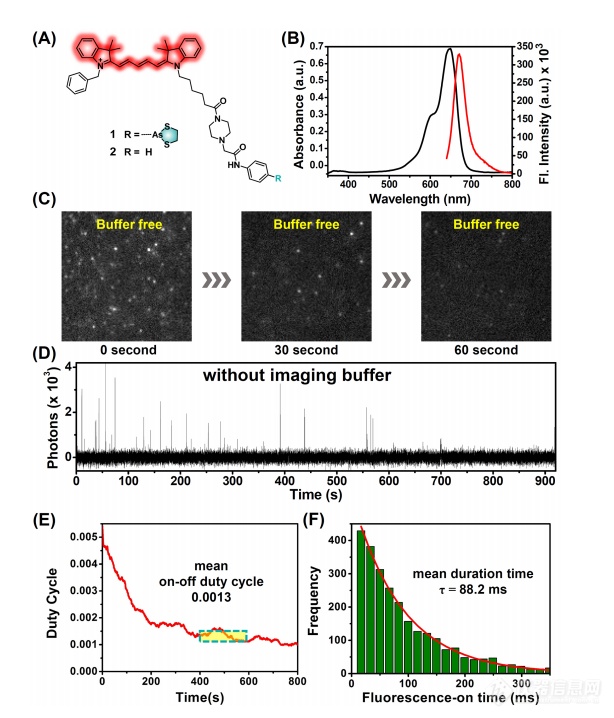
图1. 目标化合物1在没有成像缓冲液的情况下的化学结构和光学性质
为了进一步验证在CSSTORM定位之前通过NC-PCA+ K因子处理的去噪,我们将通过CSSTORM获得的重建结果与单分子拟合(insight 3软件)算法的重建结果进行了比较,如图2所示,使用具有从公开可用的EPFL网站18获得的高密度标记STORM数据的微管蛋白。首先使用NC-PCA算法对数据集进行去噪,然后使用K因子算法进行锐化。通过CSSTORM(图2A(a-c)和单分子拟合(图2A(d))获得了微管蛋白的类似结构,并且CSSTORM仅使用500个相机帧,甚至少至200个帧就表现出更大的结构连续性;然而,在CSSTORM(图2A(例如,i-k,m-o))和insight 3算法(图2A(h,l,p))之间的比较中,当使用100帧时观察到差的连续性。图2A(a-d)中的放大视图示出了在使用NC-PCA+ K因子算法去噪时明显锐化的结构(图2A(g)),其保持了与insight 3结果的最大结构一致性(图2A(h))。在NC-PCA+ K因子处理后,七个微管是可区分的,并且在原始数据的CSSTORM处理中或仅对于K因子处理,在相邻微管之间不可避免地出现模糊的噪声峰,如图2B(a-b)中的虚线圆所示。傅立叶环相关(FRC)是一种定量成像分辨率测量工具,已用于进一步评估图像分辨率的改善。
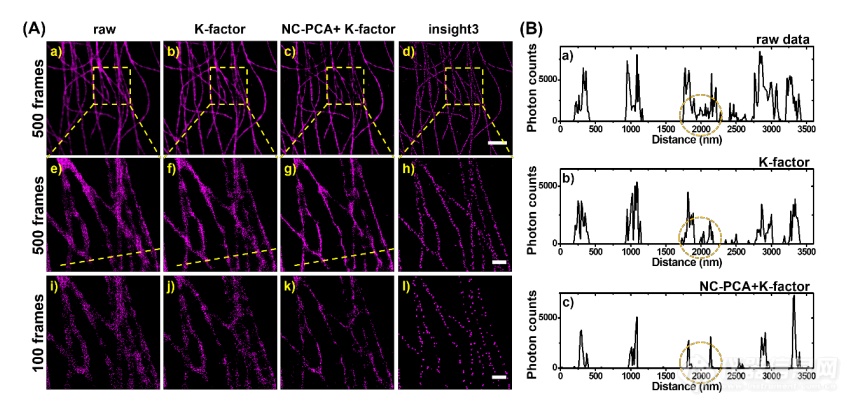
图2. 使用具有高密度标记的微管蛋白的实验数据集(来自EPFL)验证NC-PCA去噪算法
在用PBS、PBS-乙醇或乙醇溶剂洗涤后,探针不能从线粒体中除去(图S2 B、S2 C、S2 D、S5和S6)。此外,探针在我们的实验条件下未显示细胞毒性(图S7),这有利于活细胞超分辨率成像(图3)。
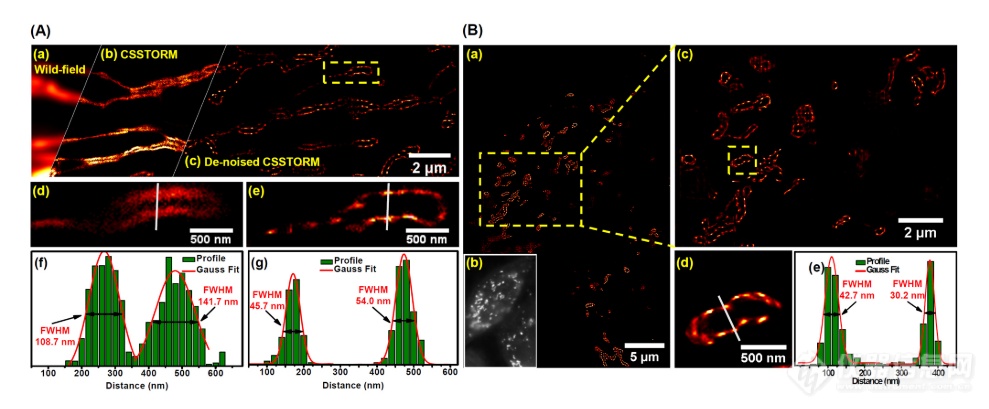
图3. 超分辨率成像探针1的线粒体膜贴上住海拉细胞固定海拉细胞(A)和(B)
为了确定1在活细胞线粒体中的确切位置,进行STORM超分辨率成像以确定由1标记的线粒体的超细结构。将探针1(1 μM)与HeLa细胞一起孵育1小时,无需进一步处理,重要的是,该程序比使用Alexa647的程序更简单。随后,在成像之前用戊二醛固定细胞样品或通过STORM系统用于活细胞成像。如图3A(a)所示,与不能提供线粒体的精细结构的宽视场图像不同,超分辨率图像显示了详细结构,其在活HeLa细胞(图3A(c))或固定细胞(图3B)中使用200帧通过CSSTORM(图3A(b))和去噪CSSTORM重建。从图3A(c)中的虚线方块所示的感兴趣区域的放大图像,去噪的CSSTORM分辨率明显高于CSSTORM的分辨率(图3A(d)),并且在图3A(e)中清楚地观察到线粒体膜上的离散颗粒分布,表明探针1选择性地标记线粒体膜上的VDP。通过高斯拟合计算CSSTORM和去噪CSSTORM的成像分辨率,示出108.7和45的半高全宽(FWHM)。如图3A(f,g)中所示。使用固定的HeLa细胞,STORM进一步支持1与线粒体膜上的VDPs的共价结合。当HeLa细胞与1孵育,用戊二醛固定并用PBS洗涤时,通过去噪CSSTORM算法获得线粒体的类似超分辨率图像(图3B(a,c,d)),并且高成像分辨率(图3B(e)中的30.2nm)使得能够研究线粒体外膜上的VDP分布以及它们的动力学。
STORM进一步应用于评估动态线粒体变化,包括线粒体融合、分裂和微管化。通过CSSTORM或去噪CSSTORM算法使用200个相机帧以20帧的步长进行重建以获得0.8s的时间分辨率来获得演示动态的视频。视频结果清楚地显示,与宽视场图像(图4A)和CSSTORM图像(图4 B)相比,去噪CSSTORM图像的分辨率明显更好。在通过NC-PCA+ K因子方法预处理后,去噪CSSTORM分析显示出明显的噪声抑制,并且实现了线粒体膜上的VDP的超细成像(图4C、)。此外,可以观察到线粒体的典型动力学以量化线粒体融合、分裂和成管的速度,这可能反映了生物活动中的线粒体状态20、21。捕获单个线粒体微管化和微管拉伸(图4C中的虚线正方形),并且不同的时间点显示在图4D中(1-6)。在管收缩期间的距离为~746 nm,并且在1.2s内完成(图4 E)。如通过高斯拟合计算的,中空管直径(图4F中放大的虚线圆)为51.8nm,并且膜宽度的FWHM值为46.9nm和43.5nm(图4G),与先前报道的结果22相当。
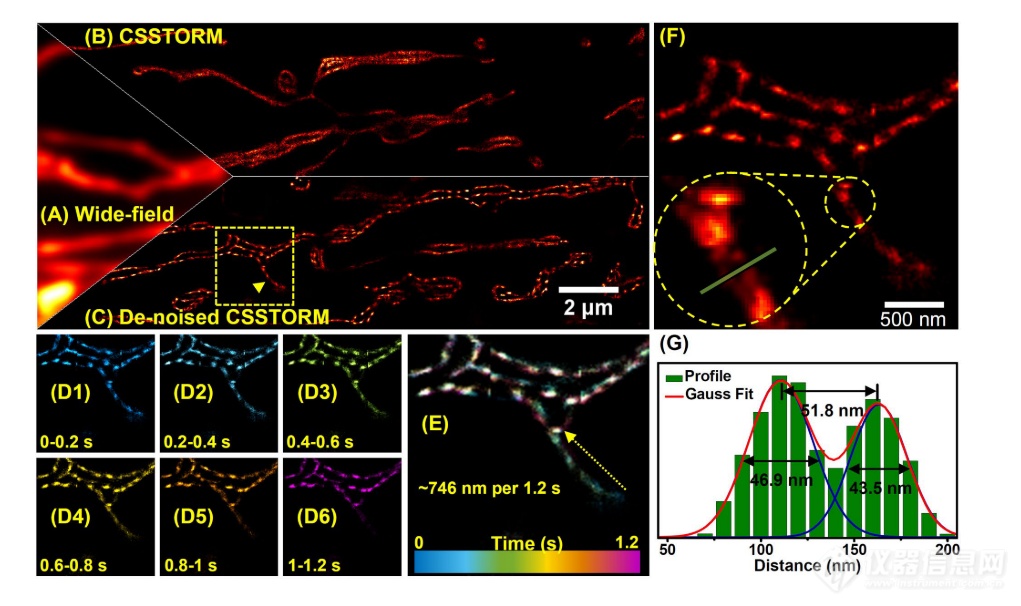
图4. 基于超分辨率成像的线粒体微管化分析
研究VDPs在线粒体膜上的分布可以提供对生物学功能的深入了解。我们使用开源软件Localization Microscopy Analyzer(LAMA)23基于基于密度的分层聚类算法来分析VDP的形态簇,即一个基于密度的算法发现集群在大型空间数据库中的噪声(DBSCAN)和排序点,以确定聚类结构(OPTICS)。考虑到压缩感测算法的像素化而不直接返回分子坐标列表,通过识别非零网格点的簇,首先将CSSTORM结果转换为分子列表作为LAMA的输入。选择感兴趣的区域(128×128像素的超分辨率网格图像)用于蛋白质聚类分析(图5A)。观察半径设定为19 nm,在DBSCAN中最小簇尺寸设定为6,并且在OPTICS 24中噪声水平设定为13.1%。总共,分别通过DBSCAN和OPTICS检测到32个和36个簇,并且在图5(B,E)中示出为簇群的2D分布。使用DBSCAN或OPTICS的结果进行基于DBSCAN的层次聚类分析,以通过多边形形成来提取单个簇的形态信息。具有16个假色的形态聚类分析结果总结在图5(C,F)中。最后,一个集群人口分布与集群大小约。如图5(D、G)所示,获得了90 nm,表明这是分析活细胞中蛋白分布的一种有前景的策略。
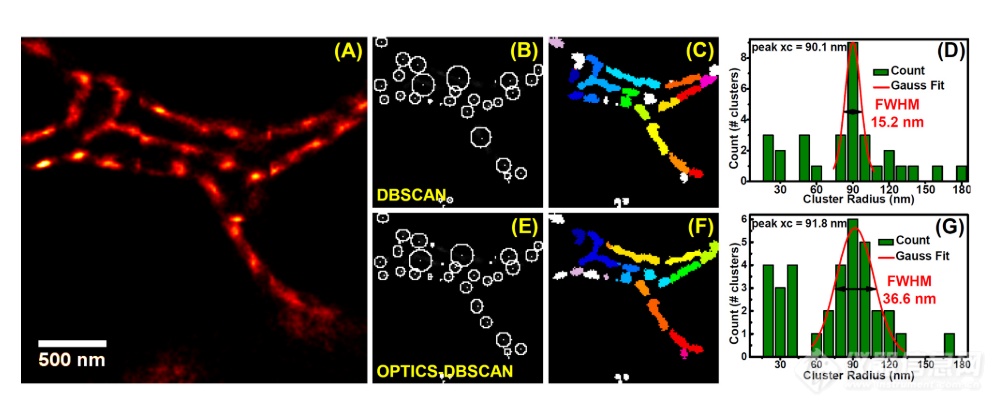
图5. 使用DBSCAN(B,C,D)和OPTICS(E,F,G)通过蛋白质聚类分析确定线粒体膜VDPs的分布

在该方法中,应用新的STORM探针共价结合线粒体外膜中的VDPs,这实现了STORM超分辨率成像,而不需要成像缓冲液和硫醇。使用由NC-PCA+ K因子预处理组成的噪声校正方法通过CSSTORM成像获得线粒体动力学分析。去噪CSSTORM能够实现线粒体的超细结构成像,在固定细胞中的空间分辨率高达30.2 nm,在活细胞中为45.7,时间分辨率为0.8 s。利用线粒体膜上1-VDP复合物的动态变化来显示线粒体动力学,包括融合、分裂和微管化,特别是ca.746 nm(1.2 s)。将线粒体外膜上的VDPs分布进一步分析为蛋白质聚集(约100%)。90 nm),以更深入地了解其生物学功能。新开发的策略将是有用的线粒体功能的进一步研究。
在本研究中,研究者主要借助STORM超助力线粒体动力学的STORM成像,目前在国内,随机光学重建显微镜STORM已成功实现商用,有需要STORM成像技术进行实验研究的专家老师们,请文末填写问卷,即可预约获得 iSTORM 超高分辨率显微成像系统试拍服务~

力显智能现已发布的超高分辨率显微成像系统 iSTORM,成功实现了光学显微镜对衍射极限的突破,使得在20纳米的分辨率尺度上从事生物大分子的单分子定位与计数、亚细胞及大分子复合物结构解析、生物大分子生物动力学等的研究成为现实,从而给生命科学、医学等领域带来重大突破。


【应用实例】使用随机光学重建显微镜STORM对皮质下白质进行超分辨率成像
【应用实例】超分辨率显微镜在观察革兰氏阳性菌的细胞外囊泡生物中的应用
用STORM成像揭示细胞间隧道纳米管(TNTs)的结构和组织
相关产品

关注

拨打电话

留言咨询