傅若农第二十一讲:碳用于固相萃取的演变
导读:傅若农教授是我国老一辈色谱研究专家,见证了我国气相色谱研究的发展,为我国培养了众多色谱研究人才。此次仪器信息网特邀傅若农教授亲述气相色谱技术发展历史及趋势,以飨读者。
往期讲座内容见:傅若农老师讲气相色谱技术发展
碳是有机世界的“主角”,在地球上按重量计算,占地壳中各元素总重量的0.4%,按原子总数计算不超过0.15%。而元素碳是一种十分神奇的物质,像碳纤维是比钢轻而抗拉强度高于钢7-9倍的材料。尤其是近20年纳米级大小的碳(富勒烯,碳纳米管,石墨烯等)人们给以前所未有的重视。
在利用各种吸附剂进行混合物分离发展的早期,人们就利用各种形态的碳做吸附剂用于分离各种混合物,现在人们又把目光投向富勒烯,碳纳米管,石墨烯等纳米级材料做新型分离材料用作固相萃取的吸附剂。
1. 活性炭作固相萃取吸附剂
活性碳是最早使用的固相萃取吸附剂,开始主要使用工业级别的活性碳,但是,使用了一段时间以后,吸附性能不能令人满意,就把它改性,以适应萃取分离的要求。在制备活性碳当中,要得到所需要的性能,碳化和活化过程的参数中最重要的是原料的选择和预处理。活性碳的基本性质取决于所用原料,使用的原料有自然的木头、泥炭、煤、果核、坚果的外壳以及人工合成物质——主要是聚合物。在没有空气和化学品条件下的碳化过程中,首先是大多数非碳元素(氢、氧和微量硫和氮)由于裂解的破坏而分解挥发了,这样元素碳就留下来,形成结晶化的石墨,其结晶以无规则方式相互排列,而碳则无规律地存在于自由空间里,这一空间是由于滞留在这里的物质被沉积和分解而形成的。进行碳化的目的是使之形成适当的空隙并形成碳的排列结构,碳化过程使碳吸附剂具有较低的吸附容量,使其比表面只有几个 m2/g,使之没有过高的吸附性。为了得到高空隙度和一定的比表面积,碳化还要进行活化过程。从天然原料制得的活性碳要比从合成物制得的活性碳具有较高的灰分,从合成化合物制得的活性碳几乎没有灰分,并且具有很好的机械性能,不易压碎和被磨损。由天然原料制得的活性碳其吸附性能受到它表面化学结构的影响,而其表面性质又决定于与其键合在一起各种杂原子(如氧、氮、氢、硫、氯等)的种类,活性碳是没有特殊选择性,或选择性很小的吸附剂。制备良好的活性碳为多孔结构,主要是各种直径的微孔和介孔,其比表面可达1000 m2/g到2m2/g,或者更高一些,使其具有高的吸附容量。活性碳表面具有很高的化学和几何不均一性,特别是工业用活性碳尤为严重。
固相萃取(SPE)使用活性炭始于上世纪 50 年代初,Braus 等人使用活性碳做吸附剂,在铁管中装1200-1500 g 碳纤维,用以富集水中的污染物,之后用索氏萃取器提取被吸附的有机物,包括水中的有机氯农药。(Anal Chem,1951,23:1160)。萃取管长91.44 cm,直径在10.16 cm,装填1200-1500 g 颗粒状活性碳,通过 5000 gal - 7500 gal 地表水吸附有机氯氯农药。
由于活性碳的缺点妨碍其使用,即吸附性不均一,重复性不好,有过高的吸附性,有不可逆活化点,回收率低。所以从上世纪 60 年代末到80 年代初,一直在寻找更为合适的适应性更强的 SPE 填料。
2. 碳分子筛作固相萃取吸附剂
在上世纪 70 到 80 年代,在研究聚合物吸附剂和键合有机物硅胶的同时,再次使用了性能改进的碳吸附剂——碳分子筛。这是由于当时的碳吸附剂结构改进、材质均一、性能稳定,同时它对极性化合物的吸附有好的选择性。碳分子筛的性能与 XAD-4 大孔树脂(以苯乙烯和丙烯酸酯为单体、乙烯苯为交联剂进行聚合)相同。
1968年 Kaiser 制备出一种碳吸附剂叫“碳分子筛”,国外的商品名是 Carbosieve B,它是用偏聚氯乙烯小球进行热裂解,得到固体多孔状的碳,其比表面为1000 m2/g,平均孔径为 1.2 nm 。这种吸附剂用于气-固色谱的固定相,我国称之为碳多孔小球(TDX),自然可以用作固相萃取的吸附剂。早年我国上海高桥化工厂、中科院化学所和天津试剂二厂相继研制成功这类碳分子筛,商品名叫做:碳多孔小球(Tan Duokong Xiaoqiu,TDX), 具体的牌号有 TDX-01;TDX-02。它们的堆积密度为 0.6 g/mL,比表面为 800 m2/g。碳多孔小球的特点是:非极性很强,表面活化点少,疏水性强,耐腐蚀、耐辐射,寿命长。表1列出国外厂家的碳分子筛的性能。
表 1 商品碳分子筛的性能
吸附剂商品名 | 厂家 | 比表面/(m2/g) | 孔径/nm | 堆积密度/(g/mL) |
Carbosieve B | 1000 | 1-1.2 | 0.226 | |
Carbosieve S | Supelco | 560 | 1-1.2 | 0.5-0.7 |
Carbosieve S-II* | Supelco | 548 | 0.5-0.7 | 0.55-0.60 |
Carbosieve G* | Supelco | 204 | 0.5-0.7 | 0.25-0.28 |
Spherocarb | Foxboro | 1200 | 1.5 | 0.5+0.05 |
Carbosphere | Chrompack | 1000 | 1.3 |
3 近年用碳纳米材料作固相萃取吸附剂
自从1991年日本学者饭岛澄男(Sumo Iijima)发现了碳纳米管(CNTs)之后,改变了人们过去对碳的三种形态(金刚石、石墨和无定形碳)的认识,对碳纳米管不断进行研究,并竞相把这种新奇的材料用在各个领域。在2004年又出现了另外一种有趣的碳物质——石墨烯,G),CNTs和G是碳的两种同素异形体,它们具有sp2杂化网络,但是结构不同,CNTs具有管状纳米结构,由石墨烯片卷成管状,形成准一维结构,而G是打开纳米管形成的平面二维薄片。CNTs可分为单壁碳纳米管(SWCNTs)和多壁碳纳米管(MWCNTs),石墨碳家族的各种形态如图1所示。
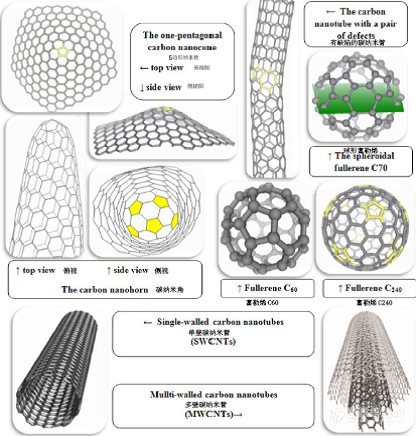
图 1 碳家族的各种形态
(TrAC,2016, 77:23–43)
(1) 富勒烯及其衍生物作固相萃取吸附剂
自从1990年Huffman 和 Kratschmer发表了能大量制备富勒烯(C60)之后,对这类物质进行大量研究,对这类化合物的制备和性能有不少文章和综述发表,日本的 Jinno Kiyokatsu研究组对富勒烯进行了大量研究(Anal. Chem., 1995, 67:2556),把富勒烯键合到硅胶上用作HPLC的固定相,分离多环芳烃。Gallego等揭示了C60作为吸附剂在分离富集金属离子的潜力(Anal Chem,1994, 66:4074),它对金属离子的分离富集能力优于常规萃取剂——键合烷基硅胶和活性炭。例如超痕量镉在C60富勒烯微柱上进行分离, 形成中性配合物,用200mL对甲基异丁基酮洗脱吸附的镉,用原子吸收光谱进行测定。用双螯合试剂,即吡咯烷铵(APDC)和8-羟基喹啉,在一个流路中进行检测。APDC和C60富勒烯对镉进行选择性吸附,与含有的铜、铅、锌、铁中分离出来。与其他方法对比, C60和APDC的方法得到更为准确的结果(J Anal Atom Spectrom, 1997, 12: 453–457)。
2000年M Valcárcel等使用一个简单的流动注射系统,在C60富勒烯吸附柱上在线富集金属二硫代氨基甲酸盐(杀菌剂),无需使用常规方法的酸水解,以便释放CS2,也不用衍生化,它可以直接保留在吸附柱上,随后用稀硝酸洗脱。将洗脱的馏分直接送入火焰原子吸收光谱仪进行测定(Analyst,2000, 125:1495–1499)。
2004年M Gallego等用富勒烯萃取柱选择性吸附汞的二乙基二硫代氨基甲酸配合物,分析水中的无机和有机汞,免除许多金属离子的干扰(J Chromatogr A, 2004, 1055 : 185–190)。
2009年M Gallegoa 等利用C60富勒烯萃取柱区分非芳香族(脂族和环状)和芳香族亚硝胺,用C60和LiChrolut EN组成一组串联萃取柱,25ml样品通过C60柱只有芳香族亚硝胺保留,然后通过LiChrolut EN柱非芳香亚硝胺馏分被保留。用150μL乙酸乙酯–乙腈溶液(9:1)洗脱非芳香亚硝胺,进样1μL萃取物到GC-MS中进行测定。通过比较C60和C70富勒烯和碳纳米管的研究,显示C60富勒烯是选择性地保留芳香族馏分最佳。(J Chromatogr A,2009,1216 :1200–1205)。 表 2 是勒烯及其衍生物作固相萃取吸附剂的用例。
表 2 富勒烯及其衍生物作固相萃取吸附剂的用例
1 | 富勒烯C60 | Cd | 水,牡蛎组织,猪肾牛肝 | AAS | -- | J Anal At Spectrom,1997,12 :453–457 |
2 | 富勒烯C60 | 汞(II)、甲基汞(I) | 海水,废水和河水 | GC-MS | 80–105 | J Chromatogr A,2004,1055:185–190 |
3 | 富勒烯C60 | 有机金属化合物 | 水溶液 | GC-MS | -- | J Chromatogr A,2000, 869:101–110 |
4 | 富勒烯C60 | 金属二硫代氨基甲酸盐 | 粮 | FAAS | 92–98 | Analyst,2000,125:1495–1499 |
5 | 富勒烯C60 | BTEX | 海水,废水,地表水,雨水,湖水,饮用水和河水 | GC-MS | 94–104 | J Sep Sci,2006,29:33–40 |
6 | 富勒烯C60,C70 | 芳烃和非芳烃,亚硝化单胞菌 | 游泳池水,废水,饮用水和河水 | GC-MS | 95–102 | |
7 | 富勒烯C60-键合硅胶 | 阿马多瑞多肽 | 人血清 | MALDI-TOF MS | -- | Anal Biochem,2009,393: |
(2)碳纳米管及其衍生物作固相萃取吸附剂
碳纳米管(CNTs)是由管状碳同素异形体,由一个单一的石墨薄片卷形成的结构,即单壁碳纳米管(SWCNT)或几个同心排列的碳纳米管结构,即多壁碳纳米管。单壁碳纳米管的直径可达3nm,多壁碳纳米管最多至100 nm。由于CNTs具有表面积大、活化点多、π-π键作用力强等特殊性能,适合于在固相萃取中应用,而且它的纳米级多孔性能有利于减小传质阻力,有利于平衡。碳纳米管具吸附性?,特别是多壁碳纳米管有很强的吸附性,比如它对TCDD(2,3,7,8-四氯代二苯并二恶英)的吸附性比一般活性碳吸附剂高1034倍(J Am Chem Soc,2001,123:2058.)。开始CNTs用于从水中分离双酚,壬基酚和辛基酚(Anal Bioanal Chem,2003,75:2517),回收率可达102.8%。其他多壁碳纳米管的SPE应用于包括极性和离子性化合物的目标物,如磺脲类除草剂,头孢菌素,抗生素、磺胺类和酚类化合物,苯氧羧酸类除草剂。(Anal Sci,2007,23 :189;Anal Chim Acta,2007,594: 81;Microchim Acta,2007,159:293)。
碳纳米管的一个有趣的特点是它们的表面可以进行化学改性,得到功能化具有独特性能的吸附剂。例如,有人在原单壁碳纳米管进行氧化,以便引入羧酸基团,可以萃取非甾体类抗炎药如布洛芬;从尿液萃取托美汀和吲哚美辛(J Chromatogr A,2007,1159 :203)。碳纳米管进行表面修饰使其具有高选择性,如吉首大学的张华斌等在多壁碳纳米管表面通过酰胺化反应接枝双键,以L-组氨酸为模板,甲基丙烯酸为功能单体,乙二醇二甲基丙烯酸酯交联剂,偶氮二异丁腈为引发剂,利用表面印迹技术,在多壁碳纳米管表面制备印迹聚合物(MWNTs-MIPs)。可选择性吸附红霉素从鸡组织制剂中提取红霉素回收率达95.8%。(Anal Bioanal Chem,2011,401:2855;J Chromatogr B,2011,879:1617)。图 2 是 多壁碳纳米管(a 和c)和多壁碳纳米管的分子印迹聚合物(MWNTs-MIPs)(b和d)的扫描电镜(a 和b)和透射电镜(c和d)图。
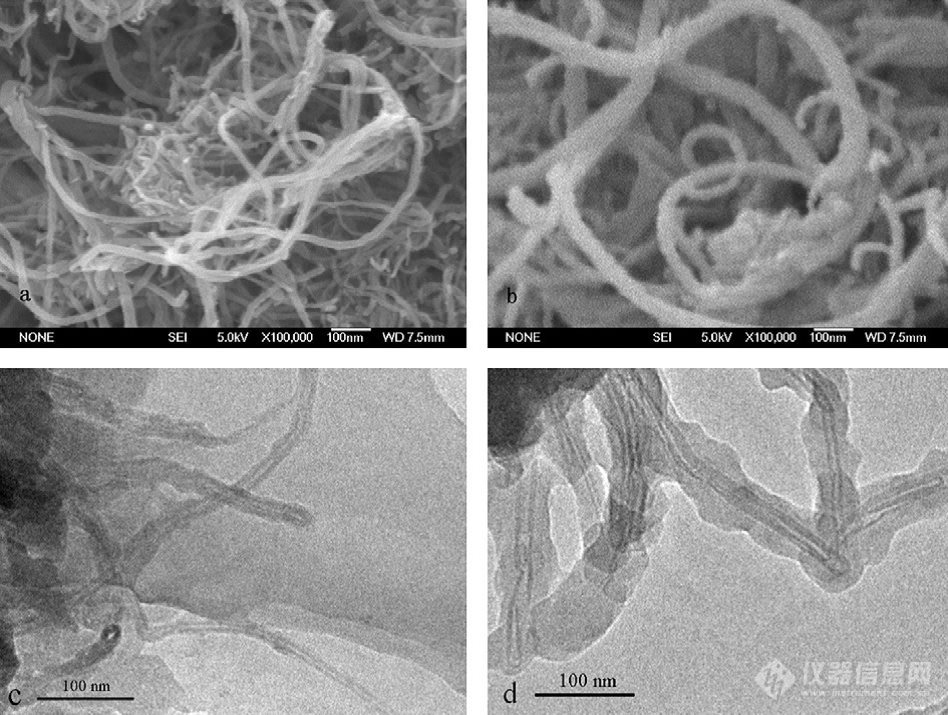
图 2 多壁碳纳米管和和多壁碳纳米管的分子印迹聚合物的扫描电镜
另外他们(J Chromatogr B,2011,879:1617)在Fe3O4磁性纳米粒子的表面涂渍了用羧基改性的多壁碳纳米管,并在表面接枝了牛血清白蛋白(BSA),使其具有印迹吸附功能(MIP)选择性吸附剂。
碳纳米管通过表面化学修饰,使之成为有选择性的吸附剂,成为近年研究的热点。表面修饰使碳纳米管物理和化学性能改性,这不仅扩大了其应用范围还可以提高其溶解性,这是由于提高了它和溶剂的色散作用力,可与大多数溶剂作用。表面化学修饰功能化过程通常包括酸化、氧化处理,提供了可作用的功能团,也减少了在碳纳米管的合成过程中造成的杂质。可以使用简单的或复杂的方法获得共价键合或非共价方式修饰碳纳米管。直接键合可通过碳纳米管壁形成的羧基可以直接与想要的功能团进行结合。另一方面,可通过范德华力、静电力、堆积作用、氢键和疏水相互作用形成非共价聚集体。两个或多个相互作用的结合,可提高了系统稳定性和选择性。表 3 是使用碳纳米管作样品前处理的应用实例。
表 3 使用碳纳米管进行样品处理的应用
分析物 | 样品基体 | 分析方法 | 碳纳米管特点 | 回收率/% | 文献 | |
1 | 邻苯二甲酸酯 | 水样 | GC–MS/MS | MWCNTs,o.d.:<8 nm,长:0.5–2μm,比表面:>500 m2/g | 86.6–100.2 | J Chromatogr A, 2014, 1357:53–67 |
2 | 饮料,自来水,香水 | GC–MS | MWCNTs,o.d.:10–20 nm,长:5–15μm | 64.6–125.6 | ||
3 | 邻苯二甲酸单酯 | 人尿 | GC–MS | MWCNTs,o.d.:30–60 nm,长:3–5μm, | 92.6–98.8 | 同上 |
4 | 直链烷基苯 | 湖水,河水,污水 | HPLC–UV | MWCNTs,o.d.:30–60 nm,长:~20μm,比表面:~60 m2/g | 87.3–106.3 | 同上 |
5 | 对羟基苯甲酸酯 | 饮料 | HPLC–DAD | -- | 同上 | |
6 | 神经剂及其标记蒸馏水 | 自来水,浑浊水 | GC–FPD | MWCNTs, o.d.: 7–15 nm,, | 55.5–96.3 | 同上 |
7 | (氟)喹诺酮类 | 人血浆 | UPLC–UV | MWCNTs, o.d.: 110–170 nm, 长:5–9 μm | 70.4–100.2 | 同上 |
8 | 氟喹诺酮类 | 矿泉水,蜂蜜 | CLC | MWCNTs, o.d.: <8 nm,长:0.5–2μm | 84.0–112 | 同上 |
9 | 苯并[a]芘 | 有机溶剂、水溶液 | MALDI–TOF–MS | MWCNTs | -- | 同上 |
10 | PAHs | 食用油 | GC–MS | WCNTs, o.d.: 10–20 nm, 长:5–15μm | 87.8–122.3 | 同上 |
11 | PAHs | 活性炭/烧烤肉 | GC–MS | MWCNTs, o.d.: 30–60 nm, 长:5–3μm | 81.3–96.7 | 同上 |
12 | 雌激素 | 自来水,矿泉水, | EC–UV | MWCNTs, o.d.: <8 nm, :0.5–2μm | 89.5–99.8 | 同上 |
13 | 雌激素 | 牛奶 | HPLC–FLD | 93.7–107.2 | 同上 | |
14 | 核酸相关蛋白质 | 人细胞裂解物,肝癌BEL-7402细胞 | Nano-LC–MS/MS | MWCNTs, o.d.: 20–30 nm | -- | 同上 |
15 | 核酸相关蛋白质 | 人肝癌BEL-7402细胞 | Nano-LC–MS/MS | MWCNTs, o.d.: 20–30 nm | -- | 同上 |
16 | 双酚A,双酚F和缩水甘油 | 自来水,河水, | GC–MS/MS | MWCNTs, i.d.: 60–100 nm | 88.5–115.1 | 同上 |
17 | Se(IV) | 自来水,湖水 | HG–AFS | MWCNTs 平均20 nm | 96.3–102.3 | 同上 |
18 | Pb(II) | 废水、河水,大米,红茶,绿茶,洋葱,马铃薯 | FAAS | MWCNTs, o.d.: 8–15 nm,比表面:233 m2/g | 97–104.5 | 同上 |
19 | 六种邻苯二甲酸酯 | 茶油 | GC-MS | MWCNTs, o.d.: 1–2 nm, 长:0.5–2μm 比表面:380 m2/g | 86. 4-111. 7 | 色谱,2014,32(7):735-740 |
20 | 114种农药残留 | 烟草 | LC-MS/MS | MWNCTs1-5:外径:<8->50 nm,长度: 10-30μm,比表面:40-500m2/g | 93-114 | 烟草科技,2015,48(5):47-55 |
21 | 金刚烷胺 | 鸡肉 | LC-MS/MS | MWNCTs1-5:外径:<8->50nm长度: 10-30μm,比表面:40-500m2/g | 97.8-103.6 | 肉类研究,2014,28(4):14-18 |
22 | 16种有机磷农药 | 水样 | GC-FPD | MWNCTs1-5:直径:20-40,nm长度:5-15μm,比表面:40-500m2/g | >75 | 分柝化学,2009,37(10):1479-1483 |
23 | 有机氯和除虫菊农药 | 蔬菜 | GC-ECD | 多壁碳纳米管(L-MWNT-2040),20-40,nm长度:5-15μm, | >70 | 色谱,2011,29(5):443-449 |
24 | 溶菌酶 | 蛋清 | SDS-PAGE凝胶电泳 | MWNCTs :外径:40-60nm, | 96.4 | 高等学校化学学报,2—8,29(5): 902-905 |
25 | 有机磷农药 | 水样 | GC-PFPD | -- | 70 | 厦门大学学报(自然科学版),2004,43(4):531-535 |
26 | 有机磷农药 | 大蒜 | 方波伏安法 | -- | 97.0-104.0 | 分析试验室,2007,26(增刊)(10):216-217 |
27 | 酰胺类除草剂 | 饮用水 | GC-MS/MS | -- | 82-93.5 | 分析试验室,2009,28(增刊)(5):82-84 |
28 | 唑4种磺胺类药物 | 环境水 | (HPLC—PDA | 己基-3.甲基咪唑六氟磷酸([C。MIM][PR])离子液体自聚集于磁性多壁碳纳米管上 | 0.6-99.99 | 分析化学,2015,43(5):669-674 |
29 | 多环芳烃 | 河水 | GC-MS | -- | 60.4-89.3 | 分析化学,2009,37,(增刊):D025 |
30 | 甲硝唑 | 食品 | LC-UV | -- | 68-112 | 分析测试学报。2010,29(8):807-8ll |
(3) 石墨烯作固相萃取吸附剂
石墨烯是由碳六元环组成的两维(2D)周期蜂窝状点阵结构, 它可以翘曲成零维(0D)的富勒烯(fullerene),卷成一维(1D)的碳纳米管(carbon nano-tube, CNT)或者堆垛成三维(3D)的石墨(graphite), 因此石墨烯是构成其他石墨材料的基本单元。石墨烯的基本结构单元为有机材料中最稳定的苯六元环, 是目前最理想的二维纳米材料.。理想的石墨烯结构是平面六边形点阵,可以看作是一层被剥离的石墨分子,每个碳原子均为sp2杂化,并贡献剩余一个p轨道上的电子形成大π键,π电子可以自由移动,赋予石墨烯良好的导电性。二维石墨烯结构可以看是形成所有sp2杂化碳质材料的基本组成单元。石墨烯既是最薄的材料,也是最强韧的材料,断裂强度比最好的钢材还要高200倍。同时它又有很好的弹性,拉伸幅度能达到自身尺寸的20%。它是目前自然界最薄、强度最高的材料。自然,人们不会忘记把它用作吸附剂用于固相萃取。因为它有高比表面积,2630 m2/g,高的吸附能力,良好的化学和热稳定性,高机械强度,价格便宜,网上戏称是白菜价。基于它的离域π-电子体系,它可以和带有苯环的化合物形成π-π堆积相互作用,因而对这类化合物有很强的吸附作用。氧化石墨烯(GO),石墨烯的含氧基团,如羧基和羟基,可以化合物以共价键,静电或氢键结合。
基于石墨烯的吸附剂已用于含苯环化合物的预富集。2011年江桂斌院士的研究组利用石墨烯作吸附剂制成固相萃取柱,萃取水中的8种氯代酚,比较了几种吸附剂对8种氯代酚的回收率,见图 3(J Chromatogr A,2011,1218:197-204).
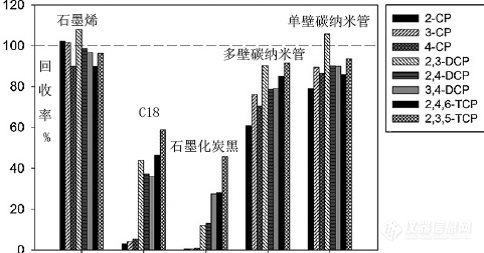
新加坡国立大学的H K Lee等使用磺化石墨烯片作为吸附剂的固相微萃取,测定水中8种多环芳烃(J Chromatogr A,2012,1233:16-21),萃取效率远高于C8和C18萃取剂,见图4.
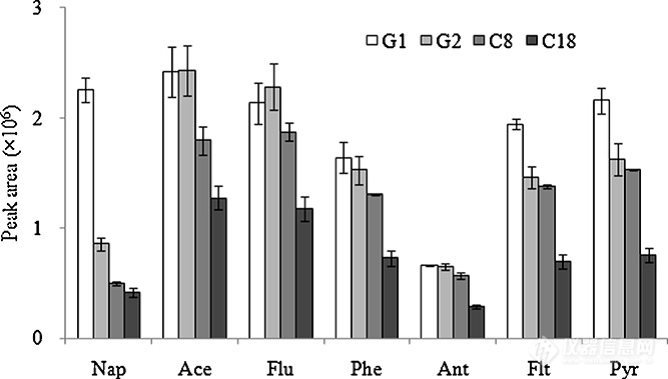
图 4 磺化石墨烯与C8和C18吸附效率的比较
G1,G2—磺化石墨烯
Nap—萘;Ace—苊;Flu—芴;Phe—菲;Ant—蒽;Flt—荧蒽;Pyr—芘
表 4 是石墨烯用作固相萃取吸附剂的用例
表4 石墨烯用作固相萃取吸附剂的用例
萃取剂 | 被分析物 | 样品基质 | 检测 | 回收率/% | 文献 | |
1 | 石墨烯, | Pb | 环境水和蔬菜 | 火焰原子吸收光谱(FAAS) | 95.3–100.4 | Anal Chim Acta,2012,716:112–118 |
2 | 石墨烯 | 谷胱甘肽 | 人血浆 | 荧光分光光度计 | 92-108 | Spectrochim Acta,2011,79:860–186 |
3 | 氧化石墨烯 | 氯苯氧酸除草剂 | 河水与海水 | CE | 93.3- 102.4 | J Chromatogr A,2013,1300:227–235 |
4 | RGO-silica(氧化石墨烯衍生物-硅胶) | 氟喹诺酮 | 自来水和河水 | LC-FLR | 72–118 | J Chromatogr A,2015,1379:9–15 |
5 | 磺化石墨烯 | 多环芳烃 | 河水 | GC-MS | 81.6 -113.5 | J Chromatogr A,2012,1233:16–21 |
3.碳用作萃取吸附剂的综述文献
表5 是碳纳米材料用作吸附剂近几年发表的综述文献,读者可以了解到更多的有关碳纳米材料在固相萃取中的应用情况。
表5 碳纳米材料用作吸附剂近几年发表的综述文献
碳纳米管在分析化学中的应用(引用273篇文献) | SPE,SPME,膜,吸附棒 | J.Chromatogr. A,2014,1357:110–146 | |
2 | 碳基吸附剂—碳纳米管(引用194篇文献) | SPE,SPME,吸附棒 | J ChromatogrA,2014, 1357: 53–67 |
3 | 石墨烯基材料—制备及其在分析化学中的吸附应用(引用203篇文献) | SPE,SPME,色谱固定相 | J Chromatogr A,2014, 1362 :1–15 |
4 | 石墨烯作吸附剂在分析化学中的应用 | SPE,SPME中的应用 | TrAC,2013,51:33-43 |
5 | 碳纳米管在分离科学中的应用-综述(引用241篇文献) | SPE,SPME LC,GC,CE,ECE,中的应用 | Anal Chim Acta,2012, 734: 1–30 |
6 | 碳纳米管在分析科学中的应用(引用93篇文献) | 在分离、传感器、样品制备中的应用 | Microchim Acta,2012,179:1–16 |
7 | 碳纳米管在分离科学中的应用研究进展(引用90篇文献) | 在SPE,SPME,LC,GC,CE中的应用 | 色谱,2011,29(1):6-14 |
8 | 碳纳米材料在分析化学中的应用(引用215篇文献) | 在样品制备、分离及检测中的应用 | Anal Chim Acta,2011,691:6-17 |
9 | 碳纳米管用于原子吸收光谱分析金属的固相萃取吸附剂(引用140篇文献) | 固相萃取吸附剂 | Anal Chim Acta,2012,749:16-35 |
10 | 碳纳米管用于磁固相萃取吸附剂(引用116篇文献) | 固相萃取吸附剂 | Anal Chim Acta, 2015,892:10-26 |
11 | 碳纳米管用于杀虫剂分析的吸附剂(引用 53篇文献) | 固相萃取吸附剂 | Chemosphere,2011, 83:1407–1413 |
12 | 碳基吸着剂-碳纳米管(引用194篇文献) | 固相萃取吸附剂 | J Chromatogr A, 2014, 1357:53–67 |
13 | 固相萃取新倾向——新吸附介质(引用153篇文献) | 固相萃取吸附剂 | TrAC,2016,77:23–43 |
14 | 色谱分析样品处理中的固相萃取吸附剂进展(引用214篇文献) | 固相萃取吸附剂 | TrAC,2014,59:26-41 |
15 | 固相萃取吸附剂中新材料及倾向(引用 68篇文献) | 固相萃取吸附剂 | TrAC,2013,43:14-:3 |
16 | 碳纳米管应用研究进展(引用 47 篇文献) | 固相萃取吸附剂 | 化工进展,2006,25(7):750-754 |
17 | 磁纳米材料的功能化修饰及在环境分析中的应用研究(引用 116 篇文献) | 固相萃取吸附剂 | 湖南大学邹瑩硕士论文,2014 |
18 | 多壁碳纳米管固相萃取--高效液相色谱技术联用在有机污染物分析中的应用 | 固相萃取吸附剂 | 河南师范大学刘珂珂硕士论文,2012 |
19 | 多壁碳纳米管在痕量元素分离富集中的应用 | 固相萃取吸附剂 | 华中师范大学丁琼硕士论文,2006 |
20 | 基于碳纳米管表面分子印迹固相萃取材料研究(引用 131 篇文献) | 固相萃取吸附剂 | 吉首大学张华斌硕士论文,2011 |
21 | 生物功能化碳纳米管的合成、表征及分析应用(引用 147 篇文献) | 碳纳米管作为吸附剂的研究 | 南开大学刘越博士论文,2009 |
22 | 碳纳米材料在环境分析化学中的应用研究(引用 107 篇文献) | 固相萃取吸附剂 | 河南师范大学汪卫东硕士论文,2006 |
23 | 新型纳米材料与传统吸附材料 | 固相萃取吸附剂 | 东南大学邓思维硕士论文,2014 |
24 | 新型吸附材料在样品前处理技术中的应用研究(引用 170 篇文献) | 固相萃取碳纳米管 | 西南大学汪卫东博士论文,2009 |
25 | 修饰碳纳米管对砷的吸附及其应用研究 | 固相萃取吸附剂 | 西南大学李璐硕士论文,2009 |
来源于:仪器信息网
热门评论
最新资讯
新闻专题
更多推荐














