冷冻电镜首个新冠病毒蛋白结构解析发布:传染性为何强?
导读:2月15日,美国得克萨斯大学奥斯汀分校在预印本平台bioRxiv上发表论文:报道了新冠病毒(2019-nCoV)S蛋白的首个冷冻电镜结构。
仪器信息网讯 2020年2月15日,美国卫生总署(NIH)与美国得克萨斯大学奥斯汀分校Jason S. McLellan研究组合作在预印本平台bioRxiv上发表论文:Cryo-EM Structure of the 2019-nCoV Spike in the Prefusion Conformation(DOI: 10.1101/2020.02.11.944462),报道了新冠病毒(2019-nCoV)S蛋白的首个冷冻电镜结构,利用冷冻电镜技术分析了新型冠状病毒表面S蛋白的近原子结构。
(注:预印本网站bioRxiv的所有论文未经同行评议, bioRxiv在所有2019-nCoV相关论文页面增加了突出字体说明(上图黄底黑字):“bioRxiv收到了许多关于2019年ncov冠状病毒的新论文。提醒一下:这些是没有经过同行评审的初步报告。他们不应被视为结论性的,指导临床实践/健康相关的行为,或在新闻媒体中作为既定信息进行报道。”)
作者通过生物物理以及结构方面的证据发现,新冠病毒的S蛋白结合人体ACE2(宿主细胞受体血管紧张素转化酶2)的亲和力要远高于SARS-CoV的S蛋白,或解释了新型冠状病毒传染性很强的主要原因。
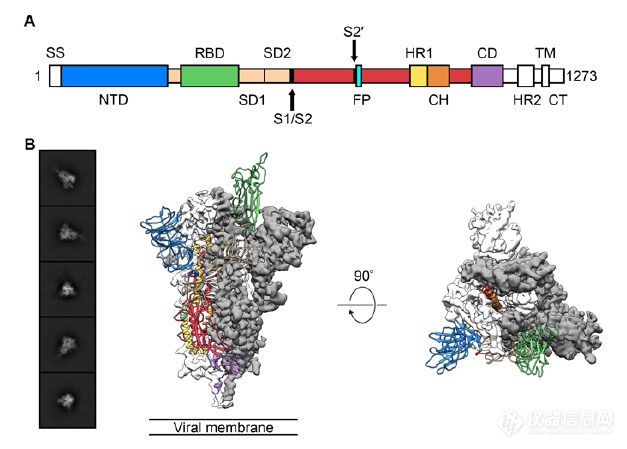
预融合构象中的2019-nCoV S结构
新型冠状病毒(2019-nCov)的爆发代表了一种流行病威胁,已宣布为国际关注的突发公共卫生事件。CoV突刺(S)糖蛋白是疫苗、治疗性抗体和诊断方法的关键靶标。此前的大量研究均基于2019-nCoV突刺蛋白的预测结构或相关病毒(如SARS)的突刺蛋白的已知结构展开。为促进医学对策(MCM)的开发,论文中确定了预融合构象中的2019-nCoV S蛋白三聚体冷冻电镜结构,为3.5埃分辨率。三聚体的主要状态为三个受体结合结构域(RBD)之一向上旋转为受体可及构象。同时,生物物理和结构证据表明, 2019-nCoV S以比SARS-CoV S更高的亲和力结合ACE2(宿主细胞受体血管紧张素转化酶2)。此外,作者测试了几种已发布的SARS-CoV RBD特异性单克隆抗体,发现它们与nCoV-2019没有明显的结合。这表明两种病毒RBD之间的抗体交叉反应性可能受到限制。
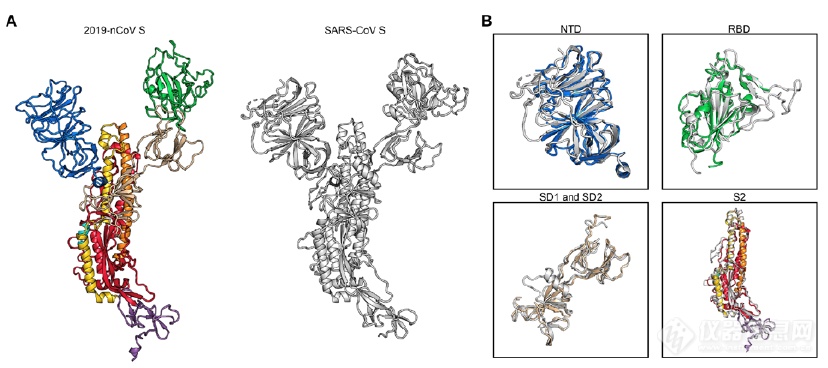
2019-nCoV S.和SARS-CoV S.之间的结构比较(A)
新型冠状病毒利用高度糖基化的同源三聚体S蛋白进入宿主细胞。S蛋白经历结构变化将病毒融合进入宿主细胞的细胞膜。此过程包括病毒的S1亚基结合到宿主细胞受体上,引发三聚体不稳定性的发生,进而造成S1亚基脱落S2亚基形成高度稳定的融合后结构。
通过该结构分析,作者发现S1亚基中的RBD经历铰链类似运动,此移动特点与SARS-CoV以及MERS-CoV均非常相似,但新型管冠状病毒中则RBD结构则更靠近三聚体的中央部位,其S蛋白中3个RBP中的1个会向上螺旋突出从而让S蛋白形成能够轻易与宿主受体ACE2结合的空间构象。这也说明,新型冠状病毒引发病毒的机制虽然与其他的冠状病毒科的病毒机制异曲同工,但传染性更强。
论文受到业界的广泛关注,研究中,John Ludes-Meyers博士对细胞转染给予很大帮助,德克萨斯大学奥斯汀分校Sauer结构生物学实验室的Aguang Dai博士在显微镜对准方面做了大量工作。
论文链接:https://www.instrument.com.cn/download/shtml/932743.shtml
来源于:仪器信息网译
热门评论
最新资讯
新闻专题
更多推荐