新冠小分子药物赛道火热,如何加速上市过审成为关键
2月11日,国家药监局批准辉瑞新冠口服药paxlovid进口注册,成为中国初款获批的新冠口服药。3月11日,辉瑞公司确认中国医药负责paxlovid在中国大陆市场的商业运营。
至此,国内小分子新冠药物研发进入“生死竞速”时刻。
什么是小分子药物?
一般来说,原料药物指用于制剂制备的活性物质,包括中药、化学药、生物制品原料药物。而小分子药物主要是指化学合成药物,通常分子量小于1000的有机化合物。
在常用药物中,小分子药物的数量可占总量的98%。如生活中常见的镇痛、解热、消炎药——阿司匹林,是世界医药史上三大经典药物之一。

图1:阿司匹林化学结构式
新冠小分子药物为何应运而生?
因其独特的作用机制,小分子药物具有对变异株普遍有效的潜力。新冠病毒不断发生变异的过程中,表面结构蛋白很容易发生结构的改变,但是胞内过程相对保守,不易发生突变,因此作用于胞内过程的小分子药物具有对变异株普遍有效的潜力。因此,小分子化药是新冠治疗的又一选择。
大部分小分子药物可以做成口服剂型。一是因为相对于需要静脉输液的中和抗体,具有便利性优势,尤其是无需住院的轻中症患者,可以在确诊后自己口服药物,不会对医疗资源(如医院床位资源、医护人员资源等)造成额外负担。二是产能优势,小分子口服药物的生产与大分子生物药相比相对简单,生产线和产能提升相对容易,能满足更多患者的需求。另外,整个治疗过程的费用更少。
而针对新冠轻中症非住院患者,目前已有3 款小分子药物获批上市,分别是辉瑞的口服药 Paxlovid,默沙东的口服药 Mulnupiraivr,和吉利德的瑞德西韦注射液。目前在研药物中,进展较快的包括开拓药业的口服药普克鲁胺,真实生物的口服药阿兹夫定,君实生物的口服药 VV116,以及日本盐野义的口服药 S-217622。国内进入临床阶段的还有先声药业的口服药 SIM0417,更多小分子口服药处于临床前阶段。
图2:辉瑞的新冠*药Paxlovid
国内外各个知名药企都在加速研发和上市新冠小分子*药,而这些药物在获得FDA/CFDA批准批准上市前及上市后,每批次都要经过一系列QC检查,其中溶出度检查至关重要!
溶出度检查
问:《中国药典》规定了哪些药物制剂需要进行溶出度检查(通则0931)?
答: 片剂:口腔贴片、分散片、缓释片、控释片、肠溶片、口崩片等应进行溶出度或释放度检查;
胶囊剂:缓释胶囊、控释胶囊、肠溶胶囊等应进行溶出度或释放度检查;
除此之外,部分颗粒剂和透皮贴剂也要进行溶出度或释放度检查;
毋庸置疑,作为口服剂型的新冠小分子药物,也要做符合《中国药典》的溶出度检查。
问: 什么是溶出度?
答: 指活性药物从片剂、胶囊剂或颗粒剂等普通制剂在规定条件(溶出介质、温度、转速)下溶出的速率和程度。
在缓释制剂、控释制剂、肠溶制剂及透皮贴剂等制剂中也称释放度。
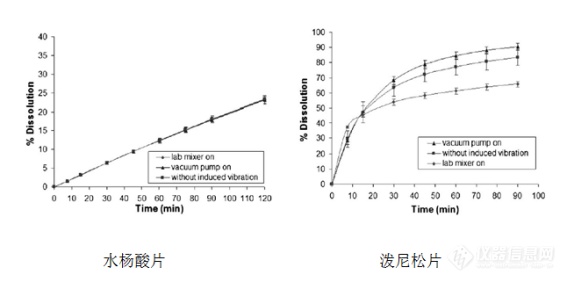
图3:溶出曲线
问: 溶出度检查方法有哪些?
答: 针对不同的药物剂型,都有特定的检查方法,如下:
*法——篮法
第二法——桨法
第三法——小杯法
第四法——桨碟法
第五法——转筒法
第六法——流池法
第七法——往复筒法
篮法和桨法适合普通制剂、缓释制剂、控释制剂、肠溶制剂等大部分药物制剂;小杯法适合特定制剂;桨碟法、转筒法适合透皮贴剂;流池法和往复筒法适合难溶制剂。
溶出度仪为小分子药物质检把关

图4:PTWS 1420 14杯位溶出度仪
Pharma Test溶出度仪优势
1)根据取样方式,分为手动、半自动和全自动,多种取样方式可选,适合不同类型的操作习惯;
2)根据溶出杯数量,分为6杯位、7杯位、8杯位、12杯位和14杯位,满足大部分用户的使用要求;
3)完全符合USP<711 724="">和EP<2.9.3 4="">,以及中国药典的要求;
4)Monoshaft™设计,在更换USP1、2、5、6法装置时,无需重新定高度,见图6;
5)EPE自动取样器在取样点自动进入溶媒中并自动定位取样位点,取样结束后自动回位等待下一次取样;
6)ITM可实时监测每个杯位温度,TMA可自动投药;
7)1500W快速水浴升温功能,水浴槽可以简单的进行拆除和清洗,水浴扩散器可保证温度的均一性;
8)具有方法管理和用户管理功能,可进行三级管理,SD卡自动储存无限种方法。

图5:Monoshaft™设计
来源于:德祥科技有限公司
热门评论
最新资讯
厂商动态
新闻专题
更多推荐













