中山大学李惠琳团队成果:整合Top-down及Bottom-up蛋白质组学质谱表征核糖体蛋白异质性
导读:本文整合了Top-down及Bottom-up蛋白质组学质谱方法,全面表征了E.coli 70S核糖体和HeLa 80S核糖体蛋白质,提供了一种先进的方法来确定疾病特异性proteoforms或靶点。
大家好,本周为大家分享一篇本课题组发表在Journal of Pharmaceutical Analysis上的文章,Integrated top-down and bottom-up proteomics mass spectrometry for the characterization of endogenous ribosomal protein heterogeneity [1],文章的通讯作者是中山大学药学院的李惠琳教授。
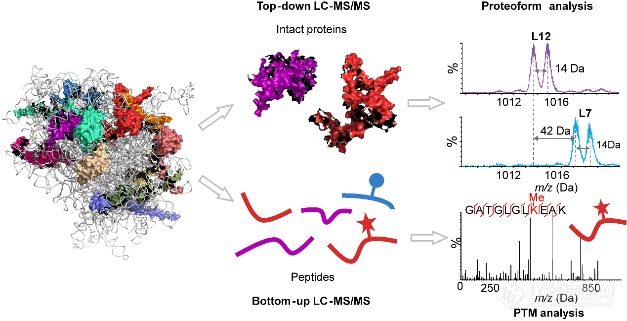
蛋白质的合成过程是生物体内最重要的生命活动之一。在细胞中,核糖体是信使RNA翻译合成蛋白质的细胞机器。核糖体高度复杂,它主要由特化的RNA和几十个蛋白组成。这些蛋白和RNA组装成两个不同大小的核糖体亚基即大亚基和小亚基。近年来,多项研究表明,核糖体与多种疾病的发生密切相关,包括恶性肿瘤、阿尔兹海默病和帕金森病等,这些过程中除发生rRNA合成异常和核糖体蛋白表达失调外,还伴有核糖体蛋白基因突变、RNA剪切、翻译后修饰(PTMs)变化所形成的核糖体蛋白异质体(proteoforms)的异常表达和调节。本文中,作者整合了Top-down及Bottom-up蛋白质组学质谱全面表征了核糖体蛋白异质性,为发现疾病特异型proteoform生物标志物或靶点提供了方法。
首先,作者采用E.coli 70S核糖体在Waters SYNAPT G2-Si MS仪器上建立了Top-down检测方法(图1)。50S核糖体大亚基蛋白质L7和L12具有相同序列,其差别在于L7在N-端含有乙酰化修饰而L12无N-端非乙酰化修饰。实验发现,L7和L12在Top-down分析中取得了良好的分离,并且L7和L12的峰放大图显示二者除含有其对应野生型外,它们都具有甲基化的proteoforms,而Bottom-up仅能检测到甲基化的肽段(图2)。L7/L12在蛋白质生物合成过程中参与和翻译因子的相互作用,是肽链终止所必需的。L7/L12发生异常会降低蛋白质的合成速度和准确性。本研究中,作者采用Top-down方法对L7/L12的PTMs和proteoforms进行了全面分析,并结合Bottom-up定位了甲基化位点。同时,该结果也反映出Bottom-up方法固有的缺陷,即从小肽推断出的有限的序列信息往往不足以鉴别proteoforms。
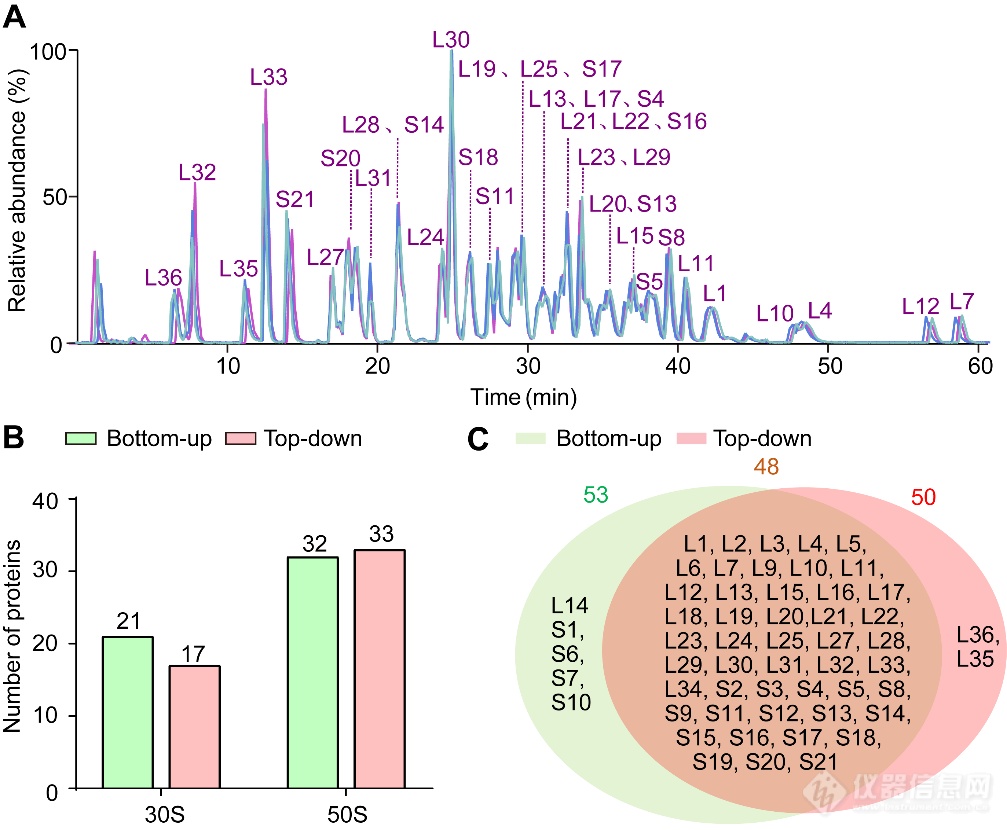
图1. Top-down和Bottom-up蛋白质组学表征E.coli 70S核糖体总览
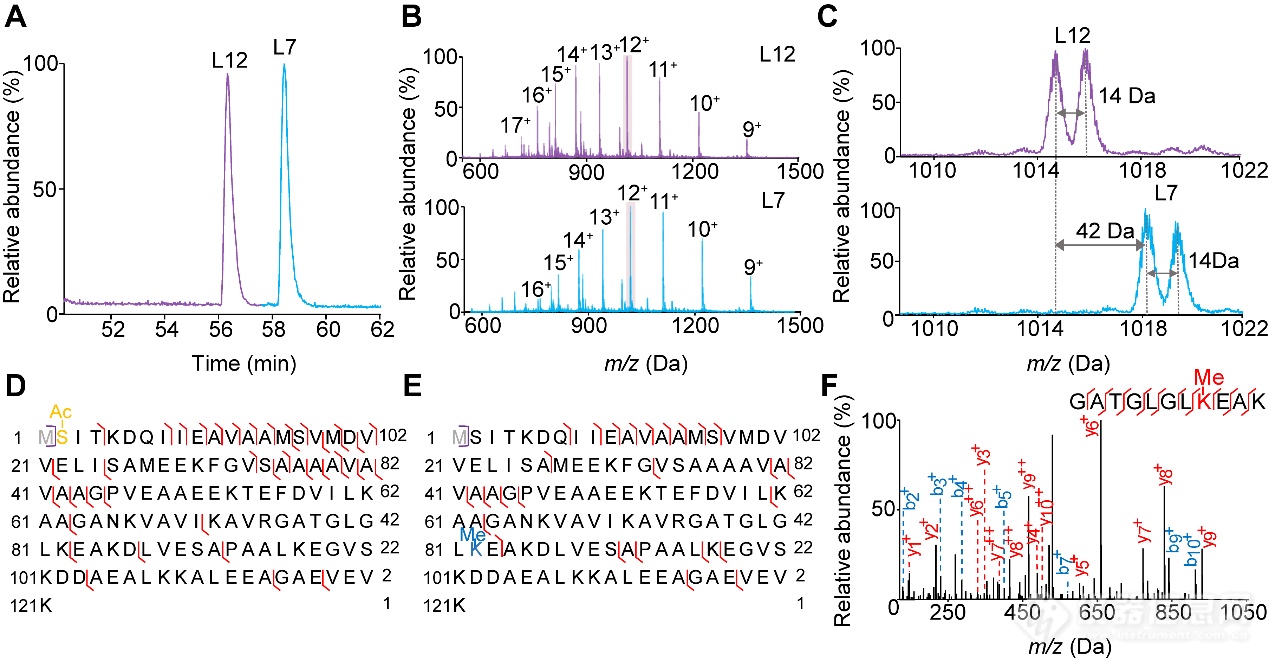
图2. Top-down和Bottom-up蛋白质组学表征E.coli 50S核糖体亚基蛋白质L7/L12
随后,作者采用建立好的方法分析了HeLa 80S核糖体蛋白。如图3A所示,实验检测到大量Methionine剪切伴随的N-端乙酰化、40S RP S10和S25上的二甲基化、40S RP S23上的hydroxyproline、60S RP L8上的hydroxyhistidine、乙酰化和甲基化等多种修饰。值得关注的是,Top-down结果显示多种蛋白存在截短型的truncated proteoforms。分子完整性是保证蛋白质生物学功能的重要因素之一。分子完整性的缺失,特别是由于选择性剪接或蛋白质水解而导致的截短,已成为一个重要的问题。作者在排除蛋白质提取过程造成的影响、色谱柱上酶切和质谱源内裂解等因素后,认为截短型的proteoforms很大程度上与生物过程相关。RP L19是一个从60S亚基突出并跨越到40S亚基的长螺旋蛋白质,L19的C端螺旋在pre-translocation状态下扭结,在亚基旋转时动态地改变构象,在post-translocation状态下变为线性(图3B)。这种构象转变导致蛋白质L19带正电的Arg172和Arg176侧链与18S rRNA核苷酸G909和G910的磷酸根之间形成盐桥。本文中,作者观察到C端部分序列缺失的截断型L19。除此之外,其他截短型的蛋白质如图C所示。目前研究发现,核糖体蛋白质除了在细胞翻译和蛋白质合成中发挥核心作用外,还具有核糖体外功能,参与细胞增殖、分化、凋亡、DNA修复、调节细胞迁移和侵袭等细胞过程。以截短型形式观察到的许多核糖体蛋白,都与血液、代谢、心血管疾病和癌症的发展与进展有关,核糖体蛋白proteoforms的全面表征为发现潜在疾病生物标志物或靶点提供了前题条件。
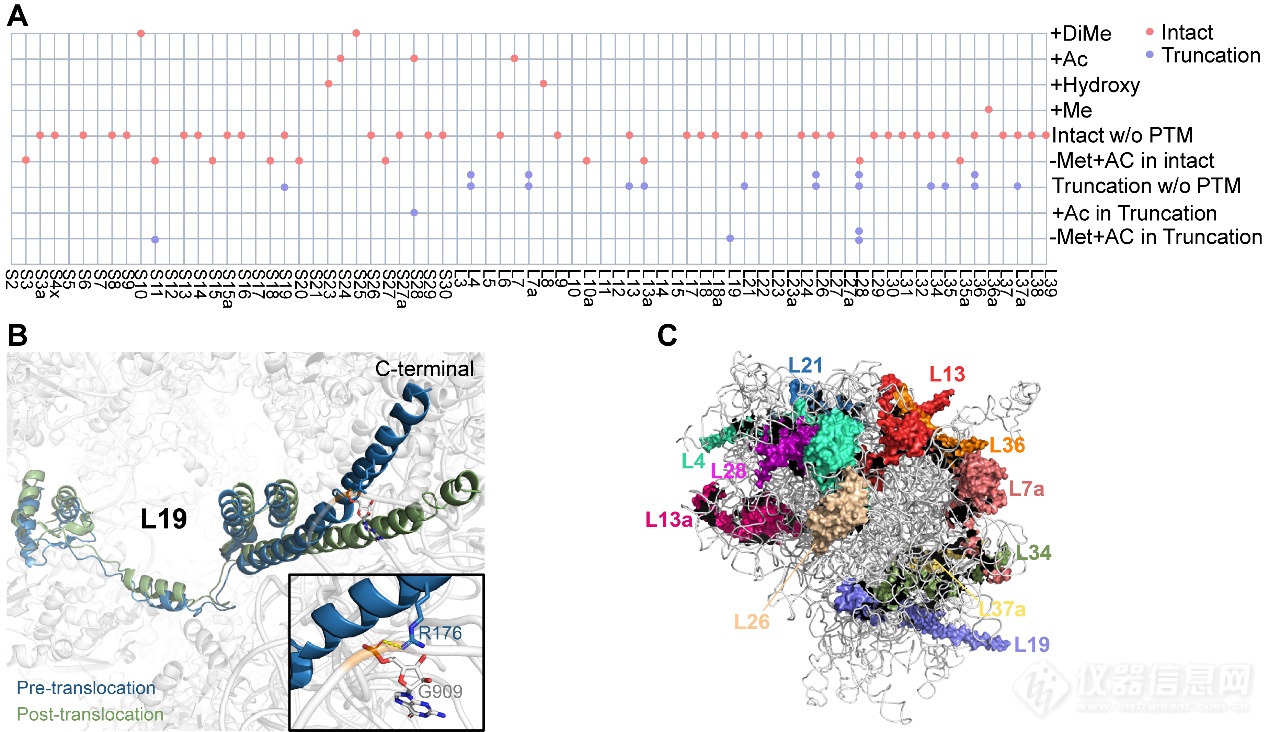
图3. 利用Top-down蛋白质组学方法鉴定HeLa 80S核糖体蛋白质PTM及proteoforms
总的来说,本文整合了Top-down及Bottom-up蛋白质组学质谱方法,全面表征了E.coli 70S核糖体和HeLa 80S核糖体蛋白质。尽管这些proteoforms和疾病的相关性还需要深入挖掘,但实验提供了一种先进的方法来确定疾病特异性proteoforms或靶点。
来源于:仪器信息网
热门评论
最新资讯
新闻专题
更多推荐