NMPA批准三类注册证:首个核酸质谱药物基因组多基因检测试剂盒
2024年7月,迪谱诊断自主研发的“先蕊谱®人CYP2C19、ALDH2、ApoE和 SLCO1B1 基因检测试剂盒(PCR-飞行时间质谱法)”,成功获批三类医疗器械注册证(国械注准20243401289)。
先蕊谱®C8基因检测试剂盒示意图
先蕊谱®C8试剂盒(Cardiovascular Diseases 4基因8位点),是以冠心病患者为代表的药物基因检测试剂,是国内首个基于飞行时间核酸质谱技术进行合并用药多基因多位点检测的试剂盒,搭载DP-TOF飞行时间质谱检测系统,合并用药-联合检测,缩短了检测技术人员多管多次PCR操作时间,减少了临床医生的选药困扰,降低了患者病程药物不良反应事件,减轻了患者经济负担,无荧光标记干扰,质谱检测提升了检测准确度,打造了更准、更全、更灵敏的心血管疾病药物基因组多联检解决方案。
作为国内首个基于飞行时间核酸质谱技术进行药物基因组(PGx)“合并用药-联合检测”的多基因多位点获证试剂盒,该产品通过体外定性检测人体外周血样本中的CYP2C19、ALDH2、ApoE和SLCO1B1基因多态性,检测结果可辅助氯吡格雷、硝酸甘油和他汀类药物的个体化用药指导,助力心血管疾病精准治疗。

据《中国心血管健康与疾病报告2022》数据显示,我国心血管疾病(CVD)现患者达3.3亿,每5例死亡中就有2例死于心血管疾病,每年心血管疾病死亡387万,占我国疾病总死亡的44.74%,高居疾病死亡构成的首位。

合并用药:由于心血管疾病患者往往多种症状并存,因此临床治疗上经常需要合并用药。以冠心病为例,《冠心病合理用药指南(第2版)》中明确指出,改善缺血、减轻症状的药物(含硝酸甘油)应与预防心肌梗死的药物(含氯吡格雷、他汀类)联合使用。《稳定性冠心病诊断与治疗指南》中建议,最佳药物治疗方案应包括至少1种抗心绞痛/缓解心肌缺血药物(含硝酸甘油)与改善预后(含氯吡格雷、他汀类)的药物联用。《急性冠脉综合征急诊快速诊治指南》指出,ACS抗血小板(含氯吡格雷)、抗缺血治疗(含硝酸甘油)是基本治疗,无他汀类药物禁忌症的患者入院后尽早开始他汀类药物治疗,长期维持。
精准治疗:心血管疾病患者大多数需要长期服药,同类疾病的患者服用同一种药物的疗效和安全性往往存在较大个体差异。除了年龄、性别、种族/民族、疾病状态、器官功能等其他因素,遗传因素基因多态性是引起药物不良反应及其疗效个体差异的首要原因。心血管药物基因学的卫生经济学研究备受关注。根据CPIC指南、PharmGKB数据库、FDA公布的相关遗传信息与用药建议、国内《药物代谢酶和药物作用靶点基因检测技术指南(试行)》等,CYP2C19基因可指导抗血小板药物种类和剂量的选择(1A证据);SLCO1B1基因指导选择更合理的他汀药物剂量,避免肌病风险(1A证据);ApoE基因评估他汀疗效,助力选择更合适的他汀(2级证据);ALDH2基因评估硝酸甘油疗效,指导心绞痛发作的预防(2级证据)。

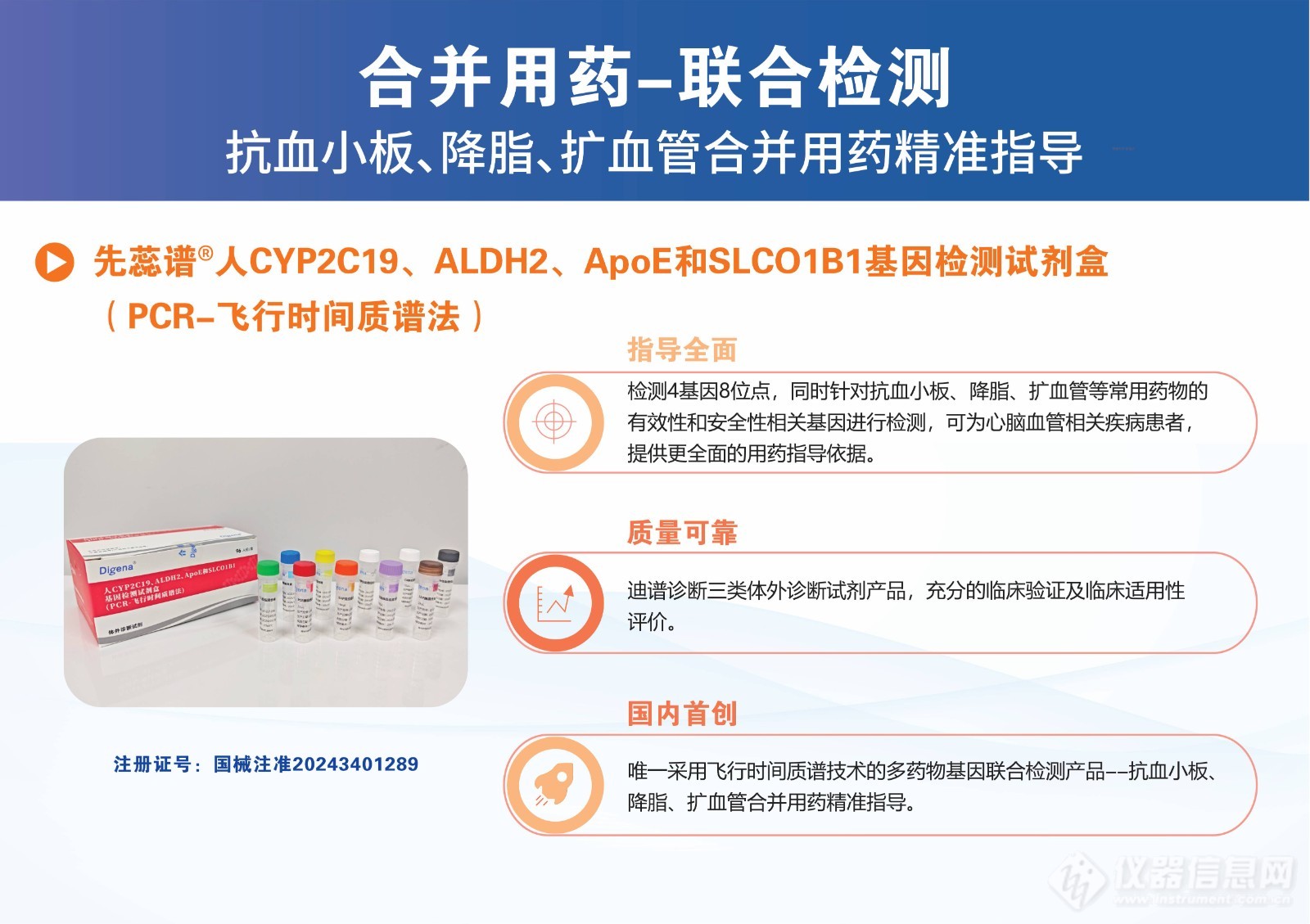
迪谱诊断DP-TOF核酸质谱检测特点
多基因多位点检测
检测周期短,高效率
高准确度,高灵敏度
操作简便,成本低
样本量与类型灵活
样本类型
人体外周血样本,需要采集受检者静脉血不小于1ml,注入含EDTA抗凝剂的采血管。
适用人群
需要服用氯吡格雷、他汀、硝酸甘油相关药物的冠心病患者/心肌梗塞或其他外周动脉疾病的患者/进行PCI手术预后治疗的患者以及高脂血症治疗。
用于脑卒中、癫痫、抑郁症、焦虑症、消化道出血、肾移植等患者的用药指导;载脂蛋白E(ApoE)基因多态性可作为阿尔兹海默症风险筛查指标。
来源于:浙江迪谱诊断技术有限公司
热门评论
最新资讯
厂商动态
新闻专题













