北卡罗来纳大学教堂山分校、国立卫生研究院等机构的研究人员开发出一种基于CRISPR-Cas9的系统,可以利用化学表观遗传修饰因子(CEM)来实现基因表达的激活,而无需使用外源的转录调控蛋白。
这项成果于本周发表在《Nature Biotechnology》杂志上。此系统由两部分组成,其一是带有FK506结合蛋白(FKBP)的催化失活Cas9(dCas9),其二则是CEM,它可以招募内源的转录调控因子,从而激活目标基因的表达。
作者写道:“我们证明,CEM可以使内源位点的基因表达上调20多倍。我们还证明了转录激活的剂量依赖性控制、在多个不同基因上的作用、CEM活性的可逆性以及我们最佳的CEM在整个基因组中的特异性。”
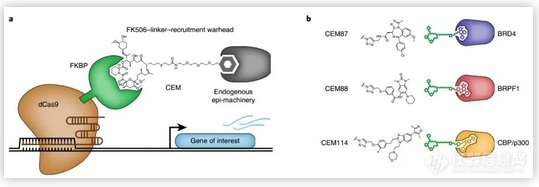
在之前的研究中,科学家证明了CEM能够修饰染色质并抑制改造位点的基因表达。在这项新研究中,他们开发出CEM激活(CEMa)分子,可以招募内源性基因激活机制,包括CEM87、CEM88和CEM114。这些分子分别与不同的转录激活因子相结合。
为了检验基因表达的变化,研究人员利用绿色荧光蛋白(GFP)基因转染了HEK293T细胞,并对共表达gRNA和dCas9机制的细胞开展流式分析。他们用共表达dCas9-FKBP×1或dCas9-FKBP×2以及CEMa分子的质粒激活报告基因。在48小时后,他们发现GFP报告基因的表达均有显著增强。
在优化dCas9系统后,研究人员选择了两个最有效的CEMa分子(CEM87和CEM114)开展时间进程分析。他们用表达dCas9、MS2-FKBP×2和GFP的质粒转染细胞。与未处理的细胞相比,经过CEM87和CEM114处理的细胞在24小时和48小时后产生了GFP高表达。他们还发现,CEM对目标基因的激活调控是可逆的。
为了研究dCas9-CEMa系统的多功能性,研究人员利用靶向白介素1受体拮抗基因(IL1RN)的gRNA进行了测试。与对照细胞相比,经过CEM87处理后,IL1RN基因的表达增强了近96倍。同时,他们还靶向了表达量相对较高的MYC1位点,发现CEM87并未明显增强其表达。
作者总结道:“通过CEMa技术与dCas9载体的融合,我们理论上可以通过该系统来靶向基因组中的任何基因。这种dCas9-CEMa技术为靶向疾病相关的基因铺平了道路,有望解答与疾病机理相关的问题
Science子刊揭示了大脑是如何将疼痛预测和刺激结合起来的
Nature:免疫细胞阻止病毒感染后的肺部愈合
《Neuron》大脑中存储和使用视觉知识的机制
Cell子刊:独特的机制保护胰腺细胞免受炎症的影响
相关产品
UPCISCC090 人舌头鳞癌细胞 QCH766
KNS62 人肺支气管鳞状细胞癌 QCH767
HCC95 人肺腺癌细胞 QCH768
HARA 人肺腺癌细胞 QCH769
EPLC272H 人肺腺癌细胞 QCH770
NCI-H810 人非小细胞肺癌细胞 QCH771
HBL-1 人弥漫性大B细胞淋巴瘤 QCH772
FTC238 人滤泡状甲状腺癌细胞,肺转移 XY-H773
SNU-719 人胃癌细胞 QCH774
BT549+GFP+LUC 人乳腺癌细胞 QCH766GL
IM95m 人胃癌细胞 QCH775
mda-mb-468+GFP+LUC 人乳腺癌细胞 XY-H776LGP
OCUM-1 人胃癌细胞 QCH777
Karpas422 人非霍奇金淋巴瘤 QCH778
CAL-33 人舌鳞癌细胞QCH779

关注

拨打电话

留言咨询