推荐厂家
暂无
暂无
 银牌1年
银牌1年
 400-860-5168转6112
400-860-5168转6112
 留言咨询
留言咨询
 金牌5年
金牌5年
 400-860-5168转4496
400-860-5168转4496
 留言咨询
留言咨询
 钻石23年
钻石23年
 400-611-9236
400-611-9236
 留言咨询
留言咨询

 400-801-8117
400-801-8117
 留言咨询
留言咨询

 400-801-8117
400-801-8117
 留言咨询
留言咨询

 400-611-9236
400-611-9236
 留言咨询
留言咨询





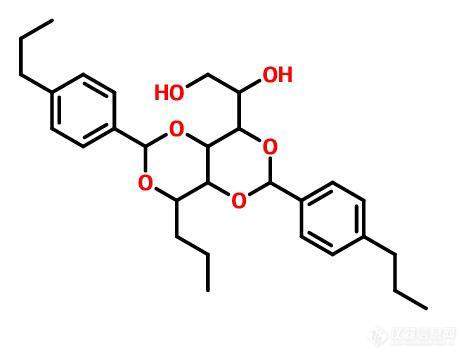
[color=#444444]本人有一化合物,分子量为484,质谱打出来的最大片段是330,求大神合理推断,谢谢[/color][color=#444444][img=,468,359]https://ng1.17img.cn/bbsfiles/images/2019/05/201905141524089682_8480_1827556_3.jpg!w468x359.jpg[/img][/color]
质谱技术是抗体药物分析最重要的技术手段之一。本文简述了抗体药物的发展和质谱技术的原理。对于质谱技术在抗体药物的分析中应用进行了归类整理,主要分为在一级结构和高级结构分析中的应用。抗体类药物是指含有抗体片段的蛋白类药物,所以在恶性肿瘤、自身免疫性疾病、心血管疾病、感染和器官移植排斥等重大疾病上得到了快速的发展,是当前生物药物领域增长最快的一类药物.1.抗体药物发展新趋势在生物药物领域,抗体药物占据着越来越重要的地位,全球销售排名前10位的药物中有6个为抗体药物,抗体药物按来源分类可以分为:鼠源单克隆抗体、人鼠嵌合抗体、人源化抗体和全人源抗体。目前,批准的单克隆抗体药物中,人源化单抗和全人源单抗数量已占据大多数。1.1 抗体药物偶联物(ADC)抗体药物偶联物(ADC)由单克隆抗体和小分子化合物两部分组成。通过抗体的靶向作用,ADC 的抗体部分和肿瘤细胞表面抗原特异性识别并结合,通过细胞内吞作用,将抗体和小分子化合物一起带进肿瘤细胞内部,释放出小分子化合物。这样既可以降低小分子药物的毒性,同时具有靶向结合的作用。已经上市的两个ADC 是Kadyla 和Adcetris。1.2 双特异性抗体(BsAb)双特异性抗体(BsAb)是含有两种特异性抗原结合位点的人工抗体,能在靶细胞和功能分子(细胞)之间架起桥梁,由于基因工程的发展,目前双特异性抗体已经研发出多种类型,主要类型有三功能双特异性抗体、IgG-scFv、三价双特异性分子、串联单链抗体(串联scFv)、DVD-Ig 等多种形式。2.质谱技术近年来质谱仪性能的显著改进主要基于开发出的两种离子化技术:一种是介质辅助的激光解吸/离子化技术。另一种是电喷雾离子化技术。由于这两种电离技术的出现,使原本只能检测小分子的质谱技术,可以运用于检测生物大分子。在过去质谱技术主要运用于对一级结构和序列的表征,而现在质谱技术越来越多地运用于高级结构的分析,而高级结构对于抗体药物的生物活性至关重要。3.质谱技术在抗体药物一级结构分析中的应用3.1 完整抗体药物精确分子量测定当得到抗体药物时,可以直接通过高分辨率的MALDI-TOF或者ESI-MS进行分子量的检测。通过对于脱糖后分子量的检测,可以对于抗体药物进行初步定性分析,并将可以作为药物常规放行的分析方法。对于脱糖前的抗体药物进行分析,可以得到抗体药物的糖基化类型的信息及糖基化水平的分布,对于快速了解生产工艺与药物质量的关系具有十分重要的意义。3.2 药物抗体偶联比(DAR)对于赖氨酸链接的抗体偶联药物,采用C4色谱柱及联用的质谱对去糖基化样品进行分析,根据偶联不同数目药物分子的质量数增加判断偶联数目。对于质谱测定的结果,不仅可以给出确切的药物抗体偶联比值,更能够给出链接不同个小分子药物的分布情况,及反应过程副产物空链接头的分布情况。3.3 肽图谱分析蛋白被特异酶切后的蛋白酶水解后得到的肽片段质量图谱。由于不同的抗体药物具有不同的氨基酸序列,蛋白质被酶水解后,产生的肽片段也各不相同,肽混合物的质量数具有唯一特征。可以通过LC-ESI-MS进行肽片段的一级质量数的鉴定,也可以通过LC-ESI-MS/MS对于每个肽片段进行进一步确证,提高肽图谱的准确性。3.4 翻译后修饰研究蛋白质的翻译后修饰(PTM)对于抗体药物的生物学功能十分重要。常见的翻译后修饰有:磷酸化、脱酰胺、甲硫氨酸氧化、糖基化修饰、N端焦谷氨酸环化,C端赖氨酸切除等。质谱分析仪检测蛋白和肽片段的分子量偏差,可以实现高灵敏、高通量和高精确地鉴别蛋白质的翻译后修饰的种类。3.5 N端氨基酸序列检测常规N端氨基酸检测用Edman降解法进行检测,但是抗体药物有时候会出现N 端环化的现象,在这种情况下用Edman降解法需要先对抗体进行去封闭处理,而直接使用质谱可以直接测出N端的氨基酸序列,同时可以检测出N端环化的相对比例。4.质谱技术在抗体药物高级结构分析中的应用4.1 氢/氘交换质谱(HDX-MS)常规的质谱只能获得蛋白的一级结构信息。氢/氘交换质谱(HDX-MS)可以进行蛋白质构象,溶液动力学和表位映射进行分析。在能够调查的蛋白质的高阶结构和动态结构技术中,HDX-MS已经证明适合单克隆抗体和单克隆抗体-抗原复合物的构象分析。4.2 离子淌度质谱法(IM-MS)离子淌度是根据蛋白的电荷和形状选择性分离的方法,可以区分相同分子量的蛋白和肽段,可用于检测蛋白的简单高级结构。4.3 高分辨率傅立叶变换离子回旋共振质谱(FTICR-MS)高分辨率傅立叶变换离子回旋共振质谱(FTICR-MS)能够检测最高质量数的质谱仪器,并且有着很高的分辨率。FTICR-MS 是目前被公认为是蛋白质组学研究的有力工具,特别是和完整的蛋白质鉴定和上/下调翻译后修饰(PTM)蛋白质的鉴定。
我的一个朋友学生物的,最近正发愁如何对DNA片段进行液相分析。问了下,DNA片段是人工合成的,所以基体并不复杂,目的是通过对目标物的测定,表征之前的生物过程效果(内切什么的),分子量3000左右。由于自己对生物学方面知识薄弱(早已忘记了DNA分子化学结构为何、有何基团),没有提出意见。回来查了一下。首先看到的是Transgenomic公司wave商品名的DNA分离分析系统。看了下介绍,原来所谓的“分子桥”就是离子对色谱法。对于阴离子(磷酸基团PKA1为1-2)的核酸片段,通过加入三乙基胺醋酸盐,与之形成离子对,通过三乙基胺的疏水性与C18作用,形成保留,然后用乙腈洗脱,似乎没什么专利的内容。后来发现,关键在于那根特别的C18链的DNA分析柱,“无孔多苯乙烯-二乙烯基苯 (PS-DVB)共聚物微球(3微米)与C18形成稳定的固相”。疑问1:这种非硅胶基质的C18柱有何神奇之处?硅胶基质的C18为能不能做(估计不能,要不就不是专利了)?(硅胶表面的硅羟基会不会和DNA有什么反应)疑问2:有孔与无孔,对于这种大分子有何不同?孔径方面要选多大的,120A的会堵柱子么?疑问3:wave仪器的柱温为50-80度之间,分别应对非变性,部分和全部变性。这里的变性为何?一般柱温箱和C18的柱子柱温上限为多少?文献方面,看到一些用强阴离子交换(SAX)做的。tris-HCl缓冲系统,pH控制在9。此时DNA片段挂在SAX柱上。然后通过NaCl梯度淋洗(Cl-竞争?),洗脱下DNA分子片断。自己并不懂离子色谱。疑问1:SAX柱怎么使用和维护?需要注意什么?硅胶基质的和聚合物基质相比除了pH耐受性外有何不同?疑问2:为何选用NaCl淋洗?淋洗完后,挂在柱上的季胺上的Cl-怎么办?疑问3:此方法与那个wave相比,优点和缺点为何?其实疑问有很多,就不一一列出了,希望有经验的前辈多多发言,不吝赐教,小生感激涕零。


