推荐厂家
暂无
暂无
 银牌1年
银牌1年
 400-860-5168转6112
400-860-5168转6112
 留言咨询
留言咨询
 留言咨询
留言咨询
 金牌5年
金牌5年
 400-860-5168转4496
400-860-5168转4496
 留言咨询
留言咨询

 400-611-9236
400-611-9236
 留言咨询
留言咨询

 400-860-5168转0230
400-860-5168转0230
 留言咨询
留言咨询

 400-611-9236
400-611-9236
 留言咨询
留言咨询
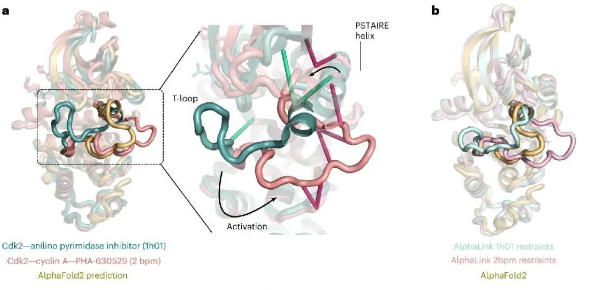


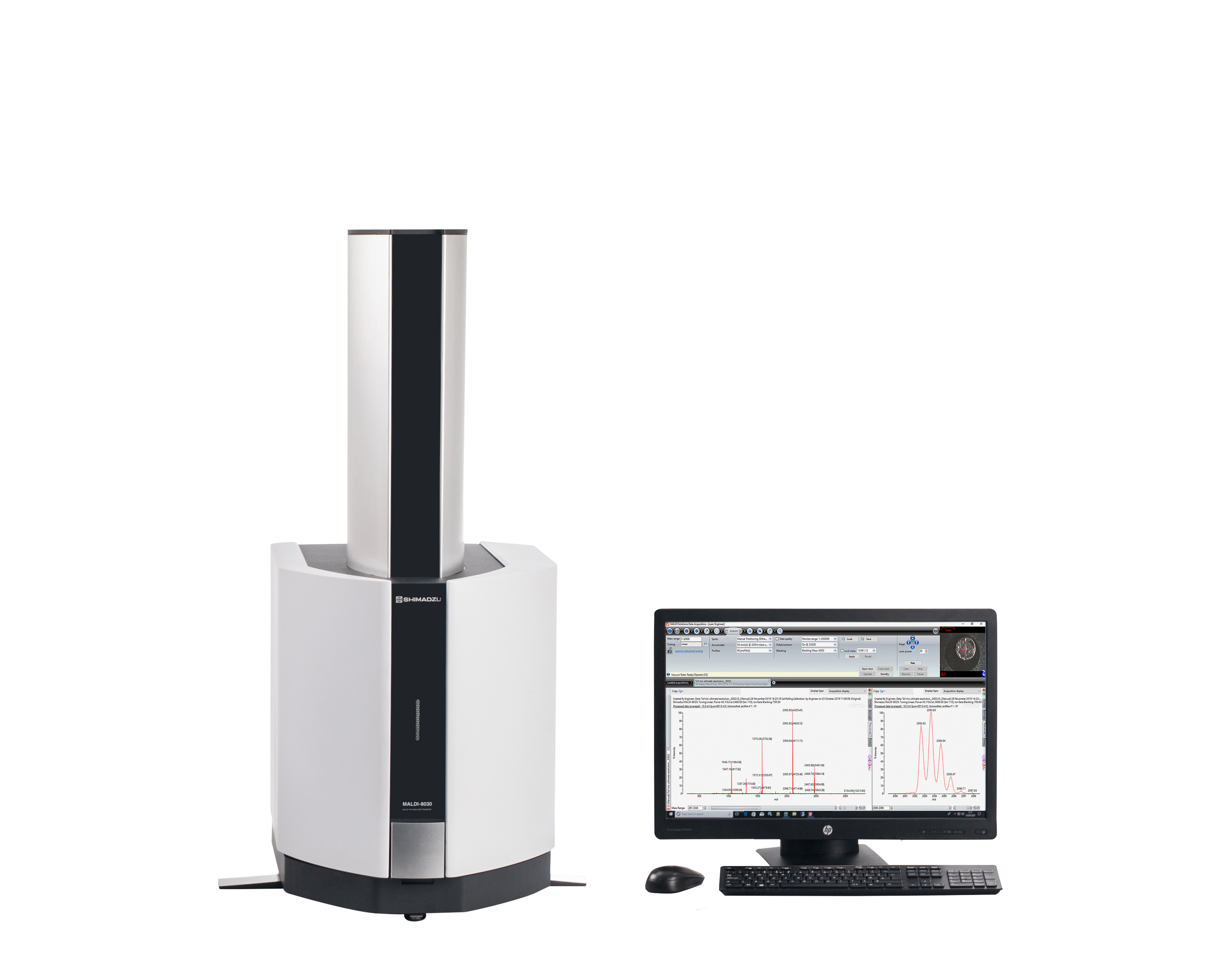

chemdraw怎么预测质谱
质谱市场规模预计将从2020年的41亿美元增长到2025年的56亿美元,复合年增长率为6.5%。全球药品研发支出增加,政府对药品安全的监管,对食品质量的日益重视,原油和页岩气产量增加,在预测期内,不断增长的政府污染控制和环境检测举措是质谱市场的高增长前景。[align=center][url=https://www.antpedia.com/batch.download.php?aid=285254][img]https://i2.antpedia.com/attachments/2021/02/171857_202102261424281.jpg[/img][/url][/align][align=center][font=黑体, SimHei]COVID-19的意外爆发极大地影响了质谱市场。预计到2020年,市场将见证一系列多样化的采用。在医疗保健和制药、生物研究以及食品和饮料行业,采用质谱技术进行测试应用的可能性很大。新药开发,药物再利用,以及药物制剂产量的增加,使得制药行业对安全和质量措施的需求日益增加。严格的政府法规和这些行业对质量维护需求的增加推动了质谱法的采用。然而,石化行业供应链的中断,以及污染监测监管的放松,预计将限制质谱仪的采用。[/font][/align][color=#0070c0][b] 质谱市场动态[/b][/color][b] 驱动因素:制药和生物技术行业研发投资增加[/b] 近两年来,医药企业的研发支出大幅增加几十年。研究制药和生物技术行业的活动是由对关键领域的投资推动的,如生物制药和个性化医药。根据2018年欧盟工业研发投资记分牌,制药和生物技术行业占全球研发支出总额的18.9%。从药物发现的早期阶段到药物开发和临床试验的后期阶段,质谱技术在制药工业中发挥着关键作用。因此,增加医药和生物技术行业的资金有望推动质谱市场的增长。[b] 限制:产品的高定价[/b] 质谱仪器配备了先进的特点和功能,因此价格昂贵。除了系统成本外,系统符合行业标准的成本也非常高。由于技术的进步和操作效率的提高,对质谱仪的需求在过去几年中不断增长。然而,技术的发展提高了系统的价格。质谱仪的价格影响最终用户的购买决策。制药公司需要许多这样的系统,因此,资本成本大大增加。此外,学术研究实验室发现很难负担得起这样的系统,因为它们控制着预算。这些是限制最终用户采用质谱系统的主要因素。[b] 机遇:新兴国家的增长机遇[/b] 中国和印度等发展中国家为质谱市场的增长提供了各种机会。由于在这些国家的各个终端用户行业正在建立绿地项目,中国和印度对单一质谱仪和混合质谱仪器产生了巨大的需求。这些国家的生物制药工业很强劲,预计将对质谱和色谱分析市场的增长作出重大贡献。主要行业参与者正在建立新的设施、研发中心和创新中心,以利用这一机会,并与亚洲市场的参与者进行合作。 [b] 挑战:缺乏熟练的专业人员[/b] 有效使用质谱分析设备需要有相关经验和知识的熟练人员。在[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]或[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]中错误的操作会影响最终结果的质量。此外,在质谱法中,样品制备(包括等分、稀释和提取)是分离感兴趣的分析物的关键步骤。它消除了可能影响结果精度的干扰。缺乏正确选择技术的知识也会影响结果,并可能给最终用户带来直接和间接的费用。目前,在方法开发、验证、操作和故障排除活动方面缺乏熟练的人员,预计这将在未来几年在一定程度上抑制质谱市场的增长。 [b] 以终端用户分类,预计2020年至2025年,制药行业终端用户部门的复合年增长率将达到最高水平。[/b] 以终端用户为基础,质谱市场被细分为制药行业、生物技术行业、科研院所、环境检测行业、食品饮料检测行业、石化行业等终端用户。制药行业是质谱仪的主要终端用户之一。在预测期内,政府和企业为药物研究提供资金的可行性、制药行业的增长以及药物开发和安全方面存在严格的监管准则是推动该领域增长的一些关键因素。[b] 以质谱种类分类,在预测期内,混合质谱细分市场预计将以质谱市场最高的复合年增长率增长。[/b] 以产品为基础,质谱市场细分为混合质谱、单一质谱和其他技术。混合质谱部分预计在预测期内增长最快。混合质谱仪的优点,如快速和高分辨率的测试能力,更准确和精确的结果,正在增加其采用。因此,用于高通量筛选的质谱设备的需求也在增长。混合质谱部分进一步分为三重四极、四极杆飞行时间(Q-TOF)和傅里叶变换质谱(FTMS)。[b] 以应用分类,在预测期内,生命科学研究部门预计将以最高的复合年增长率增长。[/b] 以应用为基础,质谱市场已细分为生命科学研究、药物发现、环境检测、食品检测、应用产业、临床诊断等应用领域。其中,生命科学研究板块在2019年占据市场主导地位。组学技术在诊断学和生物标记物鉴定中的应用日益广泛,蛋白质组学的研发支出和政府资金的增加预计将推动这一领域的市场。 预计在预测期内,北美将是最大的市场。[b] 以地区划分,在预测期内,预测北美仍是质谱法的最大市场。[/b] 北美的质谱市场主要是由以下因素推动的:美国研究和政府举措的资金不断增长,代谢组学和石油行业中质谱的广泛使用,以及加拿大质谱项目的CFI资金。此外,美国食品和药物管理局(FDA)等监管机构正在鼓励使用分析技术,以确保市场上投放的药品符合质量要求。最近,随着油田的增加,美国页岩气和原油产量显著增加,这导致了质谱仪等分析工具的使用随之增加
wsearch软件可以根据分子量预测出分子式,但不能给出分子结构,有没有软件可以直接给出可能的分子结构的。这样分析残片时可以知道是什么,毕竟小的分子量的元素组合也没多少,可能的就更少了。或者网上有没有什么地方可以用分子量检索出可能结构的。例如:质谱中最小的峰为87,那么可能的分子式是什么呢?


