推荐厂家
暂无
暂无
唐访良 朱文(杭州市环境监测中心站 杭州 310007) 摘 要:用活性炭吸附环境空气和废气中的2-丁酮和苯,经二硫化碳解吸后用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定。方法的回收率:2-丁酮为86.2%~104.6%,苯为91.3%~105.7%;变异系数:2-丁酮为2.5%~2.8%,苯为2.5%~3.8%。当采样体积为20L,解吸液体积为2.00mL,进样体积为2μL时,2-丁酮和苯的最低检测浓度分别为0.03mg/m3和0.01mg/m3。 关键词:环境空气和废气 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url] 2-丁酮 苯 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url] DETERMINATION OF 2-BUTANONE AND BENZENE IN AMBIENT AIR AND EXHAUST AIRTANG Fang-liang and ZHU Wen(Hangzhou Environmental Monitoring Centre, Hangzhou 310007,China) Abstract:Sampling of micro-amounta of 2-butanone and benzene in ambient air and exhaust air was carried out by their adsorption on active carbon filled in a sampling tube, and then desorbed with 2.00ml of carbon disulfide. Two μL of the desorbed solution were taken and analyzed by gas chromatography. Satisfactory separation was attained by using PEG-20M column. Retention time method was used in the qualitative analysis and peak height method was used in the quantitative analysis. Mixed standard solutions containing 2-butanone from 0.00 to 64.8mg• L-1 and benzene from 0.00 to 70.4 mg• L-1(in CS2) were used to prepare an external standard curve. RSD’s(n=8) for 2-butanone and for benzene were found to be in the range of 2.5%~2.8% and 2.5%~3.8% respectively. Recoveries found for 2-butanone and for benzene were in the range of 86.2% to 104.6% and 91.3% to 105.7% respectively. The detection limits(S/N=2) were found as 0.03mg• m-3(for 2-butanone and 0.01mg• m-3(for benzene) under the experimental conditions mentioned above and when 20L of sampling volume were taken. Keywords:Gas chromatography 2-Butanone Benzene Ambient air Exhaust air 2-丁酮和苯都是常用的有机溶剂,应用广泛。由于苯有毒有害,是人类公认的致癌物之一,在生产和使用过程中不可避免地会造成对人体的损害和对环境的污染[1]。随着人们环保意识的提高,人们已越来越多的用低毒或无毒溶剂来代替毒性大的溶剂,2-丁酮是常用的替代品之一,如有些胶粘剂所用的溶剂,就有用2-丁酮来代替苯、甲苯、二甲苯作为溶剂的。环境空气和废气中的苯常用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定[2],车间空气中2-丁酮也有用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法进行测定的报道[3],但环境空气和废气中2-丁酮和苯的同时分离和测定还较少报道。本文用活性炭吸附富集环境空气和废气中2-丁酮和苯,经二硫化碳(CS2)解吸后[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定,方法简便、快速,用于实际样品测定,结果满意。1 试验部分1.1主要仪器和试剂 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]-9A[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url](日本岛津公司),具FID检测器,KB-6A型大气采样器(青岛市崂山电子仪器实验所),2L铝箔复合膜软气袋(简称气袋),活性炭吸附采样管(市售,内填0.2g粒度为20~40目的粒状活性炭);苯、甲苯、对-二甲苯、间-二甲苯、邻-二甲苯皆为色谱纯试剂,2-丁酮、丙酮为分析纯试剂;二硫化碳(CS2)为分析纯试剂,经纯化处理后用作溶剂。1.2色谱条件 色谱柱为长2m内径3mm的玻璃柱,内填10%PEG-20M/Shimalite W (NAW)(60~80目);柱温为70℃,汽化室、检测室温度为150℃;载气(N2)流速为50mL/min ,燃气(H2)流速为45 mL/min ,助燃气(A ir)流速为500 mL/min 。进样量为2μL1.3样品的采集和测定 环境空气样品中的2-丁酮和苯的浓度一般较低,常需用活性炭吸附采样管进行富集浓缩,按文献[2]进行环境空气样品的采集,按文献[4]进行污染源废气样品的采集。将上述已采样的活性炭采样管中的活性炭移入10mL具塞比色管中,加2.00mLCS2,轻轻振摇2min,放置20min后,吸取2μL解吸液,进行分离测定。以保留时间定性,以峰高外标法定量。 2 结果与讨论2.1色谱柱的选择 2-丁酮的沸点为79.6℃,苯的沸点为80.1℃,二者沸点相差0.5℃,用文献[2]给出的2.5%DNP+2.5%Bentone-34和PEG-400柱分析2-丁酮和苯,二者不能分离,本文选用PEG-20M柱,2-丁酮和苯能很好分离,且分析样品所需的时间短,如图1所示。2.2干扰试验 选择与2-丁酮、苯经常同时使用或共存的丙酮、甲苯、对-二甲苯、间-二甲苯、邻-二甲苯进行干扰试验(如图1)。从图中可以看出,在选定的色谱条件下,各组分之间能很好分离,不会干扰2-丁酮和苯的分离和定性、定量测定。 图1 2-丁酮和苯与共存物质的分离色谱图 图中 1.溶剂(CS2,0.59分) 2.丙酮(0.74分) 3.2-丁酮(1.19分) 4.苯(1 .56分) 5.甲苯(2.79分) 6.对-二甲苯+间-二甲苯(5.14分) 7.邻-二甲苯(6.74分)2.3 标准曲线及精密度检验 配制2-丁酮浓度为0.00,6.48,13.0,25.9,38.9,51.8,64.8mg/L和苯浓度为0.00,7.04,14.1,28.2,42.2,56.3,70.4mg/L的CS2混合标准系列,在选定的色谱条件下进行测定,线性回归方程和相关系数:2-丁酮,H=31.3C-15.1(C为mg/L ),γ=0.9999;苯,H=45.9C-4.35(C为mg/L),γ=0.9999。以混合标准系列浓度最高点的0.1倍(即2-丁酮浓度为6.48 mg/L、苯浓度为7.04 mg/L)和0.9倍(即2-丁酮浓度为58.3 mg/L、苯浓度为63.4 mg/L)的标准溶液为样品,各重复8次试验, 其变异系数: 0.1倍溶液,2-丁酮和苯分别为2.8%、3.8%; 0.9倍溶液,2-丁酮和苯皆为2.5%。2.4采样效率试验 采用相对比较法来评价采样效率。在2L气袋中用高纯氮气配制了不同浓度的2-丁酮和苯的混合气体样品,串联2支活性炭采样管,第一管连气袋,第二管连大气采样器,如1.2进行样品的采集和测定,结果如表1。表1 采样效率试验测定结果 序号 项 目 第一管测定量(m/μg) 第二管测定量(m/μg) 第一管采样效率( %) 1 2-丁酮 8.18 0.00 100 苯 5.27 0.00 100 2 2-丁酮 70.3 0.00 100 苯 49.0 0.00 100 3 2-丁酮 900 0.00 100 苯 177 0.00 100 结果表明,在上述测定量条件下,第一支采样管的采样效率已达100%,用一支采样管已能满足测定要求。 2.5 方法的检出限按两倍噪声计算的仪器的最小检出量,2-丁酮为0.6ng,苯为0.2ng (进样体积为2μL),当采样体积为20L,解吸液体积为2.00mL时,方法的最低检出浓度:2-丁酮为0.03mg/m3,苯为0.01mg/m3。2.6 样品的测定和回收率用本法测定了环境空气样品和某污染源废气样品,并在解吸液中进行了加标回收试验,结果如表2。 表2 样品测定结果和回收率 样品名称 项 目 样品含量(m/μg) 加标量(m/μg) 测得总量(m/μg) 回收率 (%) 环境空气 2-丁酮 0.00 0.65 0.68 104.6 苯 0.32 0.70 1.06 105.7 废气 2-丁酮 1620 1396 2824 86.2 苯 7.04 6.42 12.9 91.3
如题:如何检测微量丁酮和甲苯的含量请楼主说明是什么样品?
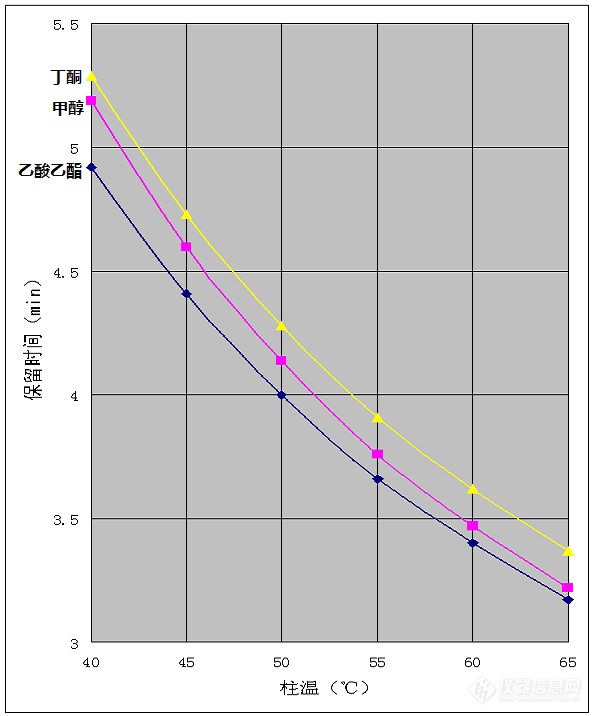
溶剂残留分析是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的重要应用之一,在药品、食品、包装等领域都是必测的项目。常见溶剂中涉及到的检测目标物经常有乙酸乙酯、甲醇、丁酮,以及二甲苯异构体这几项。最近看到 @m3091333、@p3109800、@Insm_c1196d2b 等多人发帖子讨论相关问题,我从原理上进行了一些解释,但终究纸上谈兵,于是找别的实验室要了这几种试剂,用实践检验了一下。首先,如果二甲苯异构体不要求分离,用624柱可以很容易的解决问题,这里就不讨论了。如果要求乙苯、对二甲苯、间二甲苯、邻二甲苯四种异构体分离,用624柱是无法完成的。因为二甲苯异构体色散力差异非常小,只能靠诱导力的差异分离,不同异构体在强极性柱上的极化率不同,乙苯极化率最低,其次是对二甲苯、间二甲苯,邻二甲苯极化率最大,出峰时间也随极化率的增加而延长。而624柱的极性比较弱,不能产生足够的极化作用,特别是对二甲苯与间二甲苯的极化差异非常小,无法实现分离。这个问题是由分子结构决定的,无论怎么调节色谱条件都不能解决。要想解决只能换强极性柱,常见的就是聚乙二醇柱,包括各种wax柱和FFAP柱等。三氟丙基柱也是强极性的,可以分离二甲苯异构体,但是这种柱很少使用。在聚乙二醇类的色谱柱上,乙酸乙酯、甲醇、丁酮三种目标物分离困难,各种类型的聚乙二醇柱选择性略有差异,但这三种物质都是较为接近的,想要分离是不太容易的。但是这三种物质与聚乙二醇固定相之间的作用力存在本质上的差异,因此通过调整柱温条件是可以分离的。下面三幅图是用60米*0.53mm*1um的INNOWAX柱分离乙酸乙酯、甲醇、丁酮的效果,柱温分别是40℃、50℃、60℃。[img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157168864_5041_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157170984_7926_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157172914_736_2204387_3.png!w690x796.jpg[/img]图中很明显,柱温低时甲醇与丁酮出峰时间接近分不开,高温时甲醇与乙酸乙酯出峰时间接近分不开,温度适中时三者可以实现分离。虽然未达到基线分离,但分离度都超过1,用来定量是完全可以的。这是找别人借的一根旧柱子,柱效只有4万塔板,如果是新柱子柱效应该能达到七八万塔板,分离度肯定更高,如果是0.32mm口径的柱子分离就更没问题了。要强调的是,能够实现分离的条件并不是完全靠盲目尝试获得的。我们看一看三种目标物的保留时间随柱温的变化就能发现其中的规律,见下图:[img=,594,716]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022156374904_6999_2204387_3.png!w594x716.jpg[/img]图中可以看出,三种目标物的保留时间都是随温度升高而减小的,但是减小的幅度却并不相同。甲醇的保留时间随温度升高而减小的幅度明显大一些。这是因为甲醇具有羟基,与聚乙二醇固定相的相互作用力以氢键为主,氢键的强度随温度升高而迅速减弱。而乙酸乙酯、丁酮与聚乙二醇固定相的作用力都是以诱导力和取向力为主,这种力是由分子偶极矩决定的,受温度的影响要小一些。甲醇峰位置在乙酸乙酯与丁酮之间,温度升高时保留时间都减小,但甲醇减小更多,于是甲醇与乙酸乙酯靠的更近,与丁酮的分离度提高。温度降低时保留时间都增大,但甲醇增大更多,于是甲醇与丁酮靠的更近,与乙酸乙酯的分离度提高。用其他的柱子,如DB-wax或者FFAP时,各组分之间的相对位置会有差别,甚至有时出峰顺序都会变,但是保留时间随温度变化的这种规律仍然是适用的。所以遇到分不开的情况,一定不要盲目的乱试一通,也不用盲目的换柱子,一定要把问题想明白,有针对性的优化条件。最后要强调的是,这里虽然是以溶剂检测为例讨论了如何只用一根柱子就实现分离,但实际样品很复杂,并不是每次都能通过这种优化实现全部分离目的。所以色谱实验室配备多种不同极性的色谱柱是非常重要的。特别是做复杂样品时,即使谱图上看起来分离不错,最好也能用另外一种柱子进行一次验证,以免实际样品中有干扰物共流出,造成假阳性。






 400-877-2799
400-877-2799
 留言咨询
留言咨询

 400-860-5168转3986
400-860-5168转3986
 留言咨询
留言咨询

 400-860-5168转2141
400-860-5168转2141
 留言咨询
留言咨询