推荐厂家
暂无
暂无
[color=#333333]老师有下面这个标准吗?成分分析中见过这种纤维吗?[/color][color=#333333]FZ/T 50018-2013《蛋白粘胶纤维蛋白质含量[/color][color=#333333]试验方法》?[/color]
如题,肌原纤维蛋白形成凝胶的微观结构用什么观察?光学显微镜能观察吗?
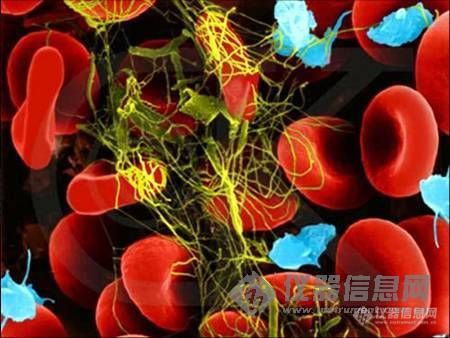
扫描电镜下血液凝块构造(红色为红血球,兰色为血小板,黄色为纤维蛋白)。[img]http://ng1.17img.cn/bbsfiles/images/2005/12/200512071347_11393_1697463_3.jpg[/img][color=blue]Sean:非常感谢楼主一直以来的好图,同时也希望大家踊跃将自己的图片发上来跟大家分享、讨论!![/color]





 400-876-8980
400-876-8980
 留言咨询
留言咨询

 400-860-5168转4421
400-860-5168转4421
 留言咨询
留言咨询

 400-860-5168转5943
400-860-5168转5943
 留言咨询
留言咨询