推荐厂家
暂无
暂无
[size=14px] [/size] [size=14px]黏膜愈合是炎症性肠病(IBD)患者长期缓解和降低手术风险的重要预后指标,未愈合的黏膜会诱发持续性炎症。肠上皮细胞群的适当分化在损伤后黏膜再生中起着重要作用。表达SOX9的标记保留细胞(LRC)已被确定为通过补充LGR5肠道干细胞(ISC)促进上皮修复。另一方面,LRC也被认为是肠内分泌细胞(EEC)的前体细胞,可加剧IBD中的黏膜损伤。因此,干预 LRC-EEC分化轴理论上有利于IBD的黏膜愈合。[/size] [size=14px]大黄是多年生草本植物,自公元前三千年以来在中国一直被用作泻药。大黄的主要化学成分包括蒽醌、蒽酮、蒽烯等。前期作者使用硫酸葡聚糖钠盐(DSS)诱导的IBD模型筛选大黄中的主要成分,发现芦荟大黄素显著缓解结肠炎。芦荟大黄素(1,8-二羟基-3-羟甲基蒽醌)是天然蒽醌衍生物之一,据报道具有抗肿瘤、抗病毒、抗炎、抗菌和保肝药理作用,但其在缓解结肠炎上的具体作用机制与直接靶点尚不清楚。[/size] [size=14px]2024年5月31日,复旦大学药学院沈晓燕、陈道峰团队在ASPB(IF=14.4)发表题为“Aloe emodin promotes mucosal healing by modifying the differentiation fate of enteroendocrine cells via regulating cellular free fatty acid sensitivity”的文章,发现芦荟大黄素可直接拮抗游离脂肪酸受体1(FFAR1)的激活,并阻断AKT介导的FOXO1磷酸化和FOXO1的核输出。然后,FOXO1的核输入相对增加导致SOX9高表达,从而抑制LRC向EEC的过度分化,并保留了更多的SOX9 LRCs,促进结肠炎的黏膜愈合和上皮重建。[/size] [size=14px] [/size] [size=14px]1、筛选大黄中的活性化合物治疗小鼠结肠炎[/size] [size=14px]根据大黄中检测到的成分含量,作者选择五种游离蒽醌类(emodin、aloe emodin、chrysophanol、rhein和physcione)、四种二苯乙烯类化合物(piceatannol、rhapontigenin、desoxyrhapontigenin、rhaponticin),以及sennoside A(大黄中最有效的泻药),采用DSS诱导的结肠炎开展基于药效的筛选,发现芦荟大黄素等部分化合物可有效抑制结肠炎小鼠体重减轻,缓解结肠缩短,抑制促炎细胞因子表达,特别是在芦荟大黄素组中观察到炎症细胞因子最显著的减少。作者结合体重、结肠长度和炎性细胞因子表达,选择了芦荟大黄素进行进一步研究。[/size] [size=14px] [/size] [size=14px]2、芦荟大黄素改善小鼠结肠炎模型的炎症反应[/size] [size=14px]多剂量组口服芦荟大黄素的药效学实验表明,在小鼠模型中DSS诱导的结肠炎发作后,芦荟大黄素治疗促进体重恢复,缓解结肠缩短,改善肠道屏障完整性,缓解炎症细胞浸润和隐窝结构丧失。此外,芦荟大黄素改善血清和组织中促炎细胞因子水平的升高。这些结果表明芦荟大黄素对DSS模型具有剂量依赖性治疗效果,且芦荟大黄素优于5-氨基水杨酸(5-ASA)。此外,作者还评估了芦荟大黄素在TNBS诱导的结肠炎模型中的药效学,同样发现芦荟大黄素在TNSB模型中也表现剂量依赖性缓解。[/size] [size=14px] [/size] [size=14px]3、芦荟大黄素干扰前体细胞向早期EEC的分化[/size] [size=14px]作者取芦荟大黄素处理组和对照组的肠道组织开展RNA-seq检测,GSEA分析显示与芦荟大黄素组相比,对照组的胰腺分泌、内分泌和其他因子调节的钙重吸收和胰岛素分泌基因集富集,表明芦荟大黄素在体内下调肠道分泌细胞相关功能。对选定损伤区域的免疫荧光染色发现芦荟大黄素对EECs(CHGA)数量有显著抑制,而对吸收细胞(CAII)、杯状细胞(MUC2)和簇(COX1)细胞数量没有影响,支持GSEA分析的发现。通过检测EEC转录调节因子在不同阶段的表达,发现芦荟大黄素可能从早期就抑制EEC成熟。此外,CHGA染色和结肠类器官的5-HT水平表明芦荟大黄素抑制了上皮细胞谱系向肠内分泌细胞的分化。此外,芦荟大黄素在所有时期都抑制了EECs标记物的表达。这些数据表明,芦荟大黄素会干扰前体细胞向早期EEC的分化。[/size] [size=14px] [/size] [size=14px]4、SOX9介导的LRC分化阻滞是芦荟大黄素促进黏膜修复所必需的[/size] [size=14px]为了明确芦荟大黄素如何影响上皮细胞分化,作者通过免疫磁珠分选获得小鼠纯化的结肠上皮细胞,测定ISCs分化出的不同上皮细胞的标记基因表达,发现Sox9表达在结肠炎中显著降低,并通过芦荟大黄素治疗得以挽救,而且芦荟大黄素还上调了分选上皮细胞中的SOX9蛋白水平,下调了CHGA蛋白水平。免疫荧光染色显示芦荟大黄素上调损伤区域SOX9细胞的数量,且SOX9细胞数量与CHGA细胞数量均呈显著负相关。高SOX9表达是LRC的特征之一,隐窝纵切片的SOX9染色表明,芦荟大黄素增加了SOX9细胞群。使用激光捕获显微切割分离富含SOX9细胞的区域表明,与SOX9-区域相比,SOX9+区域的转录谱接近 LRC。这些数据表明由芦荟大黄素引起的增加的SOX9细胞是LRC。来自培养的小鼠结肠类器官的数据也表明,芦荟大黄素上调了SOX9 LRC的数量和Sox9的表达。作者还分析了活动性克罗恩病患者的转录组谱发现与非发炎区域相比,发炎区域活检样本中的SOX9 表达显著降低, NEUROG3表达显著增加,临床样本染色还显示,随着炎症的增加,克罗恩病患者结肠隐窝中的SOX9 LRCs显著减少,而NEUROG3 EECs显著增加。先前的单细胞测序数据结果显示,发炎区域的EEC数量高于健康对照组和非发炎区域,而发炎区域的LRC数量低于非发炎区域。此外,SOX9在非发炎区域的EEC中的表达显著高于发炎区域。这些数据表明炎症中SOX9表达水平下调可能会导致LRC向EEC过度分化的趋势。作者采用TNF-α处理类器官以模拟结肠炎症并观察类器官的凋亡,发现芦荟大黄素显著抑制TNF-α诱导的类器官凋亡。此外,芦荟大黄素部分逆转了TNF-α诱导的Sox9表达降低和Neurog3表达增加,而所有芦荟大黄素诱导的作用都被SOX9-CRISPR敲除和JQ-1(作为表观遗传抑制剂可下调SOX9转录)阻断。这些数据证实SOX9介导的LRC分化阻滞是芦荟大黄素促进黏膜修复所必需的。[/size] [size=14px] [/size] [size=14px] [/size] [size=14px]5、FOXO1 是芦荟大黄素上调 SOX9 表达的关键转录因子[/size] [size=14px]作者进一步检测了芦荟大黄素诱导的SOX9表达上调的可能信号通路。使用RcisTarget包鉴定了芦荟大黄素和载体处理的小鼠结肠之间DEGs中富集的转录因子(TF)结合基序,结合JASPAR TFBS和ReMap ChIP-seq数据库进一步鉴定了可能与 SOX9 基因启动子上游 2000 bp序列结合的TF,结合三种分析的预测,芦荟大黄素可能调节21个TF,最终上调 SOX9 表达,进一步发现,在CD环境中,有6个TFs与SOX9表达显著相关,结合备选的TF可能导致SOX9的上调和NEUROG3的下调,确定FOXO1 是最有可能通过芦荟大黄素调节导致SOX9上调的 TF。FOXO1抑制剂(AS1842856)阻断芦荟大黄素对SOX9和NEUROG3表达的调节证明了这一点。使用Jaspar数据库预测表明FOXO1可以与SOX9上游的多个序列结合,DNA pulldown和CHIP-q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]实验均表明FOXO1能够与FOXO1上游的预测序列结合,并可以通过芦荟大黄素增强。总的来说,FOXO1确定为芦荟大黄素上调 SOX9 表达的关键转录因子。[/size] [size=14px] [/size] [size=14px]6、芦荟大黄素抑制 FOXO1 磷酸化促进其核易位[/size] [size=14px]FOXO1活性与其表达丰度、翻译后修饰(主要包括磷酸化和乙酰化)、核细胞质穿梭和亚细胞定位有关。作者通过蛋白质印迹和免疫荧光染色显示芦荟大黄素上调了FOXO1的核易位,然而,芦荟大黄素不影响FOXO1的蛋白质和mRNA丰度。进一步的结果表明,蛋白磷酸酶抑制剂而不是组蛋白脱乙酰酶抑制剂或sirtuin抑制剂阻断了芦荟大黄素对SOX9表达的上调,这表明芦荟大黄素通过影响磷酸化修饰而不是乙酰化来上调SOX9表达。AKT、ERK1/2和CK1α诱导 FOXO1 的磷酸化和核输出。作者发现芦荟大黄素通过影响AKT活性上调SOX9表达。AKT 在三个不同的位点(Thr24、Ser256、Ser319)上直接磷酸化 FOXO1,导致其通过核输出进行转录失活,作者发现芦荟大黄素剂量依赖性地降低AKT诱导的FOXO1磷酸化(Ser256)。AKT 磷酸化的FOXO1与14-3-3伴侣蛋白结合,阻断FOXO1的核易位信号,免疫荧光图像和免疫共沉淀显示芦荟大黄素削弱了FOXO1和14-3-3σ的相互作用。此外,FOXO1-CRISPR ko Caco-2细胞上FOXO1标志的过表达挽救了芦荟大黄素诱导的SOX9高表达。总之,数据表明芦荟大黄素降低了AKT诱导的FOXO1磷酸化,并促进了FOXO1进入细胞核以上调SOX9转录。[/size] [size=14px] [/size] [size=14px]7、芦荟大黄素靶向FFAR1抑制Gβγ/AKT/p-FOXO1通路[/size] [size=14px]根据SuperPred网站结果,结合SYBYL-X软件对接评分(5.0),作者获得了5个高可能性的芦荟大黄素靶点。相关性分析表明只有游离脂肪酸受体1(FFAR1)与SOX9/NEUROG3平衡显著相关。分子对接显示芦荟大黄素被包埋在二聚体之间的残基VAL1094、ASP1092、ARG1095和THR1155周围的口袋中。DARTS和CETSA结果一致地表明芦荟大黄素与FFAR1的结合。亚油酸是FFAR的内源性配体,这可以解释为什么芦荟大黄素会导致KEGG富集的亚油酸途径改变。作者使用了亚油酸和TAK-875(FFAR1的选择性激动剂)确认芦荟大黄素对FFAR1的影响,RT-q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]和Western blot数据显示亚油酸和TAK-875对SOX9/NEUROG3表达水平和磷酸化(Ser256)以及FOXO1的核易位具有与芦荟大黄素相反的作用。体内实验同样表明,TAK-875消除了芦荟大黄素对结肠炎的缓解作用,并逆转了芦荟大黄素对上皮细胞进行分选时Sox9/Neurog3的调节。此外,TAK875阻断芦荟大黄素诱导的p-AKT(Thr308)下调,表明FFAR1通过p-AKT(Thr308)转导信号至FOXO1。据报道,Gα偶联受体激活后释放的Gβγ亚基直接与PI3K相互作用以激活 PI3Kγ/p-AKT(Thr308)信号通路,作者发现FFAR1驱动的SOX9/NEUROG3轴主要由Gβγ调控。总之,FFAR1是芦荟大黄素的靶标,并且激活的FFAR1通过Gβ2γ3/AKT/p-FOXO1信号通路下调SOX9表达,该通路可被芦荟大黄素阻断。[/size] [size=14px]总结[/size] [size=14px]该研究发现来自传统药用植物大黄的活性成分—芦荟大黄素可直接拮抗游离脂肪酸受体1(FFAR1)的激活,并阻断AKT介导的FOXO1磷酸化和FOXO1的核输出,导致SOX9高表达,从而抑制LRC向EEC的过度分化,并保留了更多的SOX9 LRCs,从而促进黏膜愈合,促进上皮重建。[/size]
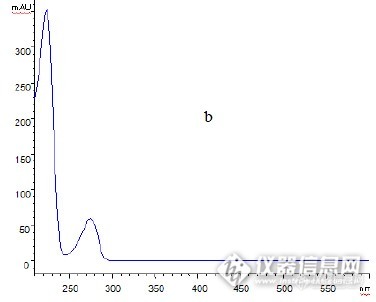
HPLC-DAD分析酸浆中木犀草素及木犀草素-7-β-D-葡萄糖甙成分酸浆(拉丁文名:Physali alkekengi L.)又名红菇娘、挂金灯、戈力、灯笼草、灯笼果、洛神珠、泡泡草、鬼灯等北方称为菇蔫儿、姑娘儿,以果实供食用。化学成分含酸浆苦素A(Physalin A)、酸浆苦素B、酸浆苦素C、木犀草素(Luteolin)及木犀草素-7-β-D-葡萄糖甙。果实含枸橼酸、草酸、维生素C、酸浆红色素(physalien)、酸浆醇(physanol)A,B。花萼含α胡萝卜素、酸浆黄质(physoxanthin)及叶黄素等,种子油的不皂化物中分得多种4α-甲基甾醇,主要为禾本甾醇(gramisterol)和钝叶醇(obtusifoliol)及4种新甾体。此外尚含多种4-脱甲基甾醇,如胆甾醇和24-乙基胆甾醇等。还含有多种三萜3β-一元醇,其中环木菠萝烷醇(cycloartanol)35%,环木菠萝烯醇(cycloartenol)27%、羊毛脂-8-烯-3β-醇(lanost-8-en-3β-ol)。木犀草素(luteolin)是一种天然黄酮类化合物,存在于多种植物中,具有抗炎、抗肿瘤、抗过敏等方面的作用。化学是如下:http://ng1.17img.cn/bbsfiles/images/2016/08/201608311303_607620_2217446_3.jpg目前,国内传统中药有效成分的提取方法普遍存在提取率低、杂质清除率不高、生产周期过长、能耗高、溶剂用量大等缺点。随着中药现代化进程的不断深入,许多现代高新技术不断地被应用到中药有效成分的提取和分离,使得中药有效成分的提取更高效和简便。超声-微波协同萃取技术直接将超声振动与开放式微波两种作用方式相结合,充分利用超声波振动的空化作用以及微波的高能作用,实现了低温常压条件环境下,对固体样品进行快速、高效、可靠的预处理,与常规提取方法相比,超声-微波协同萃取技术具有快速、节能、节省溶剂、污染小等优点。本实验应用超声-微波协同萃取法提取酸浆中的木犀草素及木犀草素-7-β-D-葡萄糖甙,采用高效液相-二极管阵列检测法(HPLC-DAD)测定提取物中木犀草素及木犀草素-7-β-D-葡萄糖甙的含量,药材中二者成分的含量分别为:1.200mg/g 和0.43mg/g,二个峰,木犀草素-7-β-D-葡萄糖甙峰位置分别为:221nm,270nm,木犀草素峰位置分别为:226nm,276nm,由于木犀草素-7-β-D-葡萄糖甙比木犀草素多了一个 β-D-吡喃葡萄糖基团,天麻素二个峰位置都发生了蓝移,样品中二个峰的光谱图与标准品二个峰的光谱图相同,可以进一步确定酸浆中含有木犀草素及木犀草素-7-β-D-葡萄糖甙。主要仪器与试剂主要仪器Agilent1100型四元梯度高效液相色谱仪(美国 Agilent 公司)Agilent TC-C18(ODS)色谱柱(5μm,4.6×250mm,美国 Agilent 公司)CW-2000 超声-微波协同萃取仪(新拓微波溶样测试技术有限公司)DJ-10A 型倾倒式粉碎机(上海隆拓仪器设备有限公司)RE-52AA 型旋转蒸发仪(河南巩义仪器厂)LXJ-IIB 型低速大容量多管离心机(上海安亭科学仪器厂)试剂木犀草素(中检所,含量98%;)木犀草素-7-β-D-葡萄糖甙(中检所,含量98%;)酸浆全草(采于黑龙江)除甲醇、乙腈为色谱纯(国药集团化学试剂有限公司),其余试剂除专门提到外,均为分析醇,实验用水为二次蒸馏水。实验方法供试品溶液的制备 精密称取酸浆粉末1.0g,置于超声-微波萃取仪玻璃容器中,加入50mL70%甲醇,开启超声微波,控制在恒温50℃下提取40min,萃取3次,合并提取液,浓缩至近干,残渣加入甲醇溶解,转移至10mL 量瓶中,加甲醇稀释至刻度,摇匀,过0.45μm 的微孔滤膜,取续滤液,即得。提取条件的考察溶剂的选择:精密称取酸浆粉末1.0g,置于超声-微波萃取仪玻璃容器中,分别用水、70%甲醇、70%乙醇溶液超声-微波协同萃取40min(n=3),萃取3次,合并提取液,浓缩至近干,残渣加入甲醇溶解,转移至10mL 量瓶中,加甲醇稀释至刻度,摇匀,过0.45μm的微孔滤膜,取续滤液,HPLC 测定萃取率。溶剂体积分数的选择:分别用体积分数为40%、50%、60%、70%、80%、90%和纯甲醇溶液超声-微波协同萃取30min(n=3),方法同上。溶剂用量的选择:分别用10mL、20mL、50mL、80mL、100mL70%甲醇提取,方法同上。提取时间的选择:分别用70%甲醇超声-微波协同萃取20min、30min、40min、50min、60min(n=3),方法同上。提取温度的选择:分别在40、45、50、55、60℃下用70%甲醇超声-微波协同萃取40min,方法同上。对照品溶液的制备 分别精密称取常温减压干燥12h 的木犀草素及木犀草素-7-β-D-葡萄糖甙对照品适量,加甲醇配制成木犀草素-7-β-D-葡萄糖甙为200μg/mL、木犀草素为100μg/mL 的混合对照品溶液,冷藏备用。色谱条件 色谱柱:Agilent TC-C18柱(5μm,4.6×250mm);流动相:A-0.1%乙酸水溶液;B-甲醇,线性梯度洗脱:0~30 min,3%~5% B;30~35 min,5%~20%B;35~40min,20%~20%B;检测波长:270nm;流速:1mL/min;柱温:30℃;进样量:20μL。结果与讨论提取条件的优化结果溶剂的优化结果:分别用水、70%甲醇、70%乙醇溶液超声-微波协同萃取30min(n=3),结果表明70%甲醇提取木犀草素-7-β-D-葡萄糖甙的量较高,而木犀草素的量差异不明显,因此选择70%甲醇提取。溶剂体积分数的优化结果:分别用体积分数为40%、50%、60%、70%、80%、90%和纯甲醇溶液超声-微波协同萃取30min(n=3),结果表明,在甲醇体积分数70%时,木犀草素-7-β-D-葡萄糖甙和木犀草素的提取率随着甲醇浓度的增加而增加;但当甲醇体积分数在70%以上时,木犀草素葡萄糖甙的提取率呈现下降趋势,木犀草素没有明显的变化。木犀草素葡萄糖甙属于一种苷,分子量小,极性较大,当甲醇体积分数过高时,溶液极性降低,使得极性较强的木犀草素葡萄糖甙不易溶出,而木犀草素极性相对木犀草素葡萄糖甙小,影响不明显,因此实验选择70%甲醇作为提取溶剂。溶剂用量的优化结果:分别用10mL、20mL、50mL、80mL、100mL70%甲醇提取,结果表明溶剂体积在50mL时木犀草素葡萄糖甙和木犀草素的提取率最高,之后随着溶剂用量的增加,木犀草素葡萄糖甙和木犀草素的提取率趋于稳定,因此溶剂用量选用50mL 进行提取 。提取时间的优化结果:分别用70%甲醇超声-微波协同萃取20min、30min、40min、50min、60min(n=3),结果表明超声-微波协同萃取时间从20~40min的过程中木犀草素葡萄糖甙和木犀草素的提取率逐渐增加;而提取时间超过40min之后,提取率反而逐渐下降。超声-微波协同萃取时间太长,植物中大量细胞细胞破碎,使得大量粘性物质等进入提取液,溶剂杂质增多、粘度增大,影响了有效成分的溶出,有效成分含量反而减少,因此选择提取时间为40min。提取温度的优化结果:分别在40、45、50、55、60℃下用70%甲醇超声-微波协同萃取40min,实验表明,提取温度在50~60℃的范围内,木犀草素葡萄糖甙和木犀草素的提取率没有明显差异,考虑到温度太高容易破坏活性成分,因此选择提取温度为50℃。流动相的考察在实验过程中,流动相首先考察了甲醇-水、乙腈-水等度洗脱对酸浆超声-微波协同萃取样品溶液进行分离,乙腈-水作为流动相时,出峰较快,不能较好地把木犀草素葡萄糖甙和木犀草素与其他杂质成分分离;甲醇-水作为流动相时,出现峰形拖尾现象,分离效果不理想。为改善上述现象,改用0.1%乙酸代替水并采用梯度洗脱,经过反复筛选之后,最终确定流动相组成为 A -0.1%乙酸水溶液, B -甲醇,洗脱程序为0~30 min , 3%~5% B;30~35 min ,5%~20% B ;35~40 min 20%~3% B,木犀草素葡萄糖甙和木犀草素和其他杂质成分能够很好的分离,得到较理想的色谱图。对照品溶液和酸浆萃取样品的HPLC-DAD 分析下图分别显示了在上述的色谱条件下,采用 DAD 进行检测得到的两种混合对照品及酸浆萃取样品的 HPLC 分离色谱图。图1色谱图中木犀草素葡萄糖甙和木犀草素的保留时间分别为18.74min, 26.87min,根据保留时间判断,图2中的 a、b 色谱峰分别初步鉴定为木犀草素葡萄糖甙和木犀草素。图3、4分别显示了混合对照品和酸浆萃取物中保留时间18.74min, 26.87min 的色谱峰进行 DAD 检测后得到的光谱图,木犀草素葡萄糖甙和木犀草素 UV 光谱图形状相似,出现 二个峰,木犀草素葡萄糖甙峰位置分别为:221nm,270nm,木犀草素峰位置分别为:226nm,276nm,由于木犀草素葡萄糖甙比木犀草素多了一个 β-D-吡喃葡萄糖基团,木犀草素葡萄糖甙二个峰位置都发生了蓝移,样品中二个峰的光谱图与
[b]Q:一捻金胶囊的检测,对照品中大黄素甲醚的理论塔板数是?A:13182.473===============================================================【活动内容】1、每个工作日上午10:00左右发布一个关于应用数据库的应用问答题,版友根据题目给出自己理解的答案。2、每个工作日下午15:10公布参考答案。【活动奖励】幸运奖:抽奖软件,当天随机抽取3个或5个回答正确的版友ID号(最后一个ID号,截止至下午15:00),每人奖励[color=#ff0000]2钻石币[/color](抽奖人数≤10,抽取3个版友;抽奖人数>10,抽取5个版友);中奖名单:初心(注册ID:m3170710)千层峰(注册ID:jxyan)yy_0324(注册ID:yy_0324)捌道巴拉巴巴巴(注册ID:v3082413)m3071659(注册ID:m3071659)[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/12/201812061509027023_7191_1610895_3.png!w690x388.jpg[/img][img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/12/201812061509060797_992_1610895_3.png!w690x388.jpg[/img]积分奖励:所有回答正确的版友奖励[color=#ff0000]10个积分[/color](幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次[/b][align=left][color=#ff0000][b]PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。[/b][/color][/align][align=left][color=#ff0000][b] 下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。[/b][/color][/align][align=center]=======================================================================[/align]方法:HPLC基质:药品应用编号:103503化合物:芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚色谱柱:[url=http://www.dikma.com.cn/product/details-229.html]Diamonsil C18 5μm 250 x 4.6mm[/url]样品前处理:对照品溶液:取芦荟大黄素对照品、大黄酸对照品、大黄素对照品、大黄酚对照品、大黄素甲醚对照品适量,精密称定,加甲醇分别制成每1 mL中含芦荟大黄素、大黄酸、大黄素、大黄酚各16 μg、含大黄素甲醚8 μg的混合溶液,摇匀,即得。供试品溶液:取装量差异项下的本品内容物0.8 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,加热回流1小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过。精密量取续滤液5 mL,置烧瓶中,挥去溶剂,加8%盐酸溶液10 mL,超声处理(功率250 W,频率40 kHz)2分钟,再加三氯甲烷10 mL,加热回流1小时,放冷,置分液漏斗中,用少量三氯甲烷洗涤容器,洗涤并入分液漏斗中,分取三氯甲烷液,酸液再用三氯甲烷提取3次,每次10 mL,合并三氯甲烷液,减压回收溶剂至干,残渣加甲醇适量使溶解,转移至10 mL量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液,即得。色谱条件:色谱柱: Diamonsil C18 250*4.6 mm,5 μm (Cat#:99903)流动相: 甲醇:0.1%磷酸溶液=85:15流速: 1 mL/min柱温: 25 ℃检测器: UV 254 nm进样量: 10 μL文章出处:天津应用实验室关键字:一捻金胶囊、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚、Diamonsil C18、HPLC、2015药典摘要:Diamonsil C18检测一捻金胶囊中芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚。图谱:[img]http://www.dikma.com.cn/u/image/2014/12/30/1419931202872254.png[/img][img]http://www.dikma.com.cn/u/image/2014/12/30/1419931205664927.png[/img]






 400-801-9298
400-801-9298
 留言咨询
留言咨询

 留言咨询
留言咨询

 留言咨询
留言咨询