推荐厂家
暂无
暂无


 400-629-8889
400-629-8889
 留言咨询
留言咨询

 400-860-5168转4226
400-860-5168转4226
 留言咨询
留言咨询

 400-860-5168转1372
400-860-5168转1372
 留言咨询
留言咨询


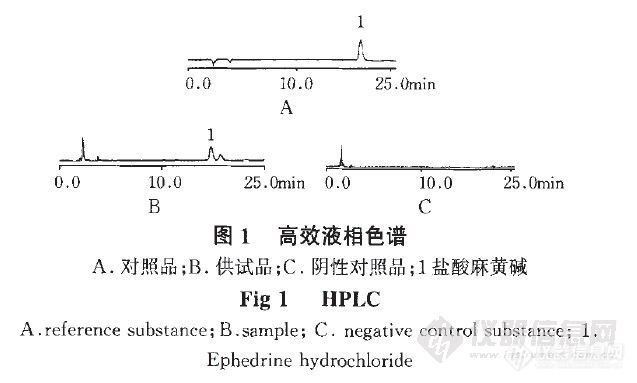
HPLC法测定抗病毒口服液中盐酸麻黄碱的含量 王林丽+,陈亮,付若秋,宋志永(第三军医大学野战外科研究所、大坪医院药剂科,重庆市400042)摘要目的:建立以HPLC法测定抗病毒口服液中盐酸麻黄碱含量的方法。方法:色谱柱为Diamonsil C18(250mm×4.6mm,5um),流动相为乙腈0.1%磷酸(6:94),检测波长为207nm,流速为1.0mL·min一,柱温为室温。结果:盐酸麻黄碱进样量在5.8~29.Otzg范围内与峰面积积分值呈良好线性关系(r=0.999 6);平均加样回收率为98.13%,RSD=1.40%(n=9).结论:本法专属性强、灵敏度高、重现性好,可用于抗病毒口服液的质量控制。关键词 高效液相色谱法;抗病毒口服液;盐酸麻黄碱;含量测定http://ng1.17img.cn/bbsfiles/images/2012/07/201207241912_379472_2355529_3.jpg

[b]2015版《中国药典》规定“抗病毒口服液”要做指纹谱图,要求:[/b]1、与标准图谱的相似度:除6号峰外,计算特征峰1〜 7 号与S峰的相对保留时间,其中1号峰的相对保留时间在规定值的±5%之内,其余特征峰的相对保留时间在规定值的±8%之内。规定值为:0.58(峰 1)、1.0(峰 2 )、2.38 (峰 3 )、2.61(峰 4)、2. 65(峰 5)、4. 94(峰7)。2、4号峰与5号峰的分离度不得低于1.0。[align=center][img=,600,399]https://ng1.17img.cn/bbsfiles/images/2019/10/201910101034387826_2267_932_3.jpg!w690x459.jpg[/img][/align]对此,各药企实验室普遍反映做出来的谱图效果较差,不符合药典要求。月旭科技特此验证本实验,发现采用Ultimate LP-C18色谱柱完全遵从药典方法条件下,可以符合药典要求。测试过程流动相配置流动相A:色谱级乙腈;流动相B:取0.1mL的磷酸置1000mL超纯水中,超声脱气,即得。样品溶液配置对照品溶液:取(R,S)-告依春、连翘苷对照品适量,精密称定,加70%甲醇制成浓度分别为0.02mg/mL、0.06mg/mL的混合溶液,即得;供试品溶液:精密称取抗病毒口服液样品25mL,用乙酸乙酯振摇提取6次,每次25mL,合并乙酸乙酯液,蒸干,残渣加70%甲醇溶解,置10mL量瓶中,加70%甲醇至刻度,摇匀,即得。色谱条件[align=left][/align][align=left]色谱柱:月旭 Ultimate LP-C18(4.6×250mm,5μm)[/align][align=left]流动相洗脱程序:[/align][align=center][img=,600,210]https://ng1.17img.cn/bbsfiles/images/2019/10/201910101034471186_3226_932_3.jpg!w565x198.jpg[/img][/align]柱温:30℃检测波长:236nm流速:1.0mL/min进样体积:10μL实验图谱1)对照溶液[align=center][img=,600,351]https://ng1.17img.cn/bbsfiles/images/2019/10/201910101034561734_6116_932_3.jpg!w690x404.jpg[/img][/align]2)样品[align=center][img=,600,545]https://ng1.17img.cn/bbsfiles/images/2019/10/201910101035030916_2678_932_3.jpg!w690x627.jpg[/img][/align]3)供试品放大图[align=center][img=,600,505]https://ng1.17img.cn/bbsfiles/images/2019/10/201910101035111154_6049_932_3.jpg!w690x581.jpg[/img][/align][b]结论:[/b]相对保留时间均在药典规定范围内;峰4与峰5的分离度为1.34,可以达到药典要求的1.0要求。

[align=center][img=,690,383]https://ng1.17img.cn/bbsfiles/images/2018/08/201808311613081805_7038_932_3.jpg!w690x383.jpg[/img][/align][b]2015版《中国药典》规定“抗病毒口服液”要做指纹谱图,要求:[/b]1、与标准图谱的相似度:除6号峰外,计算特征峰1?7 号与S峰的相对保留时间,其中1号峰的相对保留时间在规定值的±5%之内,其余特征峰的相对保留时间在规定值的±8%之内。规定值为:0.58(峰 1)、1.0(峰 2 )、2.38 (峰 3 )、2.61(峰 4)、2. 65(峰 5)、4. 94(峰7)。 2、4号峰与5号峰的分离度不得低于1.0。[img=,565,198]https://ng1.17img.cn/bbsfiles/images/2018/08/201808311614368614_8978_932_3.jpg!w565x198.jpg[/img]柱温:30℃检测波长:236nm流速:1.0mL/min进样体积:10μL实验图谱1)对照溶液[img=,690,405]https://ng1.17img.cn/bbsfiles/images/2018/08/201808311614588126_9542_932_3.jpg!w690x405.jpg[/img][color=#444444]2)样品[/color][color=#444444][img=,690,627]https://ng1.17img.cn/bbsfiles/images/2018/08/201808311615222159_6424_932_3.jpg!w690x627.jpg[/img][/color][color=#444444][color=#444444]3)供试品放大图[/color][/color][color=#444444][color=#444444][img=,690,581]https://ng1.17img.cn/bbsfiles/images/2018/08/201808311615336422_7415_932_3.jpg!w690x581.jpg[/img][/color][/color][color=#444444][color=#444444][b]结论:[/b][/color][/color][color=#444444][color=#444444]相对保留时间均在药典规定范围内;[/color][/color][color=#444444][color=#444444]峰4与峰5的分离度为1.34,可以达到药典要求的1.0要求。[/color][/color]


