推荐厂家
暂无
暂无



 400-860-5168转1222
400-860-5168转1222
 留言咨询
留言咨询

 400-860-5168转3121
400-860-5168转3121
 留言咨询
留言咨询

 留言咨询
留言咨询



我们有个蛋白质含量约45%-60%的蛋白型固体饮料,公司制定菌落总数的检测标准依据GB/T 4789.21进行检验,可是在我们公司检验菌落总数是合格的但送我们省质检院检验就会检测出十几万的菌落总数?GB/T 4789.21这检验方法我们公司很多产品都在用都没有出现问题,就是蛋白型固体饮料与质检院检测结果相差太大。请教各位高手是不是蛋白型固体饮料做微检时有特殊的处理方法?或者需要注意什么?谢谢
一、菌落总数介绍: 菌落是指细菌在固体培养基上生长繁殖而形成的能被肉眼识别的生长物,它是由数以万计相同的细菌集合而成。当样品被稀释到一定程度,与培养基混合,在一定培养条件下,每个能够生长繁殖的细菌细胞都可以在平板上形成一个可见的菌落。 菌落总数就是指在一定条件下(如需氧情况、营养条件、pH、培养温度和时间等)每克(每毫升)检样所生长出来的细菌菌落总数。按国家标准方法规定,即在需氧情况下,37℃培养48h,能在普通营养琼脂平板上生长的细菌菌落总数,所以厌氧或微需氧菌、有特殊营养要求的以及非嗜中温的细菌,由于现有条件不能满足其生理需求,故难以繁殖生长。因此菌落总数并不表示实际中的所有细菌总数,菌落总数并不能区分其中细菌的种类,所以有时被称为杂菌数,需氧菌数等。 菌落总数测定是用来判定食品被细菌污染的程度及卫生质量,它反映食品在生产过程中是否符合卫生要求,以便对被检样品做出适当的卫生学评价。菌落总数的多少在一定程度上标志着食品卫生质量的优劣。二、检验方法 菌落总数的测定,一般将被检样品制成几个不同的10倍递增稀释液,然后从每个稀释液中分别取出1mL置于灭菌平皿中与营养琼脂培养基混合,在一定温度下,培养一定时间后(一般为48小时),记录每个平皿中形成的菌落数量,依据稀释倍数,计算出每克(或每ml)原始样品中所含细菌菌落总数。 基本操作一般包括:样品的稀释--倾注平皿--培养48小时--计数报告。 国内外菌落总数测定方法基本一致,从检样处理、稀释、倾注平皿到计数报告无何明显不同,只是在某些具体要求方面稍有差别,如有的国家在样品稀释和倾注培养进,对吸管内液体的流速,稀释液的振荡幅度、时间和次数以及放置时间等均作了比较具体的规定。 检验方法参见: GB4789.2-94 《中华人民共和国国家标准 食品卫生微生物学检验 菌落总数测定》 SN0168-92 《中华人民共和国进出口商品检验行业标准 出口食品菌落计数》三、说明(一)样品的处理和稀释: 1.操作方法:以无菌操作取检样25g(或25ml),放于225mL灭菌生理盐水或其他稀释液的灭菌玻璃瓶内(瓶内预置适当数量的玻璃珠)或灭菌乳钵内,经充分振要或研磨制成1:10的均匀稀释液。 固体检样在加入稀释液后,最好置灭菌均质器中以8000~10000r/min的速度处理1min,制成1:10的均匀稀释液。 用1ml灭菌吸管吸取1:10稀释液1ml,沿管壁徐徐注入含有9ml灭菌生理盐水或其他稀释液的试管内,振摇试管混合均匀,制成1:100的稀释液。 另取1ml灭菌吸管,按上项操作顺序,制10倍递增稀释液,如此每递增稀释一次即换用1支1ml灭菌吸管。 2.无菌操作:操作中必须有“无菌操作”的概念,所用玻璃器皿必须是完全灭菌的,不得残留有细菌或抑菌物质。所用剪刀、镊子等器具也必须进行消毒处理。样品如果有包装,应用75%乙醇在包装开口处擦拭后取样。 操作应当在超净工作台或经过消毒处理的无菌室进行。琼脂平板在工作台暴露15分钟,每个平板不得超过15个菌落。 3.采样的代表性:如系固体样品,取样时不应集中一点,宜多采几个部位。固体样品必须经过均质或研磨,液体样品须经过振摇,以获得均匀稀释液。 4.样品稀释误差:为减少样品稀释误差,在连续递次稀释时,每一稀释液应充分振摇,使其均匀,同时每一稀释度应更换一支吸管。 在进行连续稀释时,应将吸管内液体沿管壁流入,勿使吸管尖端伸入稀释液内,以免吸管外部粘附的检液溶于其内。 为减少稀释误差,SN标准采用取10mL稀释液,注入90mL缓冲液中。 5.稀释液:样品稀释液主要是灭菌生理盐水,有的采用磷酸盐缓冲液(或0.1%蛋白胨水),后者对食品已受损伤的细菌细胞有一定的保护作用。如对含盐量较高的食品(如酱油)进行稀释,可以采用灭菌蒸馏水。(二)倾注培养 1.操作方法:根据标准要求或对污染情况的估计,选择2~3个适宜稀释度,分别在制10倍递增稀释的同时,以吸取该稀释度的吸管移取1ml稀释液于灭菌平皿中,每个稀释度做两个平皿。 将凉至46℃营养琼脂培养基注入平皿约15ml,并转动平皿,混合均匀。同时将营养琼脂培养基倾入加有1ml稀释液(不含样品)的灭菌平皿内作空白对照。 待琼脂凝固后,翻转平板,置36±1℃温箱内培养48±2h,取出计算平板内菌落数目,乘以稀释倍数,即得每克(每毫升)样品所含菌落总数。 2.倾注用培养基应在46℃水浴内保温,温度过高会影响细菌生长,过低琼脂易于凝因而不能与菌液充分混匀。如无水浴,应以皮肤感受较热而不烫为宜。 倾注培养基的量规定不一,从12~20ml不等,一般以15ml较为适宜,平板过厚可影响观察,太薄又易于干裂。倾注时,培基底部如有沉淀物,应将底部弃去,以免与菌落混淆而影响计数观察。 3.为使菌落能在平板上均匀分布,检液加入平皿后,应尽快倾注培养基并旋转混匀,可正反两个方向旋转,检样从开始稀释到倾注最后一个平皿所用时间不宜超过[
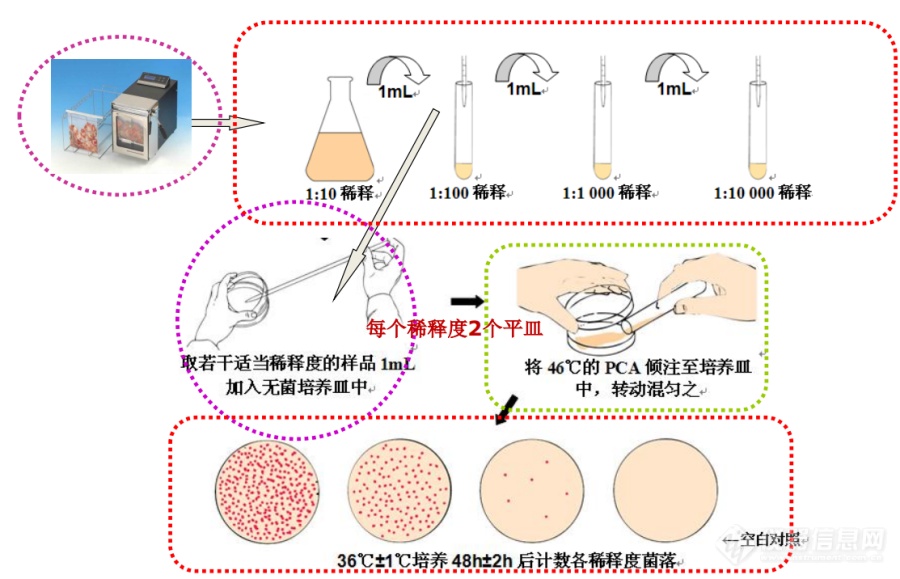
[align=center][font=宋体]菌落总数的检验讨论[/font][/align][align=center][font=宋体] [/font][/align][font=宋体][font=宋体]概念理解[/font] [/font][font=宋体]1、菌落总数英译实为需氧菌平板计数,并不表示实际样品中的所有细菌总数。由于倾注平板法的局限,会有一部分细菌在该实验条件下不生长,故计数结果要比实际值低。 [/font][font=宋体]2、菌落总数并不能区分其中细菌的种类。实际上是把检样中的致病菌、非致病菌、酵母 菌、霉菌都计算在内的微生物杂菌总数。 [/font][font=宋体]3、菌落总数的卫生学意义:用于判定样品受污染的程度、微生物生长存活动态,对样品进行综合卫生评价。反映食品被细菌污染的程度 预测食品耐放程度和时间 估测食品腐败 状况。[/font][font=宋体]菌落:[/font][i][font=宋体]Colony[/font][/i][font=宋体][font=宋体],单个微生物在适固体培养基表面或内部生长繁殖到一定程度;形成肉眼可见有一定细菌群落。[/font] [font=宋体]CFU: [/font][/font][i][font=宋体]Colony Forming Units[/font][/i][font=宋体][font=宋体],菌落形成单位[/font] [/font][font=宋体][font=宋体]鉴于食品的细菌细胞是以单个、成双、链状、葡萄状或成堆的形式存在,因而在平板上出现的菌落可以来源于细胞块,也可以来源于单个细胞,因而平板上所得菌落的数字不应报告活菌数,而应以单位重量、容积或表面积内的菌落数或菌落形成单位([/font][font=宋体]colony forming units,CFU)报告。 [/font][/font][font=宋体] [/font][font=宋体]4.检验步骤直接上图[/font][img=,690,443]https://ng1.17img.cn/bbsfiles/images/2023/08/202308011004578351_4999_6113937_3.png!w690x443.jpg[/img][font=宋体] [/font][font=宋体]5.培养温度: [/font][font=宋体]? 一般食品:36℃±1℃,培养48h ±2h [/font][font=宋体]? 水产品: 30℃±1℃,培养72h ±3h[/font][font=宋体][font=宋体]注意呀:未加工水产品受到海洋和陆地细菌的污染,[/font] [font=宋体]水产品的培养温度,由于其生活环境水温较低,检验时应采用[/font][font=宋体]30℃±1℃。水产品定义见GB 2760或GB2762 [/font][/font][font=宋体]此处并非指水产制品[/font][font=宋体] [/font][font=宋体]6.[/font][font=宋体]操作注意事项:[/font][font=宋体][font=宋体]每个样品从开始稀释到倾注平皿所用的时间不得超过[/font][font=宋体]15min,主要为 [/font][/font][font=宋体][font=宋体]防止细菌增殖和产生片状菌落。(因肠杆菌科繁殖一代所需的时间为[/font] [/font][font=宋体]20min,故选择在15min内) [/font][font=宋体]? 样液与琼脂应充分混合,避免将混合物溅到平皿壁和皿盖上。平皿内 [/font][font=宋体][font=宋体]琼脂凝固后,不要长时间放置,然后倒置培养,可避免菌落蔓延生长。[/font] [/font][font=宋体]? 检样过程中应用稀释剂做空白对照,用以判定稀释液、培养基、平皿或吸管可能存在的污染。应为吸取1mL空白稀释液加入到两个无菌平皿内,可表示为空白对照平皿结果0/0。[/font][font=宋体][color=#000090] [/color][/font][font=宋体][font=宋体]选取菌落数在[/font][font=宋体]30~300CFU之间,无蔓延生长的平板计数 [/font][/font][font=宋体][font=宋体]低于[/font][font=宋体]30的记录具体菌落数,大于300的 可记录为多不可计,每个稀释度采用两个平行的均数。 [/font][/font][font=宋体][font=宋体]有较大片状菌落生长者不宜采用,若片状小于平板一半时且余部均匀分布,则以半个平板菌落数[/font][font=宋体]2倍报告 [/font][/font][font=宋体][font=宋体]无明显界限链状菌落每条单链视为一个菌落[/font] [font=宋体](可采用覆盖方式减少菌落蔓延,如对水产、蜂蜜样品时)[/font][/font][font=宋体] [/font]