推荐厂家
暂无
暂无
 留言咨询
留言咨询
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-805-0826
400-805-0826
 留言咨询
留言咨询
 留言咨询
留言咨询

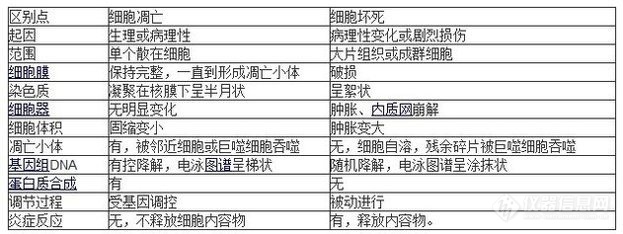


摘要:细胞凋亡与坏死是两种完全不同的细胞凋亡形式,根据死亡细胞在形态学、生物化学和分子生物学上的差别,可以将二者区别开来。细胞凋亡的检测方法有很多,下面介绍几种常用的测定方法。一、细胞凋亡的形态学检测根据凋亡细胞固有的形态特征,人们已经设计了许多不同的细胞凋亡形态学检测方法。1. 光学显微镜和倒置显微镜(1) 未染色细胞:凋亡细胞的体积变小、变形,细胞膜完整但出现发泡现象,细胞凋亡晚期可见凋亡小体。贴壁细胞出现皱缩、变圆、脱落。(2) 染色细胞:常用姬姆萨染色、瑞氏染色等。凋亡细胞的染色质浓缩、边缘化,核膜裂解、染色质分割成块状和凋亡小体等典型的凋亡形态。2. 荧光显微镜和共聚焦激光扫描显微镜一般以细胞核染色质的形态学改变为指标来评判细胞凋亡的进展情况。常用的DNA特异性染料有:HO 33342 (Hoechst 33342),HO 33258 (Hoechst 33258), DAPI。三种染料与 DNA的结合是非嵌入式的,主要结合在DNA的A-T碱基区。紫外光激发时发射明亮的蓝色荧光。Hoechst是与DNA特异结合的活性染料,储存液用蒸馏水配成1mg/ml的浓度,使用时用PBS稀释成终浓度为2~5mg/ml。DAPI为半通透性,用于常规固定细胞的染色。储存液用蒸馏水配成1mg/ml的浓度,使用终浓度一般为0.5 ~1mg/ml。结果评判:细胞凋亡过程中细胞核染色质的形态学改变分为三期:Ⅰ期的细胞核呈波纹状(rippled)或呈折缝样(creased),部分染色质出现浓缩状态;Ⅱa期细胞核的染色质高度凝聚、边缘化;Ⅱb期的细胞核裂解为碎块,产生凋亡小体(图1)。 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376278_small.jpg3 透射电子显微镜观察结果评判:凋亡细胞体积变小,细胞质浓缩。凋亡Ⅰ期(pro-apoptosis nuclei)的细胞核内染色质高度盘绕,出现许多称为气穴现象(cavitations)的空泡结构(图2);Ⅱa期细胞核的染色质高度凝聚、边缘化;细胞凋亡的晚期,细胞核裂解为碎块,产生凋亡小体。 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376295_small.jpg二、磷脂酰丝氨酸外翻分析(Annexin V法)磷脂酰丝氨酸(Phosphatidylserine, PS)正常位于细胞膜的内侧,但在细胞凋亡的早期,PS可从细胞膜的内侧翻转到细胞膜的表面,暴露在细胞外环境中(图3)。Annexin-V是一种分子量为35~36KD的Ca2+依赖性磷脂结合蛋白,能与PS高亲和力特异性结合。将Annexin-V进行荧光素(FITC、PE)或biotin标记,以标记了的Annexin-V作为荧光探针,利用流式细胞仪或荧光显微镜可检测细胞凋亡的发生。碘化丙啶(propidine iodide, PI)是一种核酸染料,它不能透过完整的细胞膜,但在凋亡中晚期的细胞和死细胞,PI能够透过细胞膜而使细胞核红染。因此将Annexin-V与PI匹配使用,就可以将凋亡早晚期的细胞以及死细胞区分开来。http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376296_small.jpg方法1. 悬浮细胞的染色:将正常培养和诱导凋亡的悬浮细胞(0.5~1×106)用PBS洗2次,加入100 ul Binding Buffer和FITC标记的Annexin-V(20ug/ml)10 ul,室温避光30 min,再加入PI(50 ug/ml)5 ul,避光反应5 min后,加入400 ul Binding Buffer,立即用FACScan进行流式细胞术定量检测(一般不超过1 h), 同时以不加AnnexinV-FITC及PI的一管作为阴性对照。2. 贴壁培养的细胞染色:先用0.25%的胰酶消化,洗涤、染色和分析同悬浮细胞。3. 爬片细胞染色:同上,最后用荧光显微镜和共聚焦激光扫描显微镜进行观察。结果 http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376298_small.jpg http://img.dxycdn.com/trademd/upload/userfiles/image/2013/08/A1376376300_small.jpg
一、实验目的1、掌屋凋亡细胞的形态特征 2、学会用荧光探针对细胞进行双标记来检测正常活细胞、凋亡细胞和坏死细胞的方法二、实验原理 细胞死亡根据其性质、起源及生物学意义区分为凋亡和坏死两种不同类型。凋亡普遍存在于生命界,在生物个体和生存中起着非常重要的作用。它是细胞在一定生理条件下一系列顺序发生事件的组合,是细胞遵循一定规律自己结束生命的自主控制过程。细胞凋亡具有可鉴别的形态学和生物化学特征。在形态上可见凋亡细胞与周围细胞脱离接触,细胞变园,细胞膜向内皱缩、胞浆浓缩、内质网扩张、细胞核固缩破裂呈团块状或新月状分布、内质网和细胞膜进一步融合将细胞分成多个完整包裹的凋亡小体,凋亡小体最后被吞噬细胞吞噬消化。在凋亡过程中细胞内容物并不释放到细胞外,不会影响其它细胞,因而不引起炎症反应。在生物化学上,多数细胞凋亡的过程中,内源性核酸内切酶活化,活性增加。核DNA随机地在核小体的连接部位被酶切断,降解为180-200bp或它的整倍数的各种片断。如果对核DNA进行琼脂糖电泳,可显示以180-200bp为基数的DNA ladder(梯状带纹)的特征。相比之下,坏死是细胞处于剧烈损伤条件下发生的细胞死亡。细胞在坏死早期即丧失质膜完整性,各种细胞器膨胀,进而质膜崩解释放出其中的内容物,引起炎症反应,坏死过程中细胞核DNA虽也降解,但由于存在各种长度不等的DNA片断,不能形成梯状带纹,而呈弥散状。一些温和的损伤刺激及一些抗肿瘤药物可诱导细胞凋亡,通常这些因素在诱导凋亡的同时,也可产生细胞坏死,这取决于损伤的剧烈程度和细胞本身对刺激的敏感程度。三尖杉酯碱(HT)是我国自行研制的一种对急性粒细胞白血病,急性单核白血病等有良好疗效的抗肿瘤药物。研究表明HT在0.02~5μg/ml范围内作用2小时,即可诱导HL-60细胞凋亡,并表现出典型的凋亡特征。本实验用1μg/ml HT在体外诱导培养的HL-60细胞发生凋亡,同时也有少数细胞发生坏死。用Hoechst33342和碘化丙啶(propidium iodide,PI)对细胞进行双重染色,可以区别凋亡、坏死及正常细胞。细胞膜是一选择性的生物膜,一般的生物染料如PI等不能穿过质膜。当细胞坏死时,质膜不完整,PI就进入细胞内部,它可嵌入到DNA或RNA中,使坏死细胞着色,凋亡细胞和活细胞不着色。而一些活细胞染料由于为亲脂性物质,可跨膜进入活细胞,因而可进行活细胞染色。Hoechst33342是一种活性荧光染料且毒性较弱,它是双苯并咪唑的一种衍生物。与DNA特异结合(主要结合于A-T)碱基区),显示凋亡细胞和活细胞。凡是看到有凋亡小体的细胞都是凋亡细胞。三、实验用品1、试剂:三尖杉酯碱(HT),300μg/ml,100mmol/L Tris-HCl(pH7.5),5mol/L EDTA缓冲液、碱性裂解液:0.2mol/L NaOH, 1%SDS、醋酸钠:3mol/L KAc(pH4.8);异丙醇;70%乙醇;溴酚蓝,蔗糖指示剂。TBE电泳缓冲液,1%琼脂糖,溴乙锭。PI母液:500μg/ml;Ho33342母液:2mmol/L。 2、仪器设备:荧光显微镜,电泳仪,电泳槽,微量加样器(1ml,100μl)0.5、1.5ml离心管,载玻片,盖玻片。四、实验材料人早幼粒白血病HL-60细胞,用含10%小牛血清的RPMI1640培养基在37℃,5%CO2条件下培养。五、方法步骤 1、三尖杉酯碱诱发HL-60细胞凋亡 (1)实验前约24小时,接种两瓶HL-60细胞,标记①、②,每瓶含约6ml培养液,置37℃,5%CO2培养箱培养。 (2)实验前约2.5小时,当细胞密度达到70%,①号瓶加入三尖杉酯碱200μl,使终浓度为1μg/ml,②号瓶中加入同等量PBS(pH7.4)作对照。共同放入培养箱中继续培养2.5小时。2、Ho33342和PI双重染色鉴别三种细胞 (1)染色:将瓶中的细胞摇匀取200μl于1.5ml的离心管中,加入Ho33342母液2μl,PI 20μl,染色15分钟。 (2)滴片:取一载玻片用双面胶围成一小室,从离心管中各取以上染色后的细胞悬液10μl,加入小室内盖上盖玻片,荧光镜下用紫外激发光,高倍镜下观察,区别三种细胞,并注意三者比例。六、注意事项1、诱导培养HL-60细胞时间要准确; 2、荧光显微镜下观察细胞时,由于荧光易碎灭,观察时要尽量快。
肝癌是全球第3大癌症死亡原因,其中肝细胞癌约占所有肝癌类型的80%[1]。据世界卫生组织统计,每年因肝细胞癌死亡的人数高达83万例,且其发病率和死亡率仍呈现上升趋势,严重损害人类生命健康[2]。在慢性肝病的基础上,基因突变、表观遗传变化、信号通路失调和血管生成异常等分子机制相互作用,共同推动慢性肝病向肝细胞癌过程的发展[3]。目前肝细胞癌治疗的一线药物主要是索拉菲尼、仑伐替尼等靶向药及阿替利珠单抗、贝伐珠单抗等免疫治疗药物[4]。然而,靶向药及免疫治疗药的耐药性和不良反应导致肝细胞癌的5年生存率仍然不高。因此,亟需寻找安全性高、不良反应少的治疗药物,为肝细胞癌患者提供更有效、安全的治疗选择。 近年来,随着对肝细胞癌研究的不断深入,自噬在肝细胞癌中的作用逐渐被关注。在肝细胞癌的发展过程中,自噬一方面通过维持细胞内稳态来抑制肿瘤起始,另一方面通过影响信号通路的效应因子来抑制早期肝细胞癌的进程[5]。自噬受到多种机制的严格调控和影响,涉及自噬的几条重要信号通路有Wnt/β-catenin、丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)、磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)/蛋白激酶B(protein kinase B,Akt)/哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)、p53通路等[6],这些通路在肝细胞癌中异常激活,参与肝癌细胞的增殖、凋亡和自噬等生物学行为。研究表明,mTOR通路在自噬调控机制中发挥至关重要的作用[7],mTOR是自噬的负性调控因子,可以与UNC-51样激酶1(Unc-51 like autophagy activating kinase 1,ULK1)的丝氨酸结合抑制自噬的启动过程,也可以通过磷酸化使自噬调节复合物失活影响自噬小体的发生,磷酸化自噬相关蛋白14(autophagy-related protein 14,Atg14)、自噬和Beclin-1调节器1(activating molecule in beclin-1 regulated autophagy protein 1,AMBRA1)和核受体结合因子2(nuclear receptor binding factor 2,NRBF2)直接调节自噬的成核步骤[8]。因此,针对自噬及其机制开展治疗可能是肝细胞癌的有效对抗策略。 地榆为蔷薇科植物地榆Sanguisorba officinalis L.的干燥根,具有凉血止血、解毒敛疮的功效。地榆皂苷II是从地榆中提取的一种三萜皂苷类化合物,现代药理学研究发现,地榆皂苷II不仅具有抗炎、抗氧化、免疫调节的药理作用,同时具有广泛的抗肿瘤活性[9-11],能通过多种途径抑制多种癌症的发生和发展,其机制可能与阻滞细胞周期、促进细胞凋亡和细胞自噬有关[12-15]。课题组前期研究发现,地榆皂苷II能够抑制小鼠肝细胞癌的发展[15]。然而,地榆皂苷II是否能通过影响Akt/mTOR通路诱导凋亡和自噬抑制肝细胞癌尚不明确。本研究中选择人肝癌HepG2细胞和小鼠肝癌Hepa1-6细胞作为研究对象,探究地榆皂苷II对肝癌细胞增殖、自噬和凋亡的影响,探讨地榆皂苷II在抗肝细胞癌方面的潜在作用机制,为将来用于临床治疗提供数据支持。 1 材料 1.1 细胞 HepG2细胞购自中国科学院上海细胞生物学研究所,Hepa1-6细胞购自上海富衡生物科技有限公司。 1.2 药品与试剂 地榆皂苷II(批号MUST-11051204,质量分数≥98%)购自上海源叶生物科技有限公司;PVDF膜(批号IPVH00010)购自美国Sigma公司;青霉素-链霉素(批号S11JV)购自上海源培生物科技股份有限公司;DMEM培养基(批号C11995500BT)、胎牛血清(批号A3160801)购自美国Gibco公司;PBS(批号WHB823K091)购自武汉普诺赛生命科技有限公司;0.25%胰酶消化液(批号C0203)、RIPA组织/细胞裂解液(批号P0013C)、蛋白酶抑制剂混合物(批号P1050-1)、磷酸酶抑制剂混合物(批号P1050-2)、EdU-555细胞增殖检测试剂盒(批号C0075S)购自上海碧云天生物技术有限公司;CCK-8试剂盒(批号A311-02)、BCA蛋白浓度测定试剂盒(批号E112-01)、高敏型ECL化学发光检测试剂盒(批号E412-01)、相对分子质量为1.8×105的蛋白marker(批号MP-102AA)购自南京诺唯赞生物科技股份有限公司;一抗稀释液(批号G2025)、二抗稀释液(批号G2009)、高相对分子质量marker(批号26625)购自武汉赛维尔生物科技有限公司;7.5% PAGE凝胶快速制备试剂盒(批号PG111)、10% PAGE凝胶快速制备试剂盒(批号PG112)、12.5% PAGE凝胶快速制备试剂盒(批号PG113)购自上海雅酶生物医药科技有限公司;β-actin、Beclin1抗体(批号分别为20536-1-AP、11306-1-AP)购自美国Proteintech公司;B淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)、p62抗体(批号分别为ab196495、ab56416)购自英国Abcam公司;Bcl-2相关X蛋白(Bcl-2 associated X protein,Bax)、半胱氨酸天冬氨酸蛋白酶-3(cystein-asparate protease-3,Caspase-3)、Caspase-8、cleaved Caspase-3、Akt、p-Akt、mTOR、p-mTOR抗体(批号分别为5023T、9662S、4790T、9664T、4685S、4060T、2972S、5536T)购自美国CST公司;甲醇(批号10014118)购自国药集团化学试剂有限公司;山羊抗兔二抗(批号RS0002)购自美国ImmunoWay公司;Annexin V-FITC染色液(批号E-CK-A211)购自武汉伊莱瑞特生物科技股份有限公司。 1.3 仪器 AL104型电子分析天平(瑞士梅特勒-托利多有限公司);HH-S型恒温水浴锅(北京市永光明医疗仪器厂);CKX53型倒置生物显微镜、IX73倒置荧光显微镜(日本Olympus公司);3111型CO2培养箱、Multiskan Go-1510型全波长酶标仪(美国Thermo Fisher Scientific公司);Centrifuge 5424R型微量离心机(德国Eppendorf公司);SDS PAGE凝胶电泳及转膜电泳仪(美国Bio-Rad公司);BETS-M5型转移微型翘板摇床(海门市其林贝尔仪器制造有限公司);XH-C型涡旋混合器(金坛市医疗仪器厂);MINI-4K型微型离心机(杭州米欧仪器有限公司);5200型全自动化学发光图像分析系统(上海天能科技有限公司);CytoFLEX流式细胞仪(美国贝克曼库尔特有限公司);ThermoCell恒温金属浴(杭州博日科技股份有限公司)。 2 方法 2.1 CCK-8实验 将HepG2和Hepa1-6细胞分别以1×105个/mL接种于96孔板中,贴壁生长24 h,设置对照组、不同剂量地榆皂苷II组,对照组仅加入培养基,其余各组分别加入5、10、15、20、30、40、60、80、100 μmol/L相应药物,继续培养24 h,用CCK-8试剂盒测定各组吸光度(A)值,计算细胞存活率。 细胞存活率=(A实验-A空白)/(A对照-A空白) 2.2 EdU实验 将HepG2和Hepa1-6细胞分别以1×105个/mL接种于96孔板中,贴壁生长24 h,设置对照组和地榆皂苷II(10、20、40 μmol/L)组,给药组给予相应药物,对照组仅加入培养基,继续培养24 h。将EdU稀释到2×EdU工作液(20 μmol/L),预热后等体积加入96孔板中,孵育细胞2 h后去除培养液,加入100 μL固定液(4%多聚甲醛),孵育10 min后去除固定液,用100 μL洗涤液洗涤细胞3次后每孔加入100 μL通透液(含0.3% Triton X-100的PBS),室温孵育15 min。去除通透液,每孔用1 mL洗涤液洗涤细胞2次,每次5 min。参考说明书配制Click反应液。每孔加入50 μL Click反应液,轻轻摇晃培养板后室温避光孵育30 min。洗涤液洗涤3次,吸除洗涤液后,每孔加Hoechst 33342溶液100 μL,室温避光孵育10 min。用洗涤液洗涤3次,每次3~5 min,随后进行荧光检测。 2.3 细胞凋亡检测 将HepG2和Hepa1-6细胞分别以1×105个/mL接种于6孔板中,贴壁生长24 h,设置对照组和地榆皂苷II(10、20、40 μmol/L)组,给药组给予相应药物,对照组仅加入培养基,继续培养24 h。用胰酶消化细胞,300×g离心5 min,弃上清,收集细胞,PBS洗涤,轻轻重悬细胞,300×g离心5 min,弃上清。用PBS洗涤细胞,离心后弃上清,加入Annexin V Binding Buffer重悬细胞。细胞悬液中加入Annexin V-FITC Reagent和5 μL的碘化丙啶(PI),轻柔涡旋混匀后,室温避光孵育15~20 min,立即上机检测。 2.4 Western blotting检测相关蛋白表达 将HepG2和Hepa1-6细胞分别以1×105个/mL接种于6孔板中,贴壁生长24 h,设置对照组和地榆皂苷II(10、20、40 μmol/L)组,给药组给予相应药物,对照组仅加入培养基,继续培养24 h。加入RIPA中强度缓冲液裂解后收集细胞,使用BCA蛋白定量试剂盒检测蛋白浓度。蛋白样品经凝胶电泳,转至PVDF膜,加入5%脱脂奶粉,封闭1.5 h,加入一抗,4 ℃孵育过夜;洗膜3次后加入二抗,4 ℃孵育1.5 h;最后使用ECL化学发光检测试剂盒,用化学发光图像分析系统显影。 2.5 统计学分析 采用GraphPad Prism 9统计软件对实验数据进统计学分析,计量资料以表示,多组间比较采用单因素方差分析(One-way ANOVA)。 3 结果 3.1 地榆皂苷II对HepG2和Hepa1-6肝癌细胞增殖的影响 如图1所示,与对照组比较,随着地榆皂苷II浓度的升高,HepG2和Hepa1-6肝癌细胞的存活率明显降低,且呈剂量相关性。经GraphPad Prism 9软件分析,地榆皂苷II对HepG2、Hepa1-6细胞的IC50值分别为26.94、26.18 μmol/L,因此以10、20、40 μmol/L作为后续地榆皂苷II的给药剂量。 图片 3.2 地榆皂苷II对HepG2和Hepa1-6肝癌细胞增殖的影响 EdU-555阳性表示细胞正处于增殖状态,Hoechst33342阳性指示细胞为活细胞,EdU-555/Hoechst33342表示细胞的增殖率。如图2所示,与对照组比较,地榆皂苷II给药后HepG2和Hepa1-6细胞的EdU-555/Hoechst33342值明显降低(P<0.05、0.001),表明地榆皂苷II能够抑制肝癌细胞的增殖。 图片 3.3 地榆皂苷II对HepG2和Hepa1-6肝癌细胞凋亡的影响 如图3所示,与对照组比较,地榆皂苷II给药组HepG2和Hepa1-6细胞凋亡率显著升高(P<0.01、0.001)。凋亡蛋白(包括调控凋亡的激活因子和执行凋亡的效应因子)参与细胞凋亡的过程。采用Western blotting检测地榆皂苷II对HepG2细胞和Hepa1-6细胞凋亡相关蛋白表达的影响,如图4所示,与对照组比较,地榆皂苷II给药组Caspase-3、Caspase-8、Caspase-9、Bcl-2蛋白表达量显著降低(P<0.05、0.01、0.001),cleaved Caspase-3、Bax蛋白表达量显著升高(P<0.05、0.01)。以上结果说明地榆皂苷II促进HepG2和Hepa1-6细胞的凋亡。 图片 图片 3.4 地榆皂苷II对HepG2和Hepa1-6肝癌细胞自噬的影响 采用Western blotting检测细胞中代表自噬的核心蛋白LC3II、LC3Ⅰ、Beclin1、p62表达量,如图5所示,与对照组比较,地榆皂苷II给药组LC3Ⅱ/LC3Ⅰ值明显升高(P<0.05、0.01、0.001),Beclin1蛋白表达量上升(P<0.05、0.01),p62蛋白表达量明显下降(P<0.05、0.01),表明地榆皂苷II促进HepG2和Hepa1-6肝癌细胞的自噬。 图片 3.5 地榆皂苷II对HepG2和Hepa1-6细胞中Akt/mTOR信号通路蛋白表达的影响 采用Western blotting检测地榆皂苷II给药后Akt/mTOR信号通路蛋白表达量,如图6所示,与对照组比较,地榆皂苷II给药组p-Akt/Akt、p-mTOR/mTOR值明显下降(P<0.05、0.01、0.001),表明地榆皂苷II能够抑制Akt/mTOR信号通路。 图片 4 讨论 肝细胞癌具有高发病率、高病死率的特点,虽然目前肝细胞癌研究备受关注,但其5年生存率仍为14.1%[16]。因此,迫切需要发现新的治疗策略和候选药物。近年来,地榆皂苷II在抗肿瘤方面的研究不断深入,研究发现地榆皂苷II抑制肿瘤与细胞自噬和凋亡存在紧密的关联,地榆皂苷II可通过诱导细胞凋亡来显著抑制乳腺癌MDA-MB-435细胞和胃癌BGC-823细胞的增殖[14-15],诱导自噬显著抑制结直肠癌细胞增殖[17]。课题组既往研究证明,地榆皂苷II可在体内抑制肝细胞癌,其机制可能与抑制表皮生长因子受体(epidermal growth factor receptor,EGFR)信号通路有关[15]。然而,目前关于地榆皂苷II是否通过自噬和凋亡抑制肝细胞癌及其机制尚不明确。因此,本研究利用体外实验对地榆皂苷II刺激后肝癌细胞的增殖、自噬、凋亡及相关机制进行探究,结果表明,地榆皂苷II能抑制肝癌细胞的增殖,促进肝癌细胞的凋亡和自噬,其机制与抑制Akt/mTOR通路有关。 自噬又被称为II型程序性死亡,负责真核生物细胞质中细胞器、蛋白质和大分子的降解和回收。细胞中降解和回收的底物被吞噬后形成自噬体,自噬体与溶酶体结合形成自噬酶体最后降解。本研究检测了自噬中具有代表性的LC3、p62和Beclin1蛋白。Beclin1蛋白是一种自噬启动子,帮助自噬过程中囊泡的形成[18],地榆皂苷II作用于肝癌细胞后,Beclin1蛋白表达量上升,促进自噬启动,囊泡形成增多,从而自噬水平升高。在自噬形成时,LC3I通过泛素激活酶E1和泛素结合酶E2与磷脂酰乙醇胺偶联,生成LC3II,LC3II存在于自噬体的表面,负责膜的融合和选择性降解过程[19],p62在自噬体表面与LC3II相互作用后包裹进自噬体降解,与LC3II共同调节选择性降解过程[20]。地榆皂苷II给药后LC3II/LC3I值增高,p62蛋白表达量下降,促进自噬过程中自噬囊泡的融合和降解,进而促进自噬。Beclin1是自噬过程中的核心因子,已有研究证明Beclin1可以与抗凋亡因子Bcl-2相互作用,从而对凋亡过程产生影响[21]。细胞凋亡是一种生理性或病理性的程序性的死亡过程,近年来通过诱导促进癌细胞的凋亡来控制癌症一直是抗肿瘤的热点。Caspase级联反应是细胞凋亡过程的关键步骤,其启动受到抗凋亡因子和促凋亡因子Bcl-2和Bax的调节。在Caspase级联反应中,启动性Caspase包括Caspase-8、Caspase-9被激活后调控下游执行性Caspase如Caspase-3进而引起凋亡反应[22-24]。地榆皂苷II作用于肝癌细胞后,细胞中的Bcl-2蛋白表达量减少,Bax蛋白表达量增多,Bax蛋白在线粒体表面形成孔道,释放细胞色素C,引发Caspase级联反应,Caspase-8、Caspase-9激活进而诱导下游的Caspase-3活化为cleaved Caspase-3,切割下游多种底物,促进细胞凋亡典型形态变化。 Akt/mTOR信号通路在正常细胞生理过程中发挥关键作用,同时在多种癌症中,该通路的异常激活对自噬、细胞凋亡、化疗耐药性及转移过程产生重要影响[25]。诸多研究证据表明,Akt/mTOR途径是调控癌症细胞自噬反应的核心通路[26-28]。地榆皂苷II作用于肝癌细胞后,Akt和mTOR蛋白的磷酸化水平显著下降,Akt/mTOR信号通路被抑制,激活肝癌细胞凋亡和自噬,抑制肝癌细胞的增殖(图7,由Figdraw绘制)。 图片 上述体外研究结果初步解析了地榆皂苷II抑制肝细胞癌的机制,即地榆皂苷II通过抑制Akt/mTOR信号通路诱导肝癌细胞的凋亡和自噬,抑制肝癌细胞增殖,为地榆皂苷II在肝细胞癌治疗的药物研究开发中提供了药理学证据。