推荐厂家
暂无
暂无
 留言咨询
留言咨询
 留言咨询
留言咨询
 留言咨询
留言咨询
 400-801-8117
400-801-8117
 留言咨询
留言咨询
 400-807-5250
400-807-5250
 留言咨询
留言咨询

 400-807-5250
400-807-5250
 留言咨询
留言咨询

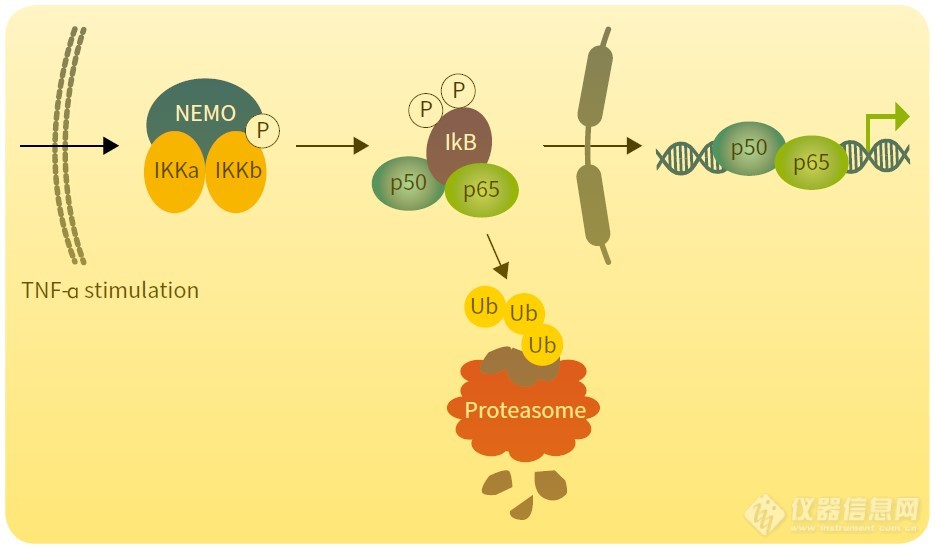




在基因表达研究中,研究者比较注意选择合适的表达载体和宿主系统,而往往忽视基因本身是否与载体和宿主系统为最佳匹配这样一个实质性问题。基因的最佳化表达可以通过对基因的重新设计和合成来实现,如消除稀有密码子而利用最佳化密码子,二级结构最小化,调整GC含量等。以下就密码子最佳化、翻译终止效率和真核细胞中异源蛋白表达的问题加以说明。密码子最佳化(codon optimization)遗传密码有64种,但是绝大多数生物倾向于利用这些密码子中的一部分。那些被最频繁利用的称为最佳密码子(optimal codons),那些不被经常利用的称为稀有或利用率低的密码子(rare or low-usage codons)。实际上用做蛋白表达或生产的每种生物(包括大肠杆菌,酵母 ,哺乳动物细胞,Pichia,植物细胞和昆虫细胞)都表现出某种程度的密码子利用的差异或偏爱。大肠杆菌、酵母 、果蝇、灵长类等每种生物都有独特的8个密码子极少被利用。有趣的是,灵长类和酵母 有6个同样的利用率低的密码子。大肠杆菌、酵母 和果蝇中编码丰度高的蛋白质的基因明显避免低利用率的密码子。因此,重组蛋白的表达可能受密码子利用的影响(尤其在异源表达系统中)的事实并不很奇怪。你的基因利用的密码子可能不是你正在利用的蛋白生产系统进行高水平表达所偏爱的密码子,这种情况是可能的。利用偏爱密码子(preferred codons)并避免利用率低的或稀有的密码子可以合成基因,基因的这种重新设计叫密码子最佳化。在同源表达系统中,同较低水平表达的基因相比,较高表达的基因可能有很不同的密码子偏爱。通过对密码子利用的归类分析,人们可以真正预测任何基因在酵母 中的表达水平。在诸如Zea mays的其他生物中,大量高表达基因强烈偏爱以G或C结尾的密码子。而且,在Dictyostelium中,同低水平表达的基因比较,高表达基因有较大数目的偏爱密码子。在大肠杆菌中表达哺乳动物基因是不可预测和具有挑战的。例如直到最近才实现了人血红蛋白的过表达。为了达到血红蛋白的好的表达水平,Alpha-球蛋白cDNA不得不用大肠杆菌偏爱的密码子进行重新合成。在异源宿主中实现象血红蛋白这样复杂的蛋白质的过表达可能需要最佳化密码子,这些研究者为此提供了令人信服的资料。成簇的低利用率的密码子抑制了核糖体的运动,这是基因不能以合适水平表达的一个明显机制。核糖体翻译由九个密码子组成的信使(含几个低利用率密码子或全部为低利用率密码子)时的运动速度要比翻译不含低利用率密码子的同样长的信使的速度慢。即使低利用率密码子簇位于3'端,信使最后也会被核糖体”拥挤”而损害,核糖体又回到5'端。3'端低利用率密码子簇的抑制效应可以和全部信使都由低利用率密码子组成的抑制效应一样大。如果低利用率密码子簇位于5'端,其效应是起始核糖体数目的全面减少,导致蛋白合成中信使的低效率。散在分布的稀有密码子对翻译的效应还未很好地研究,但是有证据表明这种情况的确对翻译效率有负面效应。其他因素也可以影响蛋白表达,包括使mRNA去稳定的序列。重新设计合成基因可以去除或改变这些序列,导致高水平表达。消除稀有密码子、去除任何去稳定序列和利用最佳密码子的基因的重新设计都可能增加蛋白产量,使的蛋白生产更有效和经济。翻译终止效率蛋白表达水平受许多不同因素和过程影响。蛋白稳定性、mRNA稳定性和翻译效率在蛋白生产和积累中起主要作用。翻译过程分为起始、延伸和终止三个期。对于翻译的起始,原核mRNA需要5'端非翻译前导序列中有一段叫Shine-Dalgarno序列的特异核糖体结合序列。在真核细胞,有效的起始依赖于围绕在起始密码子ATG上下游的一段叫Kozak序列的序列。密码子利用或偏爱对延伸有深刻的影响。例如,如果mRNA有很多成簇的稀有密码子,这可能对核糖体的运动速度造成负面影响,大大减低了蛋白表达水平。翻译终止是蛋白生产必须的一步,但其对蛋白表达水平的影响还没有被研究清楚。但是最近的科学研究表明终止对蛋白表达水平有很大的影响。总的来说,更有效的翻译终止导致更好的蛋白表达。绝大多数生物都有偏爱的围绕终止密码子的序列框架。酵母 和哺乳动物偏爱的终止密码子分别是UAA和UGA。单子叶植物最常利用UGA,而昆虫和大肠杆菌倾向于用UAA。翻译终止效率可能受紧接着终止密码子的下游碱基和紧靠终止密码子的上游序列影响。在酵母 中通过改变围绕终止密码子的局部序列框架,翻译终止效率可能被减低几个100倍。对于UGA和UAA,紧接着终止密码子的下游碱基对有效终止的影响力大小次序为GU,AC;对于UAG是U、ACG。对于大肠杆菌,翻译终止效率可因终止密码子及临近的下游碱基的不同而显著不同,从80%(UAAU)到7%(UGAC)。对于UAAN和UAGN系列,终止密码子下游碱基对翻译的有效终止的影响力大小次序为UGA、C。UAG极少被大肠杆菌利用,相比UAAN和UGAN,UAG表现了有效的终止,但其后的碱基对有效终止的影响力为GU,AC。对于哺乳动物,偏爱的终止密码子为UGA,其后的碱基可以对in vivo翻译终止有8倍的影响(A、GC、U)。对于UAAN系列,in vivo终止效率可以有70倍的差别,UGAN系列为8倍。如果终止密码子附近序列没有最佳化,可能发生明显增加的翻译通读,因此减少了蛋白表达。例如,在兔网状细胞无细胞翻译系统里,UGAC的翻译通读可以高达10%,而第四个碱基如果为A,G或C,翻译通读为1%。总的来说,翻译起始框架、翻译终止序列框架和密码子利用应该仔细选择,以利于蛋白的最高水平表达。翻译终止序列框架能几倍地改变蛋白生产水平。真核细胞中的异源蛋白表达异源蛋白质在细菌中表达是目前使用的主要的蛋白生产系统。大肠杆菌一直是最经济的系统之一。然而为了生产需要特异修饰、胞外分泌或有特异折叠需要的蛋白质,其他表达系统也是需要的。真核细胞在表达原核来源的基因、真核基因的cDNA拷贝或其他无内含子的基因时可能表现很多特异问题。富含AT的基因在很多真核细胞中表达时会遭遇很剧烈的障碍。主要的真核信号序列如 加poly-A的位点、酵母 转录终止位点和真核mRNA去稳定序列都是富含AT的。内含子序列也趋向于富含AT,尽管他们有参与剪切过程的很特异的识别序列。虽然绝大多数原核基因没有剪切或聚腺苷过程,但这些真核过程需要的保守序列可能存在于原核基因中,因此当这些基因在真核细胞中表达时可能引起特异的问题。而且诸如哺乳动物和单子叶植物细胞的特异真核表达系统可能不能有效地表达无内含子的基因。 真核mRNA在离开细胞核进而在胞浆的核糖体上被翻译前需要特异的处理和修饰。这些过程包括去除内含子、5'端甲基化帽子形成和3'端加poly-A。内含子去除需要5'剪切位点、G75/G100U100A65AG65U保守序列、3'剪切位点、富含密啶NC66A100G100/G56保守序列和C72T98R77A100Y75保守序列。有效的加poly-A和mRNA剪切需要一个由两个部分组成的信号:加poly-A保守序列AAUAAA和在切割位点内的50个碱基的富含GT的序列。酵母 真核转录终止序列(几个不同的富含AT序列,如含TTTTTATA,TATATA,TACATA,TAGTAGTA的一个38bp区域)被研究的最清楚。这些结果来自对酵母 突变体CYCI mRNA的mRNA水平和相对长度的确定的实验。近期用in vivo质粒稳定性分析的研究结果证明:TATATA似乎和原始的38bp野生型区域一样有效地终止转录,而TAGATATATATGTAA和TACATA效率差些,TTTTTTTATA几乎没有效率。所有这些序列在反方向时没有终止转录功能。不幸的是几乎没有其他真核表达系统转录终止序列方面的信息。内含子对几个哺乳动物基因的正常表达是必需的,包括Beta-球蛋白、SV40 late mRNA和二氢叶酸还原酶基因。单子叶植物细胞充分表达乙醇脱氢酶的cDNA拷贝、报告基因氯霉素乙酰转移酶、Beta葡萄糖苷酸酶和其他缺乏内含子的基因时也依赖内含子。转录区域内引入内含子可以通过未确定的转录后机制增强表达。(免疫球蛋白基因)内含子可能也包含转录增强子,因此通过转录机制增强表达。 总的来讲,如果存在某些DNA序列,真核异源蛋白表达可能是个难题。为避免剧烈的表达减少,需要对基因进行扫描,确认是否含上述提及的富含AT的序列。而且,在几个真核系统表达无内含子基因可能需要引入内含子以实现外源蛋白的充分表达。
待检测样品制备生物样品往往是非常复杂的生物分子混合体,除少数特殊样品外,一般不能直接与芯片反应,必须将样品进行生物处理。从血液或活组织中获取的DNA/mRNA样品在标记成为探针以前必须扩增以提高阅读灵敏度,但这一过程操作起来却有一定的难度。比如在一个癌细胞中有成千上万个正常基因的干扰,杂合癌基因的检测和对它的高效、特异地扩增就不是一件容易的事。因为在一般溶液中PCR扩增时,靶片段太少且不易被凝胶分离,故存在其它不同的DNA片段与其竞争引物的情况。美国Mosaic Technology公司发展了一种固相PCR系统。此系统包含两套引物,每套都可以从靶基因两头延伸。当引物和DNA样品及PCR试剂相混时,如果样品包含靶序列,DNA就从引物两头开始合成,并在引物之间形成双链DNA环或“桥”。由于上述反应在固相中产生,因而避免了引物竞争现象,并可减少残留物污染和重复引发。根据样品来源、基因含量、检测方法和分析目的不同,采用的基因分离、扩增及标记方法各异。为了获得基因的杂交信号必须对目的基因进行标记。标记方法有荧光标记法、生物素标记法、同位素标记法等。目前采用的最普遍的荧光标记方法与传统方法如体外转录、PCR、逆转录等原理上并无多大差异,只是采用的荧光素种类更多,这可以满足不同来源样品的平行分析。样品制备的常用试剂:对于检测表达的芯片,样品制备通常涉及mRNA的纯化,cDNA的合成,体外转录或者PCR,标记等步骤。而对于SNP或者突变检测,则往往涉及Genomic DNA纯化和PCR标记等步骤。1. RNA纯化:从样品中分离纯化高质量的RNA是非常重要的第一步。由于RNA样品中的DNA碎片会影响后继的PCR反应,所以要彻底除去样品中的DNA。通常用mRNA纯化的方法可以除去DNA片断,或者用RNase-Free的DNase处理RNA样品。在这里我们介绍一些常用的RNA纯化试剂盒,特别是由Affymetrix公司推荐的QIAGEN RNA纯化系列。* RNeasy Protect Kit:一旦生物样品被收集分离,它的RNA会立刻变得非常不稳定,极易被降解。由于特异及非特异的RNA降解,或者由于应激反应产生新的RNA都会引起RNA状态的改变。对于生物芯片、基因表达矩阵分析(Array Analysis)、定量RT-PCR等实验来说,采样后立即稳定样品里的RNA以保存当时RNA的表达状态,是精确/定量研究基因表达分析的重要前提。为了达到这个目的,往往需要将液氮或者干冰带到采样现场,采样后立即抽提RNA或者运回实验室保存。对于实验者来说非常不方便。著名的QIAGEN公司最近新推出一种RNA抽提试剂:RNeasy Protect Kit,提供一整套RNA保护和分离试剂,从样品的制备到RNA的抽提,只需一个试剂盒即可解决所有问题。保证样品的表达信息不受破坏,确保得到可信的基因表达分析结果。试剂盒里提供一种RNAlater RNA Stabilization Reagent,只要在采样后立即将新鲜样品浸入这种液体试剂,RNA保护剂可以迅速渗透到组织或其他生物样本中,稳定并保护RNA完整而不被降解,确保下游分析得到的数据真实反应样品的表达信息。保存在RNAlater中的样品RNA可以在37度下稳定保存1天,或者在18~25度保存7天,2~8度稳定4周,或者在-20度永久保存。这种技术为在不同温度下采样,运输和保存样品提供了极大的方便,特别适用于各种动物组织、培养细胞、细菌、白细胞,但必须说明的是它不适用于全血或体液中RNA的保存。RNAlater的用法非常简单,只要在采样后立即将样品完全浸入适量(10ul/1mg组织)的RNAlater中即可。取样的动作要尽量快速利索,组织样品的大小以不超过0.5公分厚为宜,对于一些小的组织如小鼠的脾、肾等器官则可以整个取出浸入溶液中,较大的则应切开为厚度小于0.5公分的小块,以确保RNAlater 能迅速扩散渗透入组织块中的所有细胞中。采样的容器应该足够大以容纳10倍于组织重量的溶液,避免组织块挤在一起,同时建议将溶液加满容器以避免在运输过程中组织块露出液面。注意本试剂只适用于新鲜样品,对于冷藏和包埋的样品直接抽提RNA即可。另外对于RNA已经降解的样品,RNAlater只能保护剩下的样品RNA,不能修复已破坏的RNA。保存后的样品可以直接用于RNA或者mRNA的抽提。RNAlater不会影响组织块的结构,可以在室温下切出适量的组织块用于称量和抽提RNA,剩下的部分可用于继续保存样品。-20度冻存的样品可以取出在室温下进行称量等操作而无需干冰。在-20度冻存的样品反复冻融20次RNA依然保持完好无损。RNAlater处理的样品比新鲜组织稍微硬一点,但不会影响匀浆过程。取出适量的样品即可开始加RLT缓冲液进行匀浆化。和传统的RNeasy Kit一样,RNeasy Protect Kits采用QIAGEN著名的硅胶膜纯化柱技术,迅速特异地吸附样品裂解液中的RNA,无需酚氯仿抽提,不用乙醇沉淀或LiCl沉淀,也不用CsCl超离,只要洗脱即可得到纯的RNA。通常情况下RNeasy的纯化技术足以除去绝大部分的DNA,而无需额外进行DNaes处理,但是对于一些对痕量DNA非常敏感的实验,用RNase-Free DNase Set(QIAGEN cat.no. 79254)可以直接在纯化柱上消化DNA残留,在随后的洗涤步骤中除去DNase,最后洗脱得到不含DNA的纯RNA。试剂盒具有以下优点:●迅速稳定并保护RNA,确保基因完整、基因表达信息可靠。 ●由于RNA Stabilization试剂,您可以放心地在室温下操作,方便、安全——无须液氮和干冰。 ●确保RNA不受降解——即使多次冻溶也不受影响。 ●简单、快速和可靠RNA分离——使用于所有下游分析的即用型RNA。货号 品名(规格) 价格(RMB)74124 RNeasy Protect Mini Kit(50) 3181.00 75152 RNeasy Protect Midi Kit(10) 1313.00 75182 RNeasy Protect Maxi Kit(12) 4140.00 76104 RNAlater RNA Stabilizationeagent 682.00http://www.biomart.cn/upload/asset/2008/07/28/1216791379.gif
1.目的了解外源基因在原核细胞中表达的特点和方法。2.原理外源基因克隆在含有lac启动子的表达系统中。先让宿主菌生长,lac I产生的阻遏蛋白与lac操纵基因结合抑制下游的外源基因转录。向培养基中加入诱导物IPTG(异丙基硫代-b-D-半乳糖),解除抑制使外源基因大量表达。表达的蛋白可经SDS-PAGE或Western-blotting检测。3.器材旋涡混合器,微量移液取样器,移液器吸头,50ml 微量离心管,1.5ml 微量离心管,双面微量离心管架,台式冷冻离心机,制冰机,恒温摇床,分光光度计,超净工作台,恒温培养箱,摇菌试管,三角烧瓶,接种环。4.试剂LB培养基(加抗菌素),100mg/ml IPTG,20%葡萄糖。5.实验准备无菌ddH2O,1.5ml离心管装入铝制饭盒(灭菌)、移液器吸头装入相应的吸头盒(灭菌),牙签(灭菌),摇菌管(灭菌),100mg/ml IPTG (过滤灭菌)(100ml分装,-20°C保存),100mg/ml氨苄青霉素(过滤灭菌)(100ml分装,-20°C保存),配制20%葡萄糖(8磅灭菌20分钟,添加至上述LB中,终浓度为0.2%)。6.操作步骤(1) 晚上9:00接种。在超净工作台中接种含有Pinpoint™xa-3-CHI重组载体的菌株,培养于两个三角烧瓶各20ml LB-葡萄糖培养基(含抗菌素Amp 120μg/ml)的摇菌管中,慢速70~90转/分钟30°C摇菌过夜。(2) 至第二天上午8:30 OD600约为0.5,加IPTG至 100μg/ml,150~170转/分钟37°C诱导1.5-3h。同时做不加IPTG诱导和非转化的空菌诱导的对照培养。(3) 4000rpm离心15min弃掉上清液,收获菌体,用SDS-PAGE电泳分析(表达蛋白分子量为30kDa)。菌体也可放在-20°C以下保存备用。(4) 在被细菌污染的桌面上喷洒70%乙醇,擦干桌面。