推荐厂家
暂无
暂无
 留言咨询
留言咨询
 留言咨询
留言咨询
 金牌5年
金牌5年
 400-860-5168转4265
400-860-5168转4265
 留言咨询
留言咨询

 400-801-9298
400-801-9298
 留言咨询
留言咨询

 400-831-5070
400-831-5070
 留言咨询
留言咨询

 400-860-5168转2639
400-860-5168转2639
 留言咨询
留言咨询
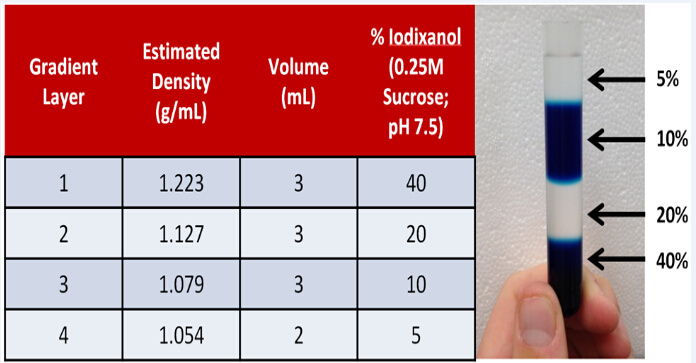





http://img3.17img.cn/bbs/upfile/images/20100518/201005181701392921.gifBioComp密度梯度制备与收集系统在生物大分子分离中的应用讲座时间:2014年08月20日 10:00 主讲人:孙福鼎 五洲东方分子生物学产品线应用工程师,负责分子成像设备以及密度梯度制备与收集产品的应用及技术支持,对密度梯度超速离心以及核糖体分离(Ribosome profiling)有着丰富的经验,目前主要致力于密度梯度超速离心在病毒分离、核糖体及叶绿体等亚细胞器分离以及其他生物学大分子分离的应用。http://img3.17img.cn/bbs/upfile/images/20100518/201005181701392921.gif【简介】1、生物学大分子分离方法2、密度梯度方法介绍及应用案例 产品应用领域应用于线性密度梯度溶液的快速制备,便于后续超速离心分离生物学样品。 产品主要特点快速高效,最快1min 内制备完成6 个离心管样品的均一线性梯度制备。程序控制,不同梯度介质及梯度范围所需程序均已内置,自动运行。适用广泛,可用于多种介质的梯度制备,包括Sucrose、Glycerol、Optiprep、Nycodenz、Ficoll、Percoll、Nacl、CsCl 等梯度介质。-------------------------------------------------------------------------------1、报名条件:只要您是仪器网注册用户均可报名参加。2、报名并参会用户有机会获得100元手机充值卡一张哦~3、报名截止时间:2014年08月20日 9:304、报名参会:http://simg.instrument.com.cn/meeting/images/20100414/baoming.jpg
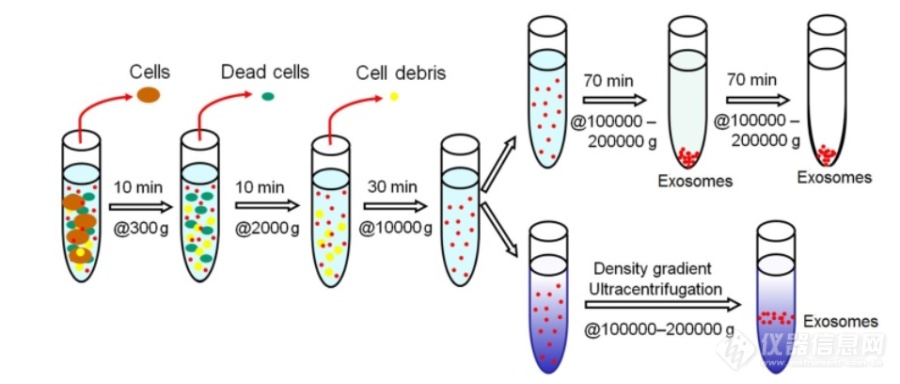
[font='times new roman'][size=18px][color=#000000]基于超速离心的外泌体分离技术[/color][/size][/font][align=left][font='times new roman'][size=16px]超速离心法([/size][/font][font='times new roman'][size=16px]UC[/size][/font][font='times new roman'][size=16px])是目前外泌体分离的“金标准”,大约[/size][/font][font='times new roman'][size=16px]56%[/size][/font][font='times new roman'][size=16px]的实验人员使用这种技术分离外泌体。目前[/size][/font][font='times new roman'][size=16px]UC[/size][/font][font='times new roman'][size=16px]包括差速超速离心和密度梯度超速离心。差速超速离心分离外泌体的方法主要受颗粒的大小、密度和形状的影响,基于颗粒的沉降速率不同,通过施加离心力,样品可以根据它们的物理性质被分离。在相同的颗粒密度下,大颗粒的沉积速度比小颗粒快,因此,更小的颗粒,如外泌体,可以通过一系列连续增加的旋转速度分离出来,具体步骤如图所示。首先用[/size][/font][font='times new roman'][size=16px]300 g[/size][/font][font='times new roman'][size=16px],[/size][/font][font='times new roman'][size=16px]2000 g[/size][/font][font='times new roman'][size=16px],[/size][/font][font='times new roman'][size=16px]10000 g[/size][/font][font='times new roman'][size=16px]的转速分别去除培养基中的细胞、坏死细胞和细胞碎片,上清液继续进行[/size][/font][font='times new roman'][size=16px]100,000 g 70[/size][/font][font='times new roman'][size=16px]分钟的超速离心,沉淀部分重悬在磷酸盐([/size][/font][font='times new roman'][size=16px]PBS[/size][/font][font='times new roman'][size=16px])缓冲液中进行另一轮[/size][/font][font='times new roman'][size=16px]100,000 g[/size][/font][font='times new roman'][size=16px]超速离心,最后,将得到的外泌体重悬于[/size][/font][font='times new roman'][size=16px]PBS[/size][/font][font='times new roman'][size=16px]缓冲液中以作下一步分析。[/size][/font][/align][align=left][font='times new roman'][size=16px]密度梯度离心[/size][/font][font='times new roman'][size=16px]法将待测生物样品添加到自上而下密度逐步增大的溶液中,在超速离心之后,这些外泌体就会移动到对应密度梯度层的底部(外泌体的密度介于[/size][/font][font='times new roman'][size=16px]1.10-1.21 g/mL[/size][/font][font='times new roman'][size=16px])。密度梯度离心法获得的外泌体具有更好的完整性和生物活性。此外,由于[/size][/font][font='times new roman'][size=16px]外泌体[/size][/font][font='times new roman'][size=16px]与胞外囊泡的大小存在重叠且外泌体存在异质性,差速超速离心分离得到的外泌体纯度和效率均较低,而密度梯度离心法使密度相对较低的外泌体漂浮,进一步净化了外泌体。[/size][/font][/align][font='times new roman'][size=16px]虽然[/size][/font][font='times new roman'][size=16px]UC[/size][/font][font='times new roman'][size=16px]是目前最常用的方法,但它也存在一些缺点:它是一种劳动密集型、耗时的方法(通常持续[/size][/font][font='times new roman'][size=16px]5-10 h[/size][/font][font='times new roman'][size=16px]),需要大量的样品和昂贵的专用设备。聚集的蛋白质和核蛋白颗粒污染使得分离的外泌体的效率和纯度相对较低。此[/size][/font][font='times new roman'][size=16px][color=#000000]外,[/color][/size][/font][font='times new roman'][size=16px]分离过程中需要超高的离心力,这可能会导致外泌体的形态和组成发生变化。[/size][/font][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108012208553147_7986_5111497_3.png[/img][/align][align=center][font='times new roman']图[/font][font='times new roman'] 1 [/font][font='times new roman']用差速超离心法分离外泌体示意图[/font][/align]
0即样品顺离心力方向沉降σ〈 S时 V〈 0即样品逆离心力方向上浮σ=S时 V=0即样品停止沉降或上浮,"稳定"在这一位置用这个公式可以很好地解释在速率一区带离心法或等密度离心法中单一样品的沉降(或上浮)行为。二、 转头的选择:1、离心转头分类:转头类别 使用的离心机 发明时间、发明者或推广商固定角式转头 低、高、超速 1943年,(英)Pickels甩平转头 低、高、超速 1951年,(德)Kahler垂直管转头 高、超速 1974-1975年,(美)Dupont公司区带转头 低、高、超速 1964-1965年,(英)Anderson、(英)MSE公司近垂直管转头 超速 1989年,(日)Hitachi Koki、(美)Beckman公司连续离心转头 低、高、超速 1965年,(英)MSE公司其他特种转头:分析转头,土壤脱水转头,细胞浮选转头,管式转头,血球比测定转头,细胞清洗转头等等。2、 各种转头用于密度梯度离心的比较:(I) 各种转头用于速率一区带(R-z)离心的优缺点分析:固定角式转头:壁部放应影响很大,用于R-z离心回、收率低,纯度也受影响一般知用于差分离心和等密度离心,离心时间向较短。是各其离心机的最高速转头。甩平转头:细长离心管用于R-z离心可以获得较高纯度和高分辨率,且容易控制离心时间,壁部入在很少。25000rpm~30000rpm的甩平转头最适用于亚细胞器的离心分离,而40000~42000rpm的甩平转头适合用于核酸、蛋白、病毒草类物质内流的分离。离心时间较长。垂直管转头:沉降距离最短,因而离心分离时间也是短。最大半径前几乎没有壁部放位,最大本径后右一定壁部效位,垂直剖面积较大,因而离心后纯样品区带的容量也较大。但在有沉殿的密度梯度离心中,沉淀和浮动区带方向转换之间存在干扰,可能影响纯样品区带的纯度。大部份R-z离心没有沉殿,垂直管转头很适合做R-z离心。近垂直管转头:管轴线与旋转主轴之间倾角7度~9度(角式转头20度~45度)沉降距离比垂直转头稍大,离心时间比角式,甩平转头都要短。由于右了倾角,沉殿可沿管壁滑向低部,因此基本上清除了沉殿与浮动区带转换之间的干扰,适合做R-z离心,特别适合做生物大分子(如质粒DNA)的自形成梯度等密度离心。区带转头:没有壁部入应特别适合做大容量的病毒,亚细胞器,生物大分子的R-z离心,可用于研究,中试和少批量生产。分离纯度高,量大,但操作要求高,转头及整体价格昂贵。连续流离心转头:工作原理的区带转头相似,可连续工作,分离量大,分离统纯度高,可用于各种生物体的差分,R-z等密度离心。近年来高速连续流转头常用于大量发酵液(大肠样菌、酝母菌)菌体的沉殿。(II) 各种转头用于等密度离心内优缺点分析:固定角式转头:主要用于差分离心的角式转头,在速离心机上可以很好地用于等密度离心,尤其是DNA平衡等密度离心,自形成梯度,用快速密封管或厚壁管,常用的单管的容量为10~15ml,常用转速40000~60000rpm,离心时间较短,分离纯度也较高。甩平转头:用作等密度离心时,壁部效应对分离效果影响较少,梯度变换在甩平时自然过渡因而很适合做等密度离心实验,优点是回收率高,分辨能力强。缺点是沉降距离长,最高转速较低(由于结构层固此类转头最主转速一般在60000rpm以下)因而,离心时间很长,对某些长离心管,10~15ml容量的转头最高转速在40000~41000rpm,用作自形成CSCL梯度的质粒DNA离心往往需要50~70小时。垂直管转头:适合作等密度离心,沉降距离最短,在没有沉殿或沉殿非常坚实的情况下,对于现代可自由选择加速、减速时间的离心机,梯度转换得很好。这类转头转进很高(目前最高转速可达100000rpm,70000xg)离心时间最短,分离纯度高,样品容量较大(垂直剖面积最大)。近垂直转头:九十年代以后开始使用的新型转头,用作生物大分子(DNA,RNA,蛋白质等)的平衡等密度离心最佳,目前这类转头的最高转速已达90000rpm近650000xg),离心时间相比垂直转头稍长。区带转头:非常适合做大容量样品的等密度离心。连续流离心转头:高、低速连续流转头一般不用作密度梯度离心超速连续流转头适合做大容量样品的等密度


