方案详情文
智能文字提取功能测试中
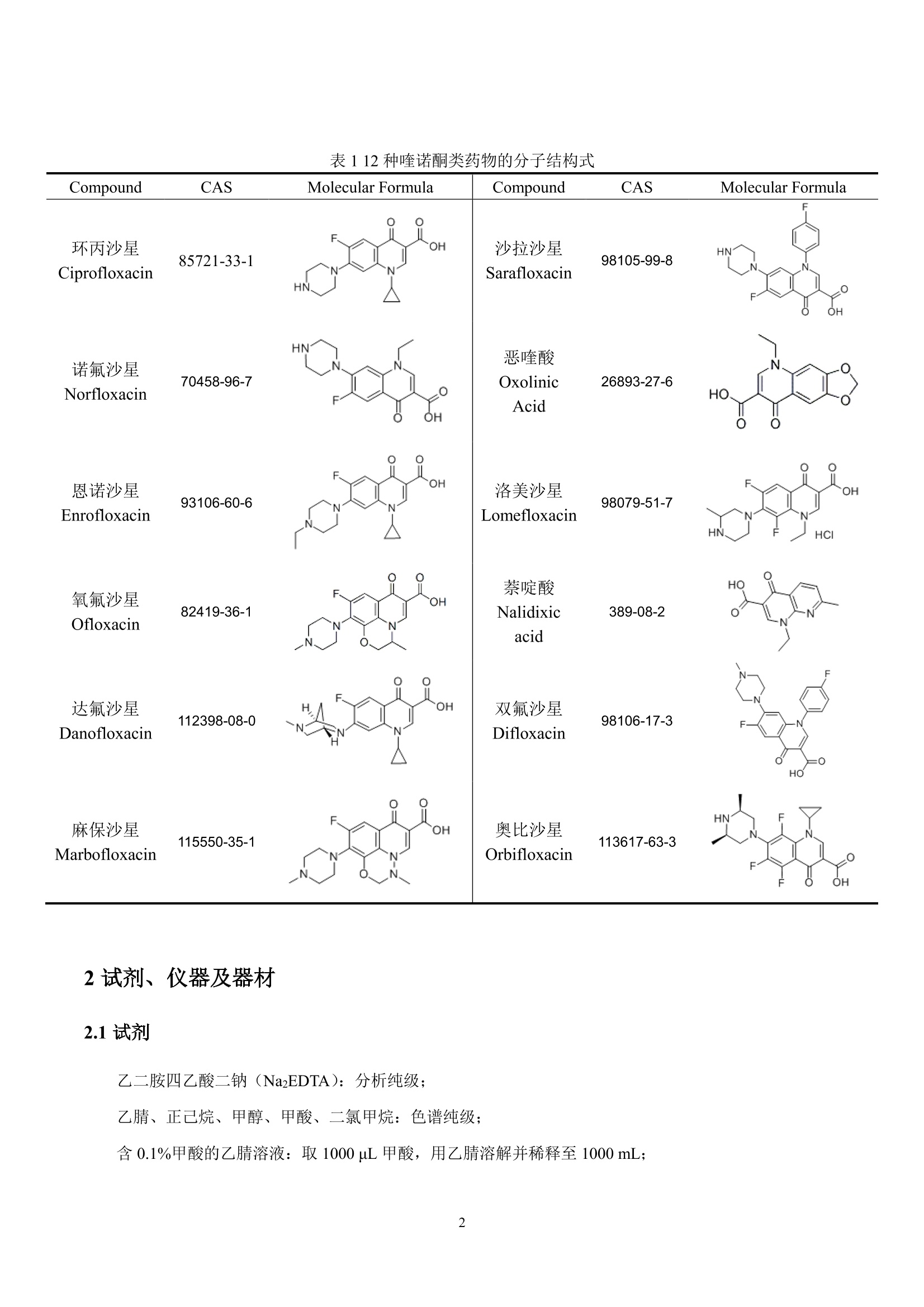
图2加标样品的 HPLC-MS/MS MRM 谱图 Preekem 全自动固相萃取-高效液相色谱串联质谱联用法检测鱼肉中的喹诺酮类药物 乡号:ANIET151118 摘要:参考《GB21312-2007 动物源性食品中14种喹诺酮药物残留检测方液液相色谱-质谱/质谱法》标准,建立了利用全自动固相萃取仪结合高效液相色谱串联质谱检测鱼肉中喹诺酮类药物的方法。样品经乙腈提取,正己烷除油, HLB 柱净化,转溶定容过滤后,用液相色谱分离,串联质谱检测。结果表明回收率良好,重现性高。 关键词:喹诺酮类药物, EXTRA, HPLC-MS/MS 1引言 喹诺酮类 (Quinolones, QNs) 药物是一类合成抗菌素,具有广谱、高效、低毒等优点,广泛应用于兽医临诊、药物预防、治疗多种因细菌或支原体引起的疾病。按其问世。先后及抗菌性能可分为四代,现常用的是第三代喹诺酮药物,也称为氟喹诺酮类(Flunroquinolones, FNs)药物。相较前几代,抗菌活性更高,半衰期长。其中,人和动物共用的有诺氟沙星、氧氟沙星、环丙沙星、依诺沙星、培氟沙星、洛美沙星等,动物专用的有恩诺沙星、沙拉沙星、达氟沙星、马波沙星、二氟沙星、奥比沙星、倍诺沙星等。过量或不当使用会导致动物性产品中喹诺酮类药物残留,可能引起消化系统、神经系统、心血管系统不良反应,对肝肾功能可能造成损害,此外也可能使致病菌产生耐药性,人类长期食用含低浓度喹诺酮类药物的动物性食品,容易诱导耐药性的传递,影响该类药物的临床疗效效。 联合国粮农组织、世界卫生组织食品添加剂专家联席委员会、欧盟都已制定了多种喹诺酮类药物在动物组织中的最高残留限量。我国于2002年规定了环丙沙星、达氟沙星、恩诺沙星、沙拉沙星、二氟沙星、恶喹酸和氟甲喹等7种药物在动物肌肉组织中的最高残留限量为 10~500 ug/kg。 本文参考《GB21312-2007动物源性食品中14种喹诺酮类药物残留检测方法液相色谱-质谱/质谱法》[],建立了利用全自动固相萃取仪 (EXTRA)结合高效液相色谱-串联质谱联用 (High Performance LiquidChromatography- Triple Quad Mass Spectrometry, HPLC-MS/MS)检测12种喹诺酮类药物在鱼肉中残留量的方法。在乙腈提取、正己烷除油后,采用 EXTRA 全自动固相萃取仪进行样品净化,自动完成 SPE 柱活化、样品上样、淋洗、目标物洗脱和收集等步骤,收集液再经氮吹浓缩、溶剂转换、定容后,用 HPLC-MS/MS检测。 表112种喹诺酮类药物的分子结构式 Compound CAS Molecular Formula Compound CAS Molecular Formula 环丙沙星 85721-33-1 OH 沙拉沙星 98105-99-8 HN Ciprofloxacin HN Sarafloxacin 0 OH HN 诺氟沙星 70458-96-7 恶喹酸 26893-27-6 Oxolinic Norfloxacin 0 HO. Acid OH 恩诺沙星 93106-60-6 'OH 洛美沙星 98079-51-7 ^(OH Enrofloxacin Lomefloxacin HN. HCI OH 萘啶酸 HO 氧氟沙星 82419-36-1 Nalidixic 389-08-2 0 Ofloxacin C acid 达氟沙星 112398-08-0 OH 双氟沙星 98106-17-3 Danofloxacin Difloxacin =O HO 麻保沙星 Marbofloxacin 115550-35-1 F、 0. OH 奥比沙星Orbifloxacin 113617-63-3 0 F OH 2试剂、仪器及器材 2.1试剂 乙二胺四乙酸二钠(Na2EDTA):分析纯级; 乙腈、正己烷、甲醇、甲酸、二氯甲烷:色谱纯级; 含0.1%甲酸的乙腈溶液:取1000 uL甲酸,用乙腈溶解并稀释至1000 mL; 乙腈饱和的正己烷;正己烷中加入一定量乙腈,剧烈振荡后静置分层,上层即为所需; 5%甲醇水溶液:取5mL甲醇,用水溶解并稀释至100 mL; 50%甲醇二氯甲烷溶液:取50mL甲醇与 50 mL 二氯甲烷混匀; 定容溶剂:取20mL 甲醇与80 mL 水混匀得25%甲醇水溶液,再加入100 p.L甲酸,混匀得含0.1%甲酸的25%甲醇水溶液,即为定容溶剂。 100 ug/mL 喹诺酮类药物标准储备液:分别准确称取标准品1 mg, 于10mL容量瓶中,用甲醇溶解并稀释至刻度,配制成浓度为 100 ug/mL 的喹诺酮类药物标准储备液,-20℃以下保存; 实验用水均为超纯水(电导率=18MQcm), 取自Milli-Q制水机(Millipore, USA). 2.2仪器及器材 固相萃取柱: HLB, 60mg/3mL,上海安谱公司; 全自动固相萃取仪: EXTRA,上海屹尧仪器科技发展有限公司; 高效液相色谱串联质谱联用仪: Agilent 1290 infinity - 6490 Triple Quad MS; 0.22 um PVDF针头式过滤器:天津津腾实验设备有限公司; 分析天平;旋涡混合仪;超声波清洗仪;离心机;氮吹仪;移液枪;均质仪; 50mL离心管;梨形瓶;玻璃滴管;收集管;样品管; 实验中所用玻璃器皿使用前均经450℃高温灼烧4h后冷却备用。 3实验方法 3.1前处理方法 3.1.1提取 称取(5.00±0.01)g绞碎后的样品,置于50ml离心管中,加入0.5 g NazEDTA、25 mL 0.1%甲酸乙腈溶液、20 mL乙腈饱和的正己烷,均质3 min 后以 3500 r/min 离心5 min, 将中间层乙腈溶液收集于梨形瓶中,样品残渣再加入25 mL 含 0.1%甲酸的乙腈溶液,重复萃取操作,合并乙腈提取溶液,在40℃下水浴减压浓缩至干。残液中准确加入20 mL 超纯水及约 10 mL正己烷,振荡后弃去正己烷层,重复一次,准确移取下层清液4 mL 于进样管中待净化。 3.1.2净化 HLB 固相萃取柱依次用5 mL 甲醇、5 mL水活化,取备用液过柱,流速1mL/min/,用5mL水及5mL 5%甲醇水溶液淋洗固相萃取柱,用8mL甲醇及4mL50%甲醇二氯甲烷溶液洗脱,收集洗脱液。 3.1.3定容 收集的洗脱液在40℃水浴中氮气吹干,以定容溶剂定容至1.0 ml, 0.22 um滤膜过滤,滤液待进样。 3.2检测方法 3.2.1 EXTRA 净化程序 EXTRA 净化程序如表2所示。 表2全自动固相萃取仪检测动物性食品中四环素类药物的净化程序 动作 位置 溶剂 体积 抽溶剂速度 打溶剂速度 (mL) (mL/min) (mL/min) 清洗 外针 水 8 90 90 活化 甲醇 20 2 水 20 上样 样品 4 20 空气 0.5 60 清洗 外针 8 90 90 淋洗 20 2 5%甲醇水溶液 5 60 2 空气 50 60 60 洗脱 甲醇 8 20 50%甲醇二氯甲烷溶液 4 60 20 空气 50 60 60 3.2.2色谱条件 色谱柱为 Phenomenex Kinetex C18柱,长度100 mm, 内径3.0mm, 涂层粒径2.6 um;柱温30℃,流速:0.25mL/min, 进样量:10.0pL。 流动相为超纯水(A)和含0.1%甲酸的乙腈溶液(B);梯度洗脱程序如下:0-2 min 10% B, 2-10 min10%-15%B, 10-12 min15%B, 12.01-16 min 25%B, 16-24 min 25%-80%B, 24-26min 80%B, 26.01-30 min10%B。 3.2.3质谱条件 电喷雾离子源(ESI),正离子扫描,多反应选择监测 (Multiple Reaction Monitoring, MRM)模式;鞘气温度 (Sheath Gas Temperature) 350℃,鞘气流速 (Sheath Gas Flow) 11 L/min, 氮气发生器提供; 干燥气温度 (Dry Gas Temperature) 160℃,干燥气流速(Gas Flow) 16L/min, 氮气发生器提供;雾化气压力(Nebulizer Pressure) 30 psi;i;喷嘴电压 (Nozzle Voltage) 1500V; 碰撞气 (Collision Gas) 为高纯氮 气,气体纯度≥99.999%。质谱 MRM 采集参数见表3, MRM 谱图见 12 11 7 10 8 图1. 表3目标物及替代物的 LC-MS/MS MRM 参数、工作曲线线性范围、相关系数和仪器检出限 Compound MS Parameters Linear IDL PI DI CE Range R2 (ug/L) (m/z) (m/z) (eV) (ug/L) 环丙沙星 332.1 314.1*,288.1 15,15 5-200 0.9951 5.0 诺氟沙星 320.1 302.1*,276.1 15,10 5-200 0.9920 5.0 恩诺沙星 360.1 342.1*,316.1 15,15 5-200 0.9945 5.0 氧氟沙星 362.1 318.1*,261.0 15,20 5-200 0.9943 0.5 达氟沙星 358.1 340.0*,283.1 20,20 5-200 0.9953 5.0 麻保沙星 363.1 345.1*,320.0 15,20 5-200 0.9905 5.0 沙拉沙星 386.0 368.0*,342.1,299.0 20,15,25 5-200 0.9961 1.0 恶喹酸 262.0 244.0* 12 5-200 0.9958 0.5 洛美沙星 352.2 308.1*,264.9 10,20 5-200 0.9994 0.1 萘酸 233.1 215.0*,187 15,20 5-200 0.9987 0.1 双氟沙星 400.2 382.1*,356 20,10 5-200 0.9907 0.1 奥比沙星 396.2 352.1*,295 15,25 5-200 0.9880 0.1 4 12 6 3 5 9 11 7 1 10 8 图1标准品中目标物的LC-MS/MS MRM谱图 注:1:环丙沙星;2:诺氟沙星;3:恩诺沙星;4:氧氟沙星;5:达氟沙星;6:麻保沙星; 7:沙拉沙星;8:恶喹酸;9:洛美沙星;10:萘啶酸;11:双氟沙星;12:奥比沙星 4结果与讨论 4.1加标回收率及精密度 在(5.00±0.01)g空白样品中添加一定量的标准混合溶液,使样品中目标物的量达到 100 ng (20ug/kg)及200 ng (40 ug/kg), 考察方法的回收率和重现性。加标样品所得谱图如图2,样品加标回收率、相对标准偏差(n=3)如表4所示: 4 6 12 117 10 8 注:1:环丙沙星;2:诺氟沙星;3:恩诺沙星;4:氧氟沙星;5:达氟沙星;6:麻保沙星; 7:沙拉沙星;8:恶喹酸;9:洛美沙星;10:萘啶酸;11:双氟沙星;12:奥比沙星 表4鱼肉中喹诺酮类药物加标回收率及相对标准偏差 Compound 20 ug/kg 40 pg/kg Rec% RSD% Rec% RSD% 环丙沙星 107.5% 11.3% 92.3% 10.3% 诺氟沙星 110.9% 6.5% 127.3% 7.9% 恩诺沙星 99.9% 13.0% 107.4% 11.3% 氧氟沙星 82.6% 12.4% 76.9% 12.1% 达氟沙星 76.6% 7.8% 111.0% 7.4% 麻保沙星 103.9% 6.9% 95.7% 4.1% 沙拉沙星 108.5% 11.9% 113.1% 7.0% 恶喹酸 96.9% 13.5% 93.9% 10.1% 洛美沙星 98.9% 8.7% 98.1% 9.0% 萘啶酸 89.6% 7.6% 93.3% 4.0% 双氟沙星 104.4% 8.2% 127.0% 10.5% 奥比沙星 86.3% 7.1% 85.6% 4.9% 4.2样品检测结果 按照本文所述方法对实际样品进行分析,基底干净无干扰峰,样品加标回收率良好,重现性高。 5结论 本方法采用乙腈对鱼肉中的12种喹诺酮类药物进行提取,全自动固相萃取进行样品净争,有效地去除了样品中的干扰成分,然后利用高效液相色谱-串联质谱联用仪进行检测。检测结果表明,该方法抗干扰性强, 在 20 ug/kg 和40 ug/kg 的加标浓度下,回收率在76.7%-127.3%之间,相对标准偏差在 4.1%-13%之间。 ( 参考文献 ) ( [1]赵思俊,李存,江海洋,等.高效液相色谱检测动物肌肉组织中7种喹诺酮类药物的残留[].分析化学, 2007,35(6):786-790. ) ( [2]《GB21312-2007 动物源性食品中14种喹诺酮类药物残留检测方法液相色谱-质谱/质谱法》. )
关闭-
1/7

-
2/7
还剩5页未读,是否继续阅读?
继续免费阅读全文产品配置单
上海屹尧仪器科技发展有限公司为您提供《动物源食品中喹诺酮类药物检测方案(固相萃取仪)》,该方案主要用于水产品中兽药残留检测,参考标准《暂无》,《动物源食品中喹诺酮类药物检测方案(固相萃取仪)》用到的仪器有PreeKem屹尧EXTRA全自动固相萃取仪、PreeKem屹尧N1全自动氮吹浓缩仪。
我要纠错
推荐专场
相关方案










 咨询
咨询