单克隆抗体中使用BiopharmaLynx 1.3软件检测方案(液相色谱仪)
检测样品 单克隆抗体
检测项目 使用BiopharmaLynx 1.3软件

 银牌会员
0 篇解决方案
银牌会员
0 篇解决方案
方案详情文
智能文字提取功能测试中
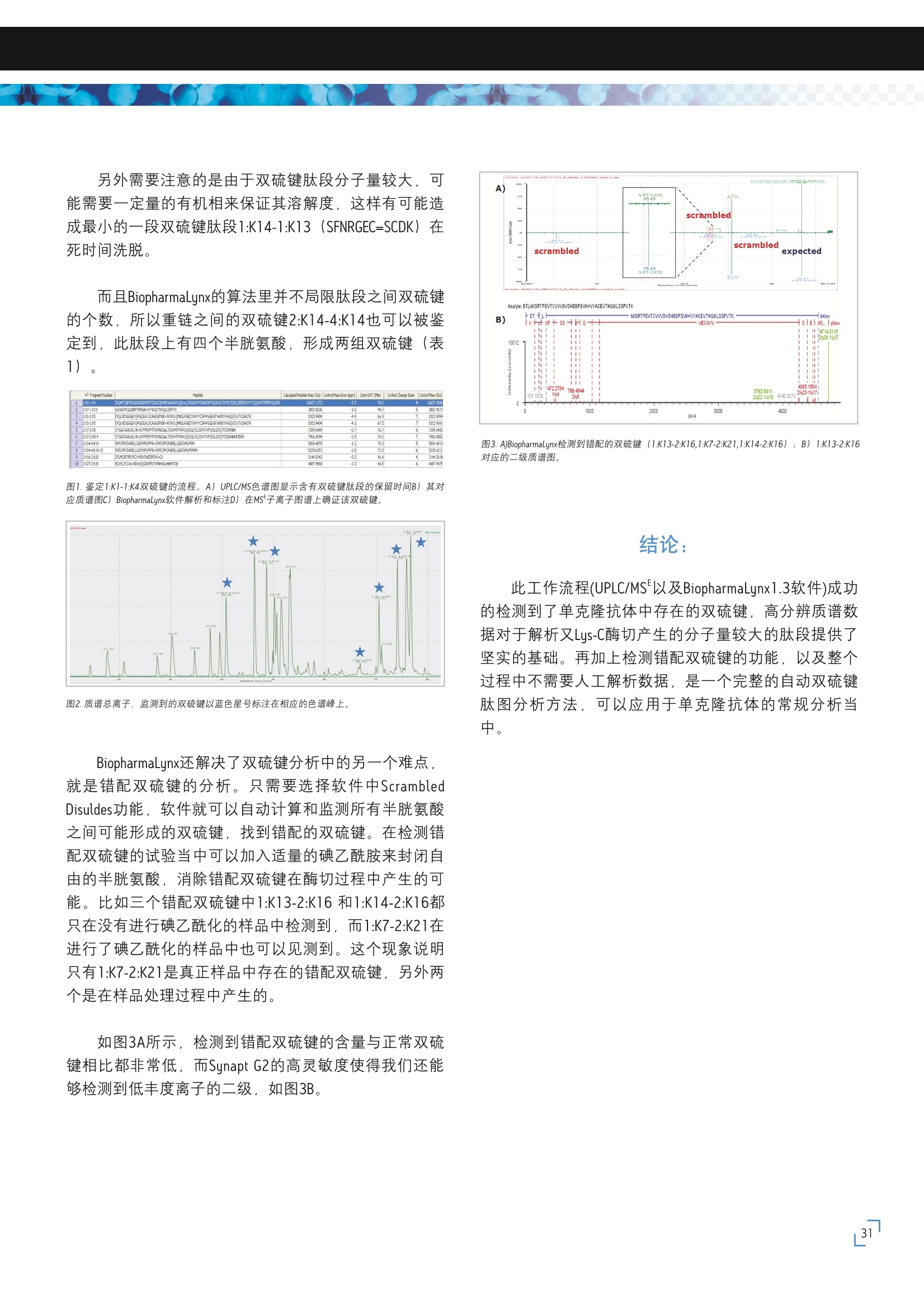
[蛋白质药物分析专业软件] 使用BiopharmaLynx 1.3软件进行自动快速的双硫键分析单克隆抗体分析实例 陈熙 沃特世科技(上海)有限公司实验中心 随着近些年来抗体类药物研发的迅速发展,质谱技术也被广泛的应用在生物药物的表征中。蛋白质的高级结构正确与否对于治疗性蛋白药物的生物活性起着至关重要的作用,但是在蛋白质表征中这方面的研究一直是一个难点,尤其是双硫键的确认,包括错配的双硫键。 如果一个蛋白含有8个半胱氨酸,就会产生105种双硫键可能的配对。而典型的单克隆抗体体般含有32个半胱氨酸,大大地增加了可能的双硫键配对。 在以往的分析工作中,双硫键的确证经常需要人为的分析质谱数据,非常耗时耗力,又可能引入人为的误差,而且人为的去寻找错配的双硫键几乎是不太可能的。 根据以上这些难点,沃特世开发了一套全自动的双硫键解析流程。此流程使用了UPLC/MS数据采集模式和BiopharmaLynx"自动数据分析处理软件。此方法不但可以确认正确的双硫键组成,还可以自动的分析出错配的双硫键来,并且提供相应的碎片离子来保证结论的正确性。 MS数据采集方式交替的采集母离子和碎片离子的信息,克服了很多传统肽图谱分析方法的缺点,是一个快速健全的可以在常规分析中使用的分析手段,被成功的应用在单克隆抗体双硫键的分析当中。 本文中以Trastuzumab为例,展示了一个完整的双硫键分析流程。 液相系统: ACQUITY UPLC (BEH300 C8,11.7um,2.1*150mm) 质谱系统: SynaptG2 HDMS正离子模式 ( 试剂: Endoproteinase Lys-C进行酶切, lodoacetamide, RapiGest" (Waters, p/n 186001861) ) 实验结果和讨论: 在进行双硫键实验的时候选择的Lys-C进行酶切,可以降低酶切后谱图的复杂程度,而且在酶切的过程中使用了RapiGest, 辅助酶切顺利进行。 首先确认整个工作流程可以鉴定到正确存在的双硫键,将LC/MS结果倒入BiopharmaLynx中, 对照Trastuzumab的序列进行搜索,确认正确的双硫键配对(图1)。图1中仅以1:K1-1:K4为例,其他双硫键也是在同一个检测中被鉴定到的,只是因为分子量大小不同,在色谱图上保留时间不同。 图1.鉴定1:K1-1:K4双硫键的流程。A) UPLC/MS色谱图显示含有双硫键肽段的保留时间B)其对应质谱图C) BiopharmaLynx软件解析和标注D)在MSE子离子图谱上确证该双硫键。 图1显示的是最大的一段含有双硫键肽段1:K1-1:K4的表征过程(此肽段为轻链链内双硫键,单同位素质量为10657.12Da)。此双硫键首先根据其MH+母离子的分子量被检测并标注出来(图1C),然后采用高能量的MS碎片离子来确认序列。MS碎片离子不但含有1:K1和1:K4各自的b/u碎片离子,而且还含有包括双硫键在内的碎片,比如7019.27Da (1/y39-2/y24)和10431.19Da (1/y39-2/y56),提供了明确的双硫键存在的证据。 另外需要注意的是由于双硫键肽段分子量较大,可能需要一定量的有机相来保证其溶解度,这样有可能造成最小的一段双硫键肽段1:K14-1:K13(SFNRGEC=SCDK) 在死时间洗脱。 而且BiopharmaLynx的算法里并不局限肽段之间双硫键的个数,所以重链之间的双硫键2:K14-4:K14也可以被鉴定到,此肽段上有四个半胱氨酸,形成两组双硫键(表1)。 图1.鉴定1:K1-1:K4双硫键的流程。A) UPLC/MS色谱图显示含有双硫键肽段的保留时间B)其对应质谱图C) BiopharmaLynx软件解析和标注D)在MS子离子图谱上确证该双硫键。 图2.质谱总离子,监测到的双硫键以蓝色星号标注在相应的色谱峰上。 BiopharmaLynx还解决了双硫键分析中的另一个难点,就是错配双硫键的分析。只需要选择软件中ScrambledDisuldes功能,软件就可以自动计算和监测所有半胱氨酸之间可能形成的双硫键,找到错配的双硫键。在检测错配双硫键的试验当中可以加入适量的碘乙酰胺来封闭自由的半胱氨酸,消除错配双硫键在酶切过程中产生的可能。比如三个错配双硫键中1:K13-2:K16和1:K14-2:K16都只在没有进行碘乙酰化的样品中检测到,而1:K7-2:K21在进行了碘乙酰化的样品中也可以见测到。这个现象说明只有1:K7-2:K21是真正样品中存在的错配双硫键,另外两个是在样品处理过程中产生的。 如图3A所示,检测到错配双硫键的含量与正常双硫键相比都非常低, 而Synapt G2的高灵敏度使得我们还能够检测到低丰度离子的二级,如图3B。 图3. A)BiopharmaLynx检测到错配的双硫键(1:K13-2:K16,1:K7-2:K21,1:K14-2:K16);B) 1:K13-2:K16对应的二级质谱图。 结论: 此工作流程(UPLC/MS"以及BiopharmaLynx1.3软件)成功的检测到了单克隆抗体中存在的双硫键,高分辨质谱数据对于解析又Lys-C酶切产生的分子量较大的肽段提供了坚实的基础。再加上检测错配双硫键的功能,以及整个过程中不需要人工解析数据,是一个完整的自动双硫键肽图分析方法,,可以应用于单克隆抗体的常规分析当中。 使用BiopharmaLynx 1.3软件自动进行快速的双硫键分析单克隆抗体,高分辨质谱数据对于解析又Lys-C酶切产生的分子量较大的肽段提供了坚实的基础,再加上检测错配双硫键的功能
关闭-
1/2

-
2/2
产品配置单
上海暄泓科学仪器有限公司为您提供《单克隆抗体中使用BiopharmaLynx 1.3软件检测方案(液相色谱仪)》,该方案主要用于单克隆抗体中使用BiopharmaLynx 1.3软件检测,参考标准《暂无》,《单克隆抗体中使用BiopharmaLynx 1.3软件检测方案(液相色谱仪)》用到的仪器有Waters 液相色谱ACQUITY UPLC系统。
我要纠错
推荐专场
相关方案




 咨询
咨询

