细胞表面表达着各种受体,这些受体用于感知环境变化以使细胞做出相应调整,其中免疫调节受体发挥着至关重要的作用,此次整理分享的文章讲的就是肿瘤表面一种免疫抑制性分子-LILRB4,文章作者深入研究了LILRB4的作用机制,具体内容如下:
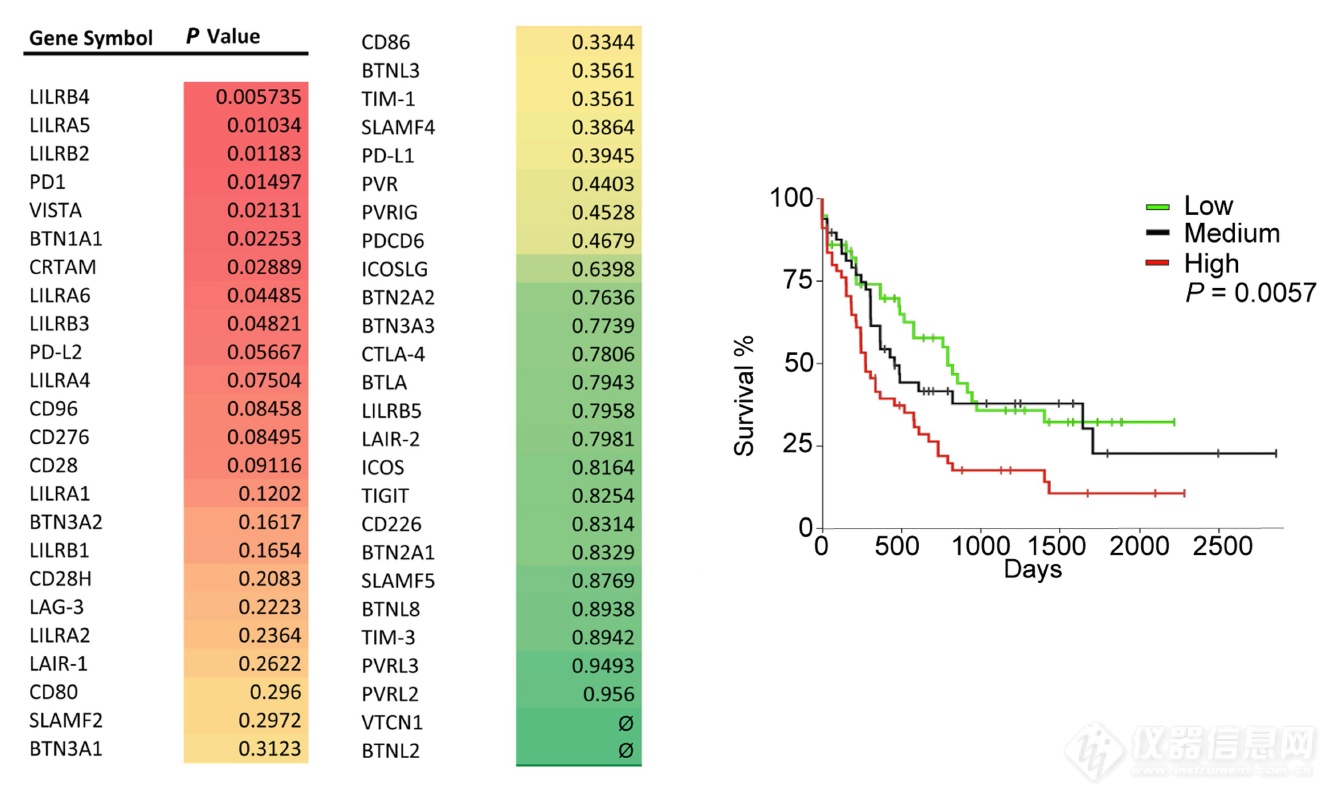
从零开始比较难,作者在TCGA数据库中检索、分析免疫调节分子和病人存活率的关系,发现LILRB4的mRNA水平和存活时间负相关
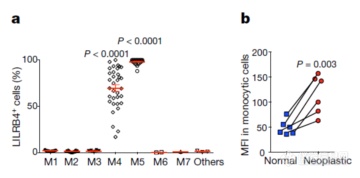
对105个病人样本进行检测,发现LILRB4主要表达于单核细胞和单核急性髓性白血病细胞,且单核急性髓性白血病细胞表达水平更高(AML subtypes by the French-American-British (FAB) classification, acute myeloblastic leukaemia with minimal maturation (M1, n = 9), acute myeloblastic leukaemia with maturation (M2, n = 34), acute promyelocytic leukaemia (M3, n = 10), acute myelomonocytic leukaemia (M4, n = 34), acute monocytic leukaemia (M5, n = 25), acute erythroid leukaemia (M6, n = 2), and acute megakaryoblastic leukaemia (M7, n = 1)),有特异性表达的意思,暗示有作为治疗靶标的价值
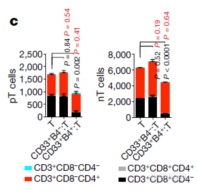
将LILRB4阳性(B4+)或阴性(B4-)的肿瘤细胞与病人T细胞或健康人T细胞共培养,发现LILRB4阳性细胞可抑制T细胞增殖
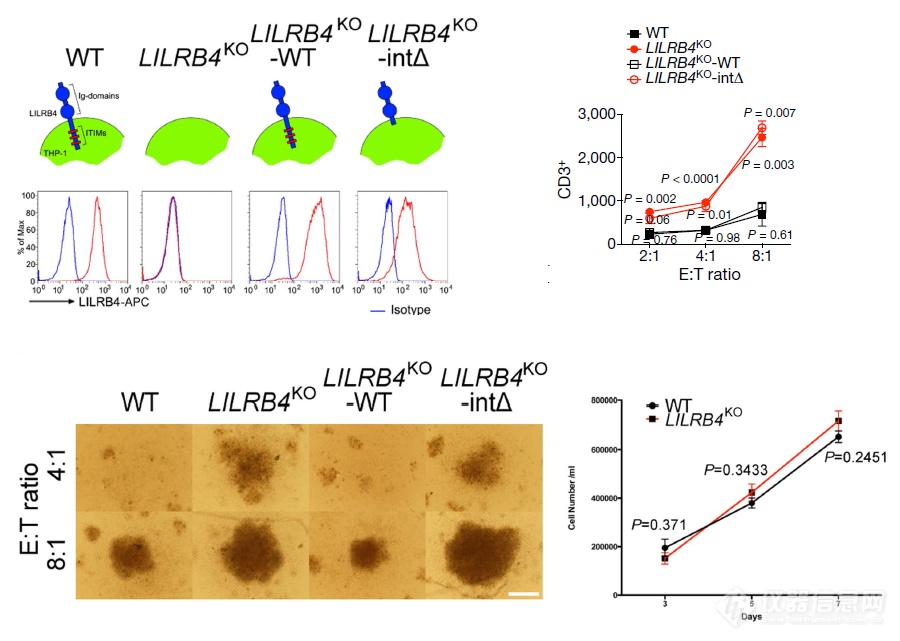
共培养实验暗示LILRB4表达的肿瘤细胞可抑制T细胞生长,作者做了LILRB4不同的细胞系:LTLRB4 KO组 - 敲掉LILRB4的肿瘤细胞(T)无法再抑制T细胞增殖(E);LILRB4 KO-WT组 - LILRB4缺陷的肿瘤细胞重新表达LILRB4后又可抑制T细胞增殖;LILRB4 KO-int△组 – 表达LILRB4胞内段缺陷蛋白的肿瘤细胞无法抑制T细胞增殖
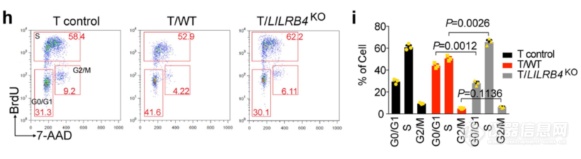
继续共培养实验:LILRB4表达肿瘤细胞可影响T细胞周期
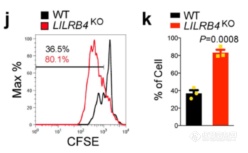
共培养实验:敲除LILRB4后的肿瘤细胞无法再抑制T细胞增殖

做完敲除做阻断,LILRB4抗体可解除LILRB4肿瘤细胞对T细胞的抑制作用
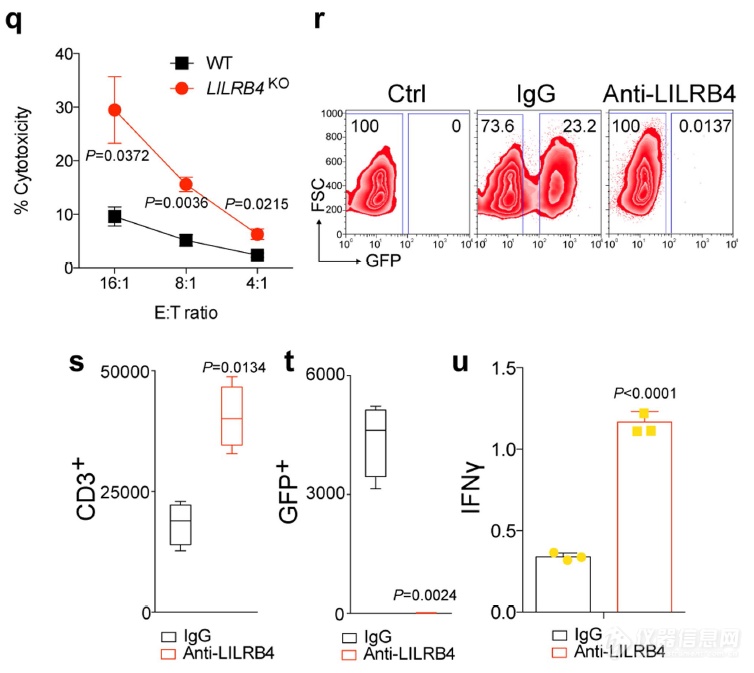
LILRB4抗体可增强T细胞对肿瘤细胞的杀伤作用(q用PI染色看杀伤;r、t
中肿瘤细胞表达GFP,通过GFP阳性群体占比看杀伤;s看T细胞数目;u看T细胞生成细胞因子的能力)
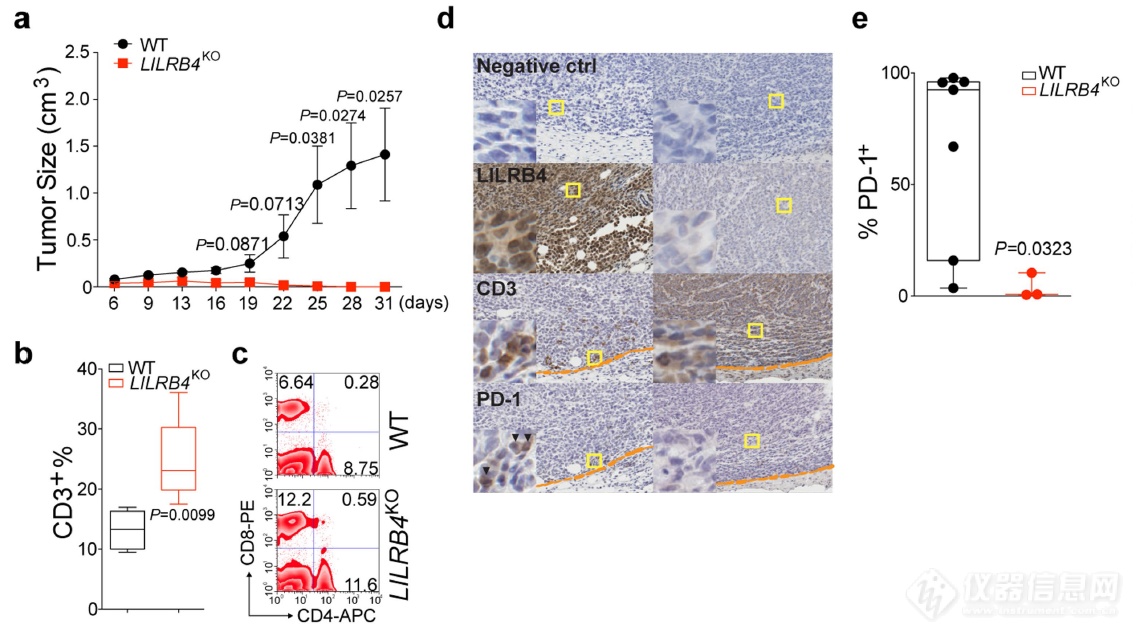
上面通过肿瘤细胞和T细胞共培养,in vitro的看LILRB4对肿瘤细胞抑制T细胞的贡献,开始in vivo实验:敲除LILRB4的肿瘤细胞成瘤能力弱,抑制T细胞的作用弱
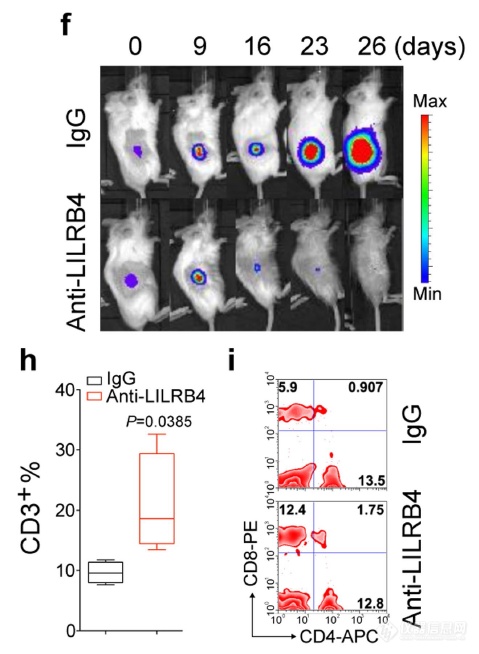
LILRB4抗体可抑制成瘤,解除LILRB4对T细胞的抑制
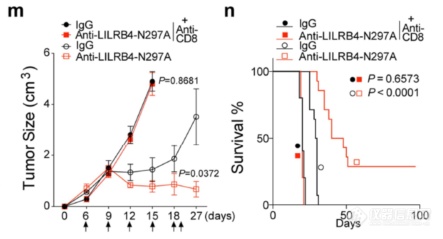
LILRB4抗体抑制肿瘤延长存活时间的作用不依赖于Fc段(anti-LILRB4-N297A为fc段突变无功能型抗体),依赖与CD8 T细胞(anti CD8敲除T细胞后LILRB4抗体无法再抑制肿瘤生长延长存活时间)
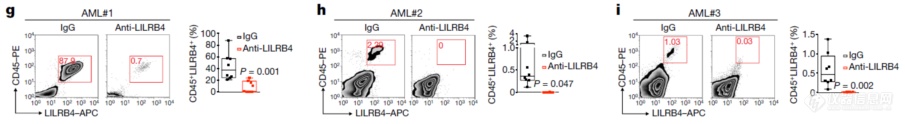
将病人肿瘤直接抑制到小鼠上,发现LILRB4抗体可抑制肿瘤的发展。到这里,作者发现LILRB4信号可抑制T细胞发挥促瘤作用
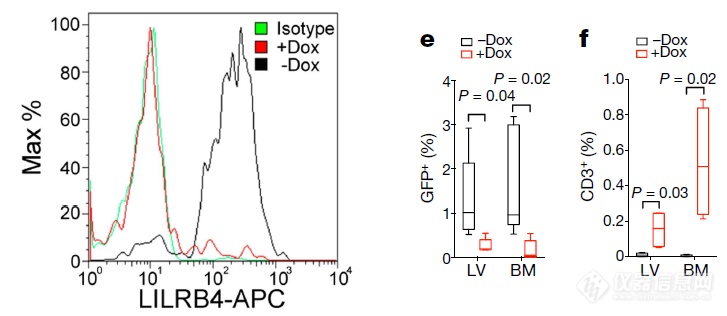
Dox诱导敲除LILRB4后,肿瘤细胞(表达了GFP)对肝脏、骨髓的浸润降低
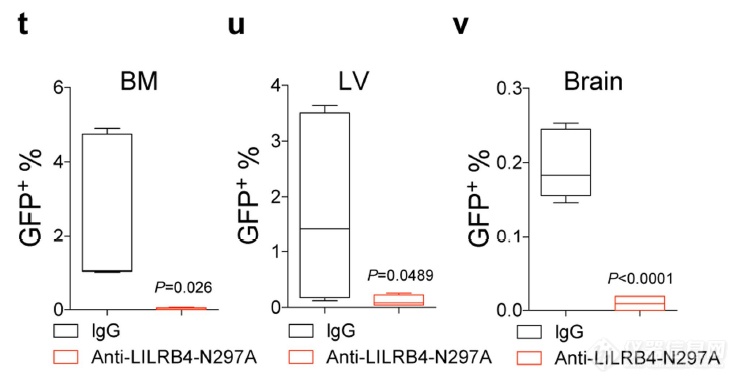
LILRB4抗体亦可降低肿瘤细胞对骨髓、肝、脑的浸润
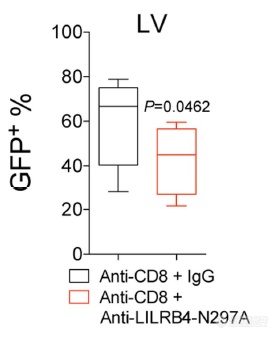
敲除CD8后,LILRB4抗体抑制浸润的作用仍在,暗示抗体阻断浸润的作用不依赖于T细胞,LILRB4参与调节肿瘤细胞的浸润
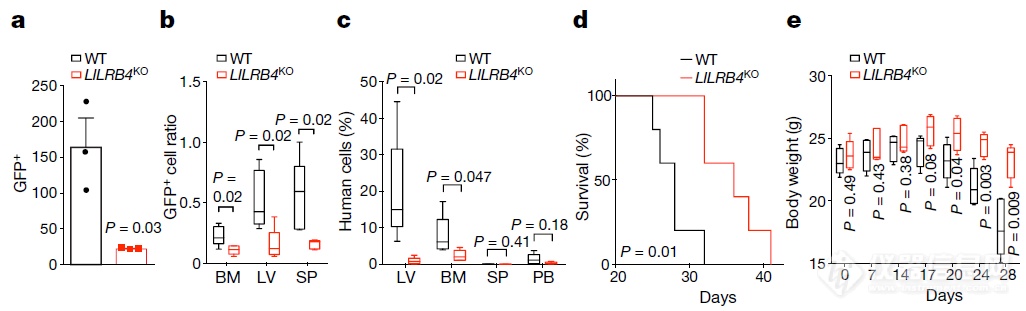
LILRB4敲除后肿瘤细胞的迁移、归巢能力降低,小鼠存活时间延长、体重减重延缓
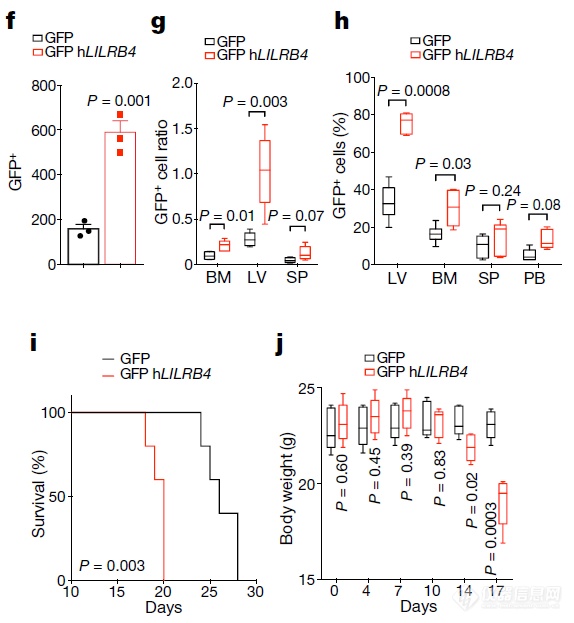
敲了看还不过瘾,让一个不表达LILRB4的细胞表达LILRB4后看对迁移、归巢、生存时间、体重的影响,再次暗示LILRB4参与调节肿瘤细胞的浸润,存在促瘤作用,小鼠健康状态负相关
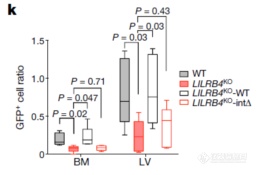
LILRB4促进浸润的作用依赖LILRB4的胞内段
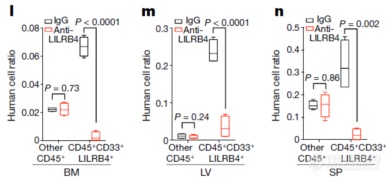
LILRB4抗体可特异性的阻断单核AML细胞(CD45+、CD33+、LILRB4)的浸润。至此,继证明LILRB4可抑制T细胞功能,又证明LILRB4还参与调节肿瘤细胞的浸润
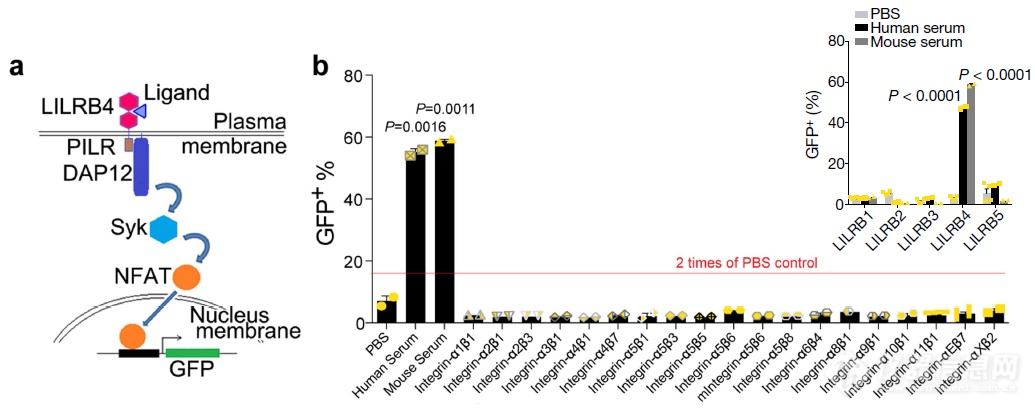
前面证明了LILRB4的功能(抑制T细胞、促进肿瘤细胞浸润),它表达于肿瘤细胞表面,发挥作用依赖胞内信号段,必然存在与其结合的配体,作者设计了一个基于GFP的报告系统以筛选LILRB4的配体:基于已有文献,尝试了一系列配体均无法激活LILRB4,发现小鼠和人的血清可特异性的激活LILRB4
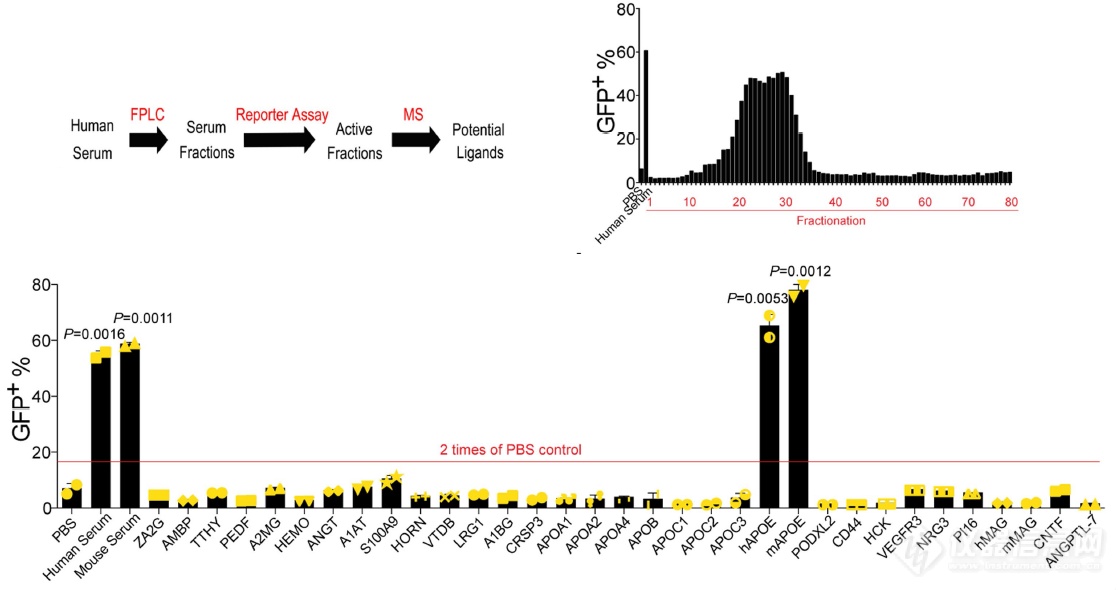
用蛋白纯化分离,之后用GFP报告系统筛选血清中能激活LILRB4的组分,发现APOE可特异性的激活LILRB4
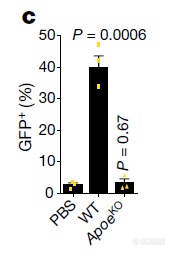
反过来再验证:APOE敲除小鼠的血清无法激活LILRB4
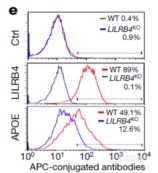
继续验证APOE可与LILRB4结合:APOE与敲除LILRB4细胞的结合能力弱
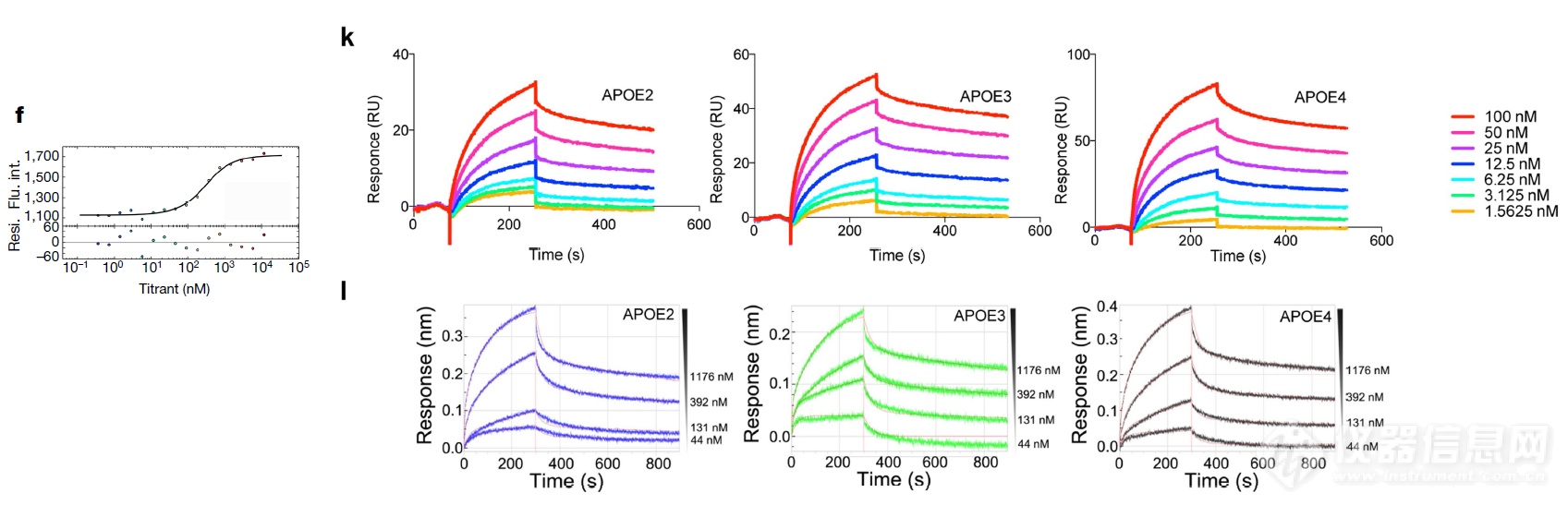
MST、SPR、Octet技术多方法确证APOE可与LILRB4结合
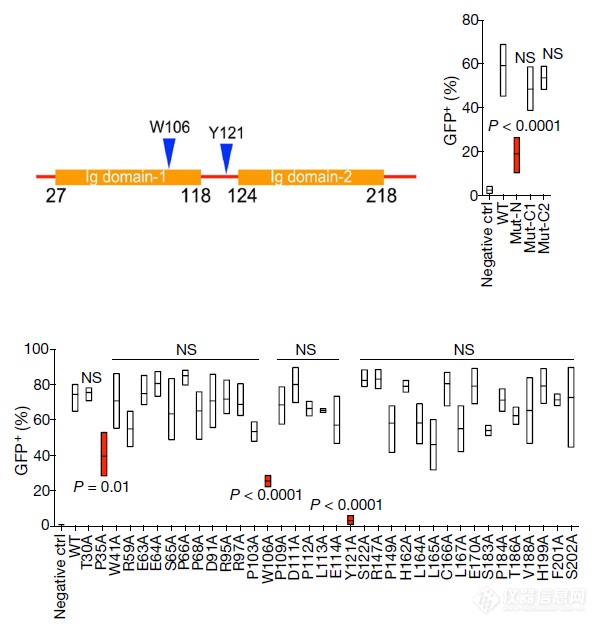
突变法找APOE上与LILRB4结合的关键位点(还是用GFP报告系统验证):W106和Y121
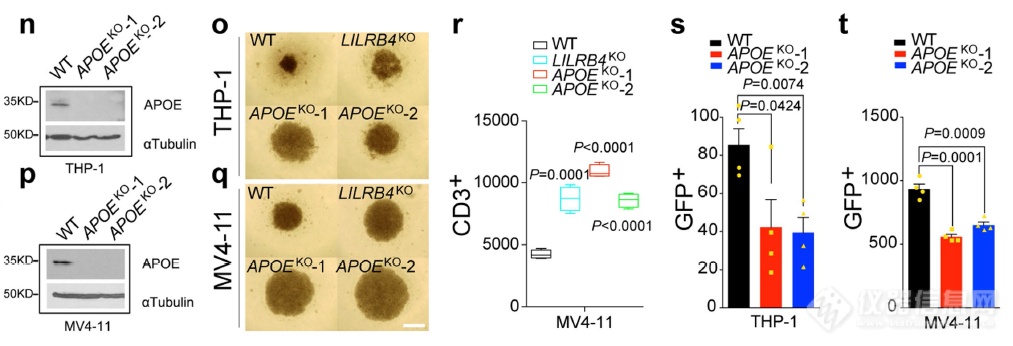
结构角度证明了APOE可结合LILRB4,开始功能角度的验证:敲除APOE可达到和敲除LILRB
4相似的效果 – 解除共培养时肿瘤细胞对T细胞的抑制作用
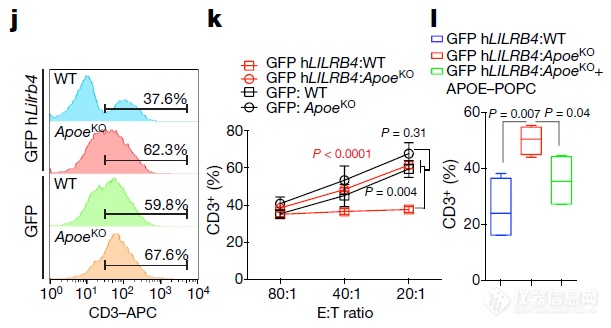
不同的肿瘤细胞(GFP或GFP LILRB4)与T细胞共培养,加入不同的血清(野生型小鼠血清-WT或APOE缺陷型小鼠血清-APOE KO),比较T细胞的比例:加入APOE缺陷小鼠血清组T细胞比例更高,缺陷血清中添加APOE-POPC又可降低T细胞比例,暗示APOE对T细胞抑制作用存在贡献
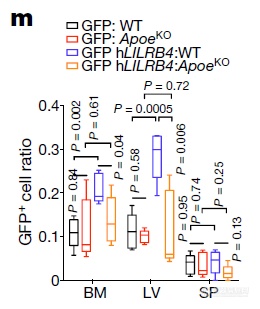
不同的肿瘤细胞移植到不同的小鼠上,APOE缺陷的受体鼠肿瘤细胞骨髓、肝、脾浸润更低,暗示APOE对肿瘤浸润存在贡献
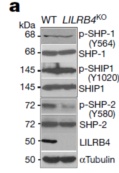
前面顺藤摸瓜摸到了LILRB4的配体,开始看LILRB4被激活后肿瘤细胞内部的信号变化:参考前人研究,将目光放到了SHP磷酸化上,KO LILRB4后,SHP-2的磷酸化降低,暗示LILRB4通过SHP-2起效
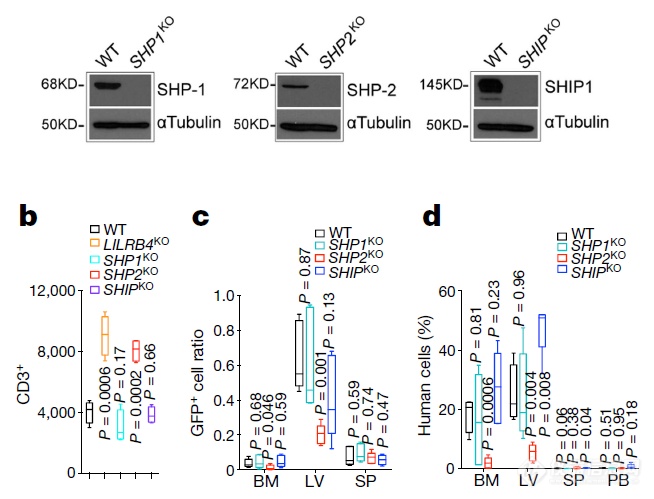
KO 肿瘤细胞SHP-2可解除肿瘤细胞对T细胞的抑制,减少浸润,暗示LILRB4通过SHP-2发挥作用
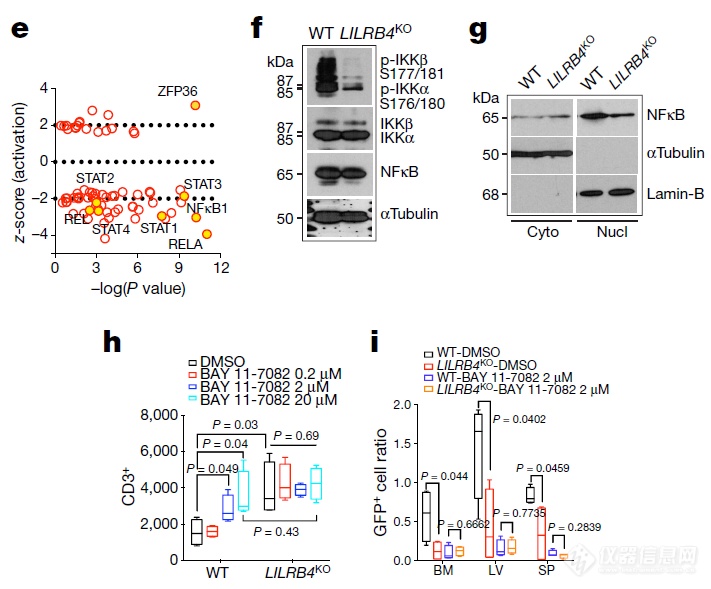
RNA测序比较野生型和LILRB4缺陷型细胞,由找到了另一个位于LILRB4下游的信号,使用该信号抑制剂BAY11可解除对T细胞的抑制、减少浸润
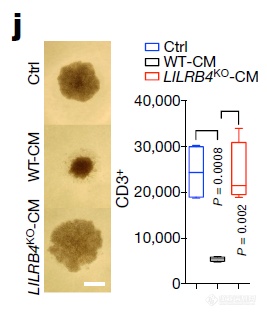
LILRB4、APOE、SHP-2都是肿瘤细胞上的,LILRB4肿瘤细胞可抑制T细胞,但这个作用必须通过特定物质传递到T细胞,野生型肿瘤细胞产生的条件培养基可抑制T细胞的增殖,看LILRB4缺陷型的肿瘤细胞的条件培养基无明显抑制作用
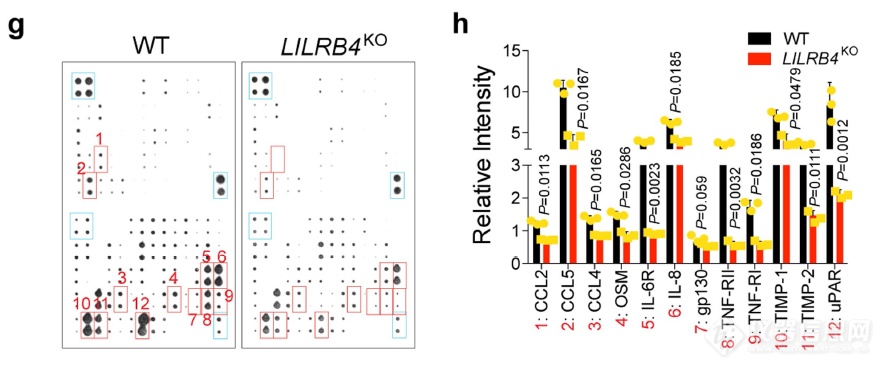
找肿瘤细胞条件培养基中发挥T细胞抑制作用的的组分,比对发现两种条件培养基中又一系列蛋白含量存在差异
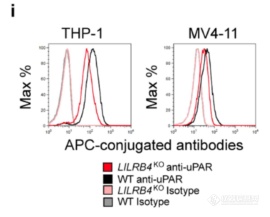
敲掉肿瘤细胞LILRB4后,uPAR在肿瘤细胞表面的表达降低
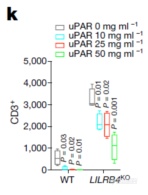
LILRB4缺陷肿瘤细胞和T细胞共培养体系中加入uPAR可抑制T细胞的生长,暗示uPAR在LILRB4抑制信号下游,即便没有LILRB4扔可抑制T细胞增殖
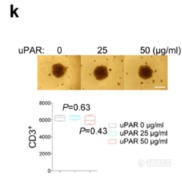
向T细胞培养体系中添加uPAR并不会抑制T细胞增殖,说明uPAR需作用在肿瘤细胞之后才可发挥抑制作用
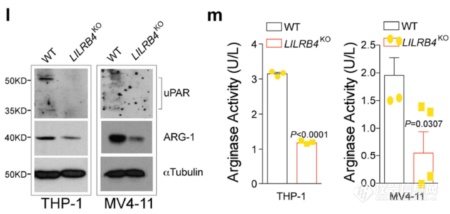
LILRB4敲除后,uPAR表达会下调,同时ARG-1也会下调,且活性降低
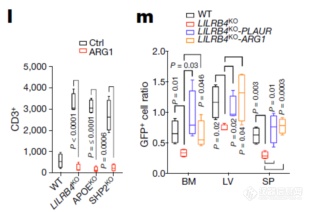
ARG-1可不依赖APOE、LILRB4、SHP-2发挥抑制T细胞增殖、促进肿瘤细胞浸润的作用 – 终于找到了LILRB4信号的“效应分子”
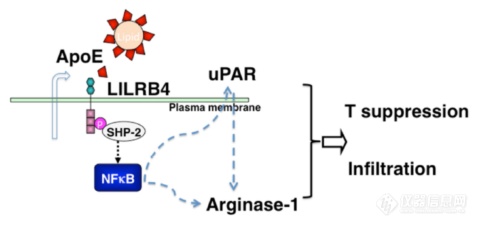
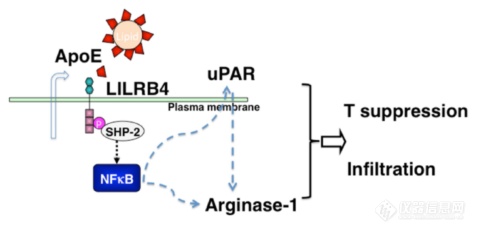
做了这么多工作就是这么一张图:肿瘤细胞上APOE激活LILRB4后SHP-2磷酸化,NFkB信号激活,uPAR表达升高,ARG-1升高,最终抑制T细胞、促进肿瘤细胞浸润
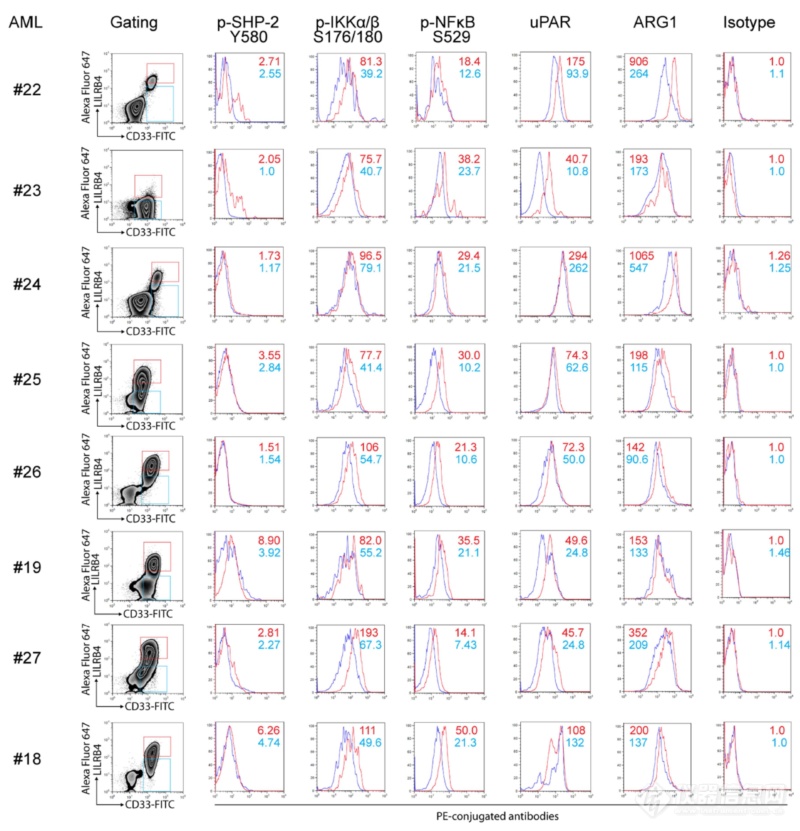
流式是个很好的技术 – 把LILRB4信号关键节点一次都给测了!
文章始于数据库检索分析,根源是对大数据的把握!找到信息点后按照分子生物学的思路顺藤摸瓜,滤清了一条免疫抑制信号 – 生命体的一切行为都有其分子基础,这就是规律,就是套路……
Mi Deng, Xun Gui, Jaehyup Kim, Li Xie, Weina Chen et al. LILRB4 signalling in leukaemia cells mediates T cell suppression and tumour infiltration.[J] .Nature, 2018.
想了解更多CNS级期刊最新内容,请关注我们的公众号,常有更新哦,也可加笔者微信交流:qianle522568!
酶标仪科普专栏丨第二期:荧光偏振(FP)介绍及应用
从分子到疾病:线粒体动力学研究取得新突破
【会议预告】第三届 3D 细胞类器官应用与高内涵成像技术研讨会邀您参加
开学啦|新学期,“心”守护实验室仪器免费巡检报名名额领取中
相关产品
上海美谱达UV-3200扫描型紫外/可见分光光度计
Leica徕卡DM750M正置显微镜
希森美康ExoCounter 全自动外泌体分析仪
智能化共聚焦高内涵成像分析系统
比利时 Bioruptor plus非接触式全自动超声破碎仪
DM3000德国徕卡leica生物显微镜
徕卡生物倒置显微镜LeicaDMi1
希森美康ExoCounter 全自动外泌体分析仪
梅特勒托利多pH 复合电极 LE438
Diagenode全自动核酸剪切仪Megaruptor ®3
化学发光成像仪Amersham ImageQuant 800
BIORUPTOR超声波细胞破碎仪new pico比利时Diagenode
美国博勒飞AMETEK Brookfield CTX质构仪
美国思拓凡 cytiva go蛋白纯化系统
ATS超高压均质机AH-D400

关注

拨打电话

留言咨询