空间蛋白组学技术——肿瘤微环境研究利器
导读:型的空间蛋白组学技术,则能两者兼顾,获得数十上百种蛋白标记的单细胞水平的空间表达,从而能更好的帮助科研工作者揭示复杂系统在疾病发生发展中的作用。
过去,受制于传统的研究方法,科研工作者很难对肿瘤微环境这样的复杂整体系统进行深入的研究和分析。要么选择包含空间信息的低通量标记技术,例如免疫荧光标记,要么选择高通量的蛋白标记,例如流式细胞技术,但是没有办法获得空间信息。近年来,新型的空间蛋白组学技术,则能两者兼顾,获得数十上百种蛋白标记的单细胞水平的空间表达,从而能更好的帮助科研工作者揭示复杂系统在疾病发生发展中的作用,其中最为显著的是推进了科研工作者对于免疫系统及其在癌症中作用的理解。
图一为冰冻切片的HER2+乳腺癌患者样本,扫描视野大约15 mm2,共标记了21种蛋白。如图所示,大多数肿瘤细胞(Pan-CK+)都同时表达HER2,表明该样本是一例上皮来源的恶性肿瘤组织。然而,在样本上同样发现了保有相对正常组织结构的正常上皮(Pan-CK+/HER2-)区域。

图1:HER2+乳腺癌组织的免疫多标记染色
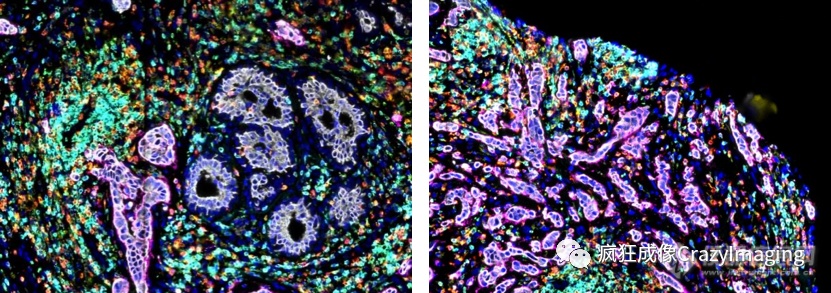
图1A:Pan-CK+/HER2- 图1B:Pan-CK+/HER2+
所有的21种蛋白标记(用不同颜色区分),可以对样本的不同区域进行细胞表型分析,图2为细胞密度相对较低的区域,便于区分各个标记蛋白。我们可以看到,单个肿瘤细胞会表达Pan-CK,EpCAM,HER2蛋白。

图2:21-plex超多标记的组织切片成像
通过单细胞分辨率的图像数据,再借由AI的全自动细胞分割,并定量分析各个蛋白的表达,从而进行细胞表型的分选(图3),同时也可以获得各类细胞的表达占比情况(图4)。
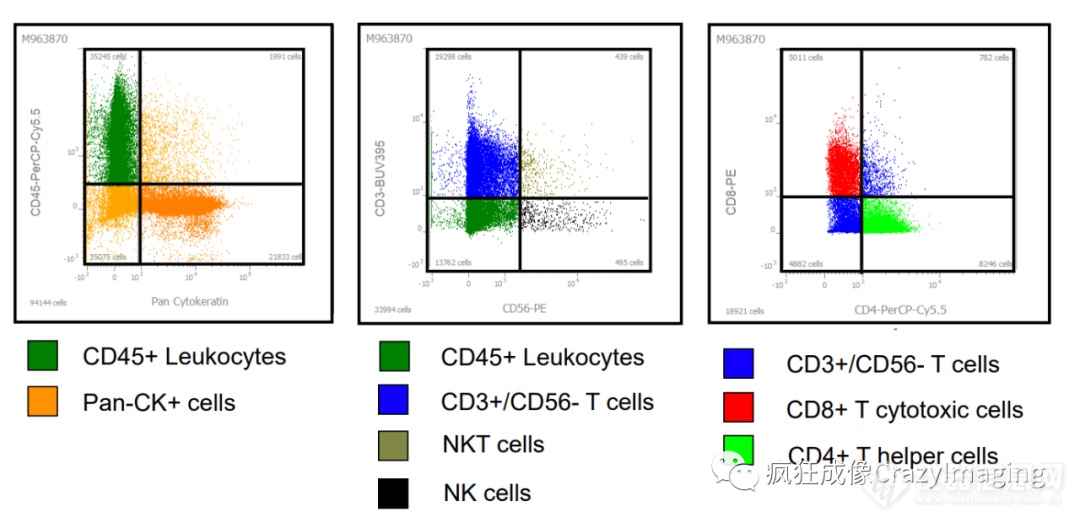
图3:细胞表型分析散点图
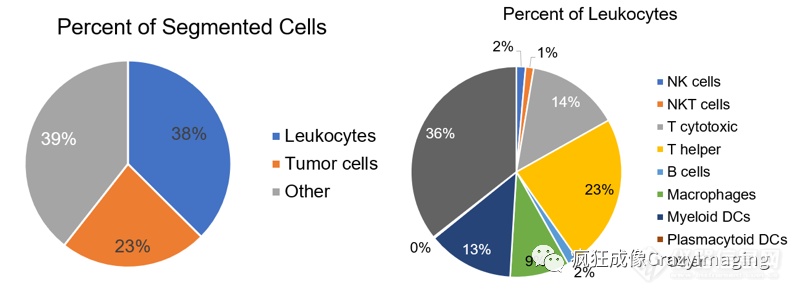
图4:各类细胞的表达占比
在非小细胞肺癌的肿瘤免疫学研究中,科研工作者同样利用单细胞空间蛋白组学技术,通过26-plex的蛋白标记,量化了样本中三十多类细胞的表型及亚型。从而揭示了非小细胞肺癌中免疫细胞侵润的异质性,并进行了量化分析。
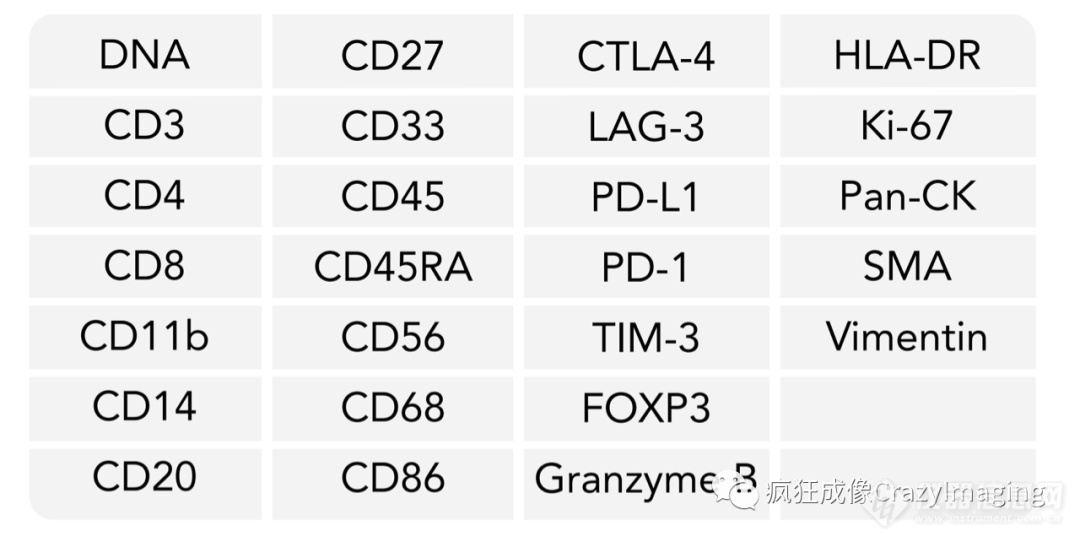
图表1:26种生物标记物列表
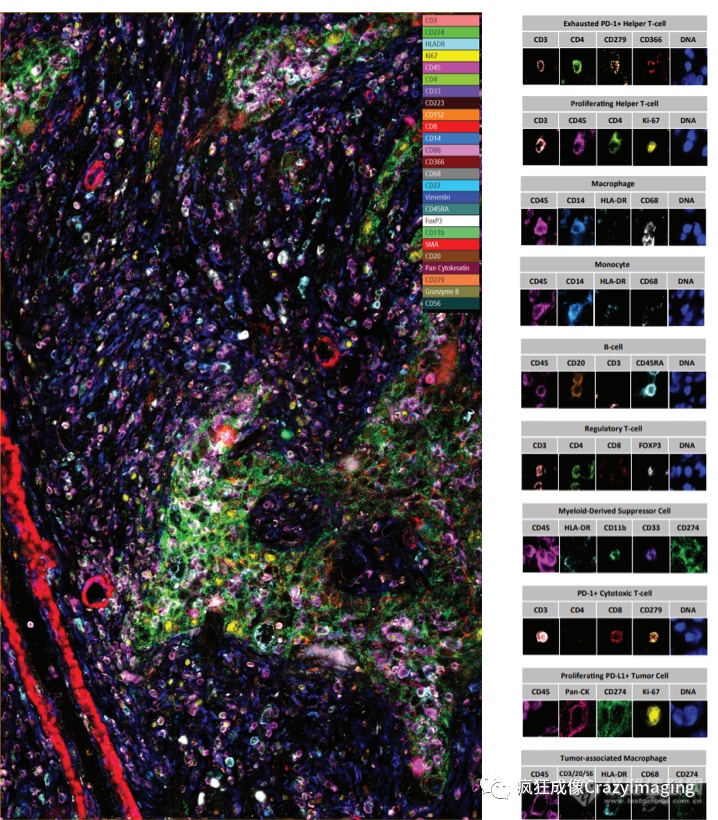
图5:肺癌样本的局部视野及细胞表型
如图5所示,肿瘤基质和肿瘤细胞附近有明显的髓样细胞浸润,而T细胞主要在肿瘤区域外聚集。 进一步的细胞定量分析发现,被认为在许多癌症中发挥促肿瘤作用的髓样细胞,具有高表达量。随后的空间分析,对肿瘤微环境中的T细胞和髓样细胞群进行了定量研究(图6),揭示了该细胞及其相关细胞类型的分布密度。
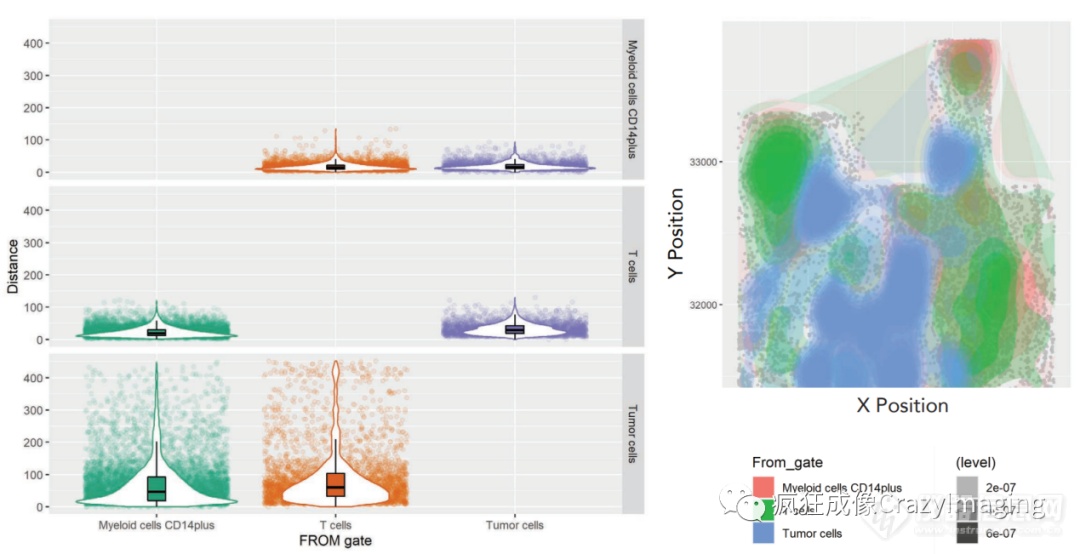
图6:T细胞及髓样细胞的空间分析
空间蛋白组学的应用,保留了组织形态和结构,又能一次性进行多种生物标记,从而能在分析复杂系统的细胞表型的同时,获得各类细胞的空间信息,更为深入的研究免疫系统及其在疾病中的作用。如图7展示的全视野的石蜡阑尾组织样本的成像,用14种生物标记物标记了免疫细胞及上皮细胞。之后分别对淋巴结(图7A)和粘膜上皮(图7B)这两个特定结构进行细胞表型分析。
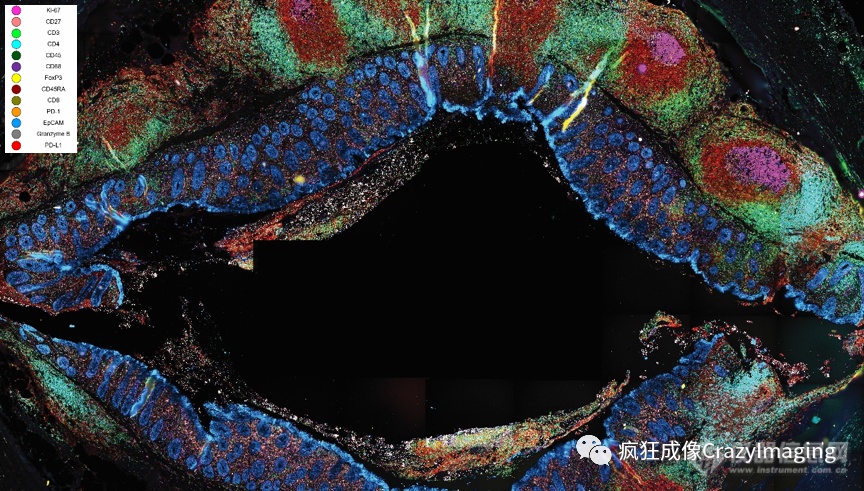
图7:石蜡阑尾组织样本的全视野超多标记成像
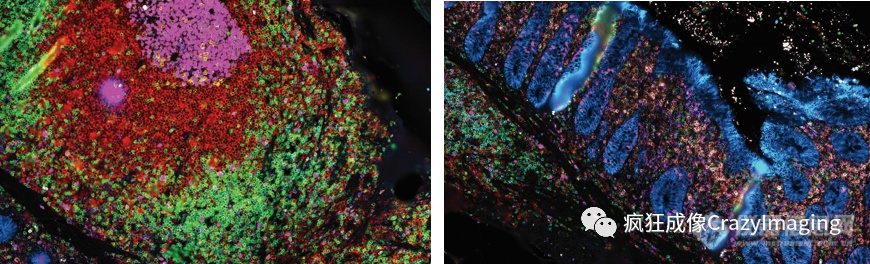
图7A:淋巴结局部视野 图7B:粘膜上皮局部视野
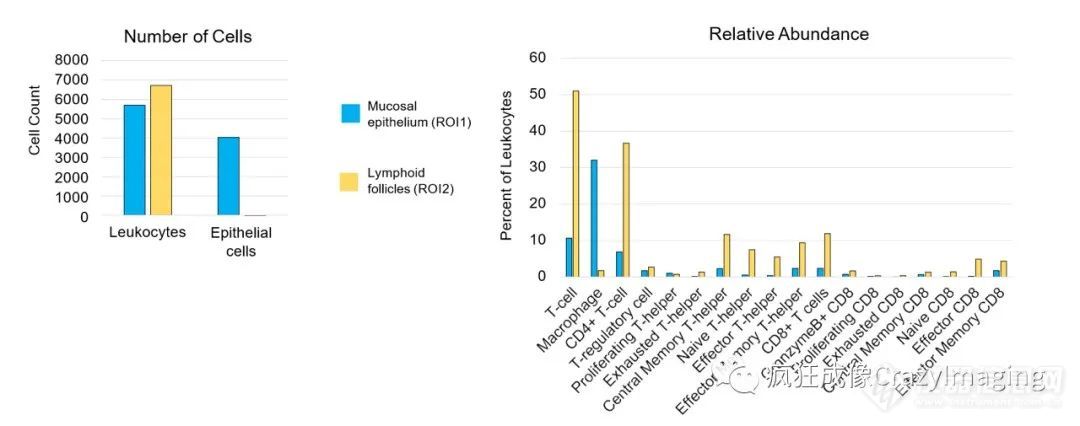
针对粘膜上皮区域和富含免疫细胞的淋巴结结构,对细胞数量及类型做了定量和表型分析(图表2),全面的揭示了临床组织样本不同区域和结构的免疫微环境差异。
图表2:组织特异性的细胞量化和表型分析
除了石蜡和冰冻组织样本,超多标记技术还可以应用于多种特殊的液体样本,例如脑脊液,痰液(图8)/支气管肺泡灌洗液(BAL)或者是用于循环肿瘤细胞的检测。不同于传统的流式细胞技术的样本需要即时处理,并且实验也需要一次性完成的特点,新型的空间蛋白组学技术,能够保存长达2年的样本活性,期间可以进行反复的标记和成像。这一特性为稀有样本和复杂实验,提供了强大的助力。
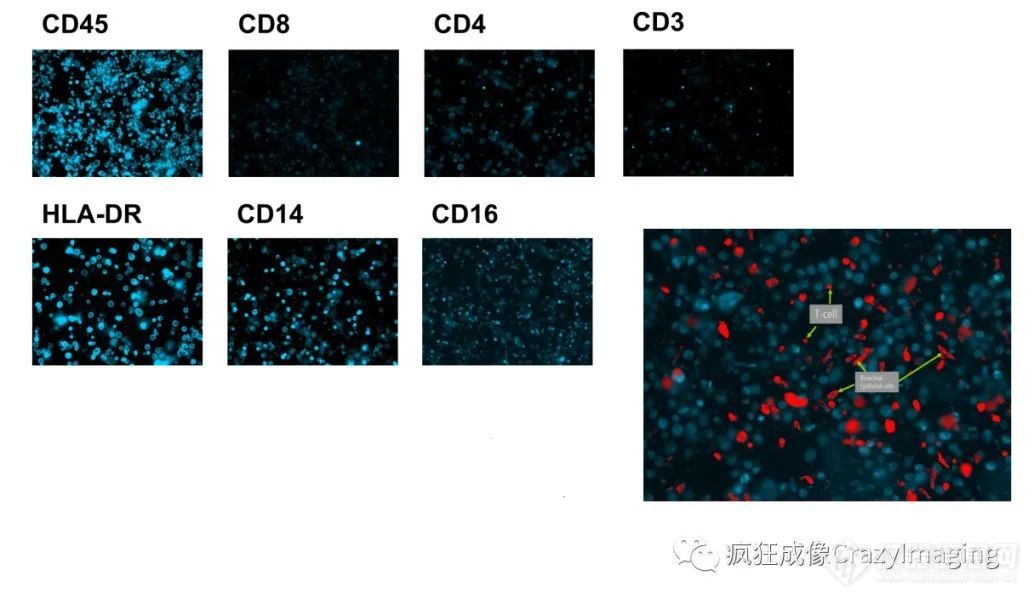
图8:对保存9天的人痰液细胞进行的六色免疫多标记成像
过去,受制于传统的研究方法,科研工作者很难对肿瘤微环境这样的复杂整体系统进行深入的研究和分析。要么选择包含空间信息的低通量标记技术,例如免疫荧光标记,要么选择高通量的蛋白标记,例如流式细胞技术,但是没有办法获得空间信息。近年来,新型的空间蛋白组学技术,则能两者兼顾,获得数十上百种蛋白标记的单细胞水平的空间表达,从而能更好的帮助科研工作者揭示复杂系统在疾病发生发展中的作用,其中最为显著的是推进了科研工作者对于免疫系统及其在癌症中作用的理解。
图一为冰冻切片的HER2+乳腺癌患者样本,扫描视野大约15 mm2,共标记了21种蛋白。如图所示,大多数肿瘤细胞(Pan-CK+)都同时表达HER2,表明该样本是一例上皮来源的恶性肿瘤组织。然而,在样本上同样发现了保有相对正常组织结构的正常上皮(Pan-CK+/HER2-)区域。

图1:HER2+乳腺癌组织的免疫多标记染色
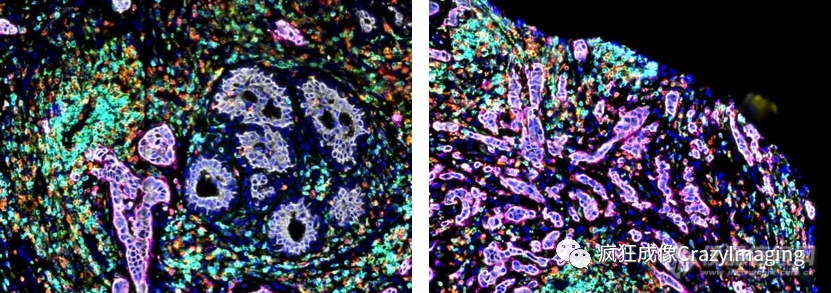
图1A:Pan-CK+/HER2- 图1B:Pan-CK+/HER2+
所有的21种蛋白标记(用不同颜色区分),可以对样本的不同区域进行细胞表型分析,图2为细胞密度相对较低的区域,便于区分各个标记蛋白。我们可以看到,单个肿瘤细胞会表达Pan-CK,EpCAM,HER2蛋白。

图2:21-plex超多标记的组织切片成像
通过单细胞分辨率的图像数据,再借由AI的全自动细胞分割,并定量分析各个蛋白的表达,从而进行细胞表型的分选(图3),同时也可以获得各类细胞的表达占比情况(图4)。
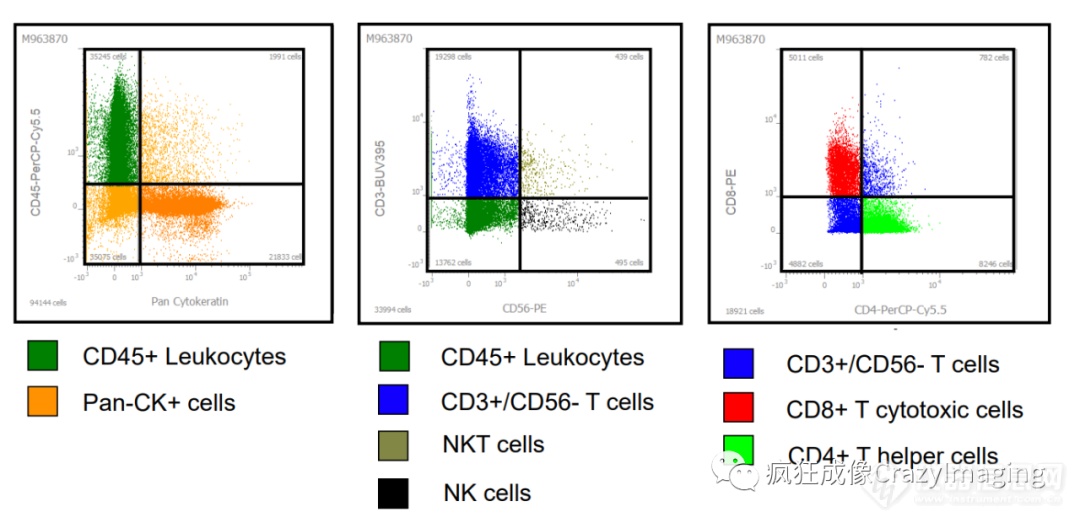
图3:细胞表型分析散点图
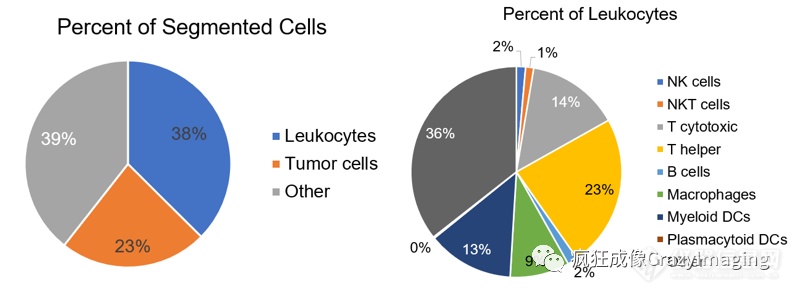
图4:各类细胞的表达占比
在非小细胞肺癌的肿瘤免疫学研究中,科研工作者同样利用单细胞空间蛋白组学技术,通过26-plex的蛋白标记,量化了样本中三十多类细胞的表型及亚型。从而揭示了非小细胞肺癌中免疫细胞侵润的异质性,并进行了量化分析。
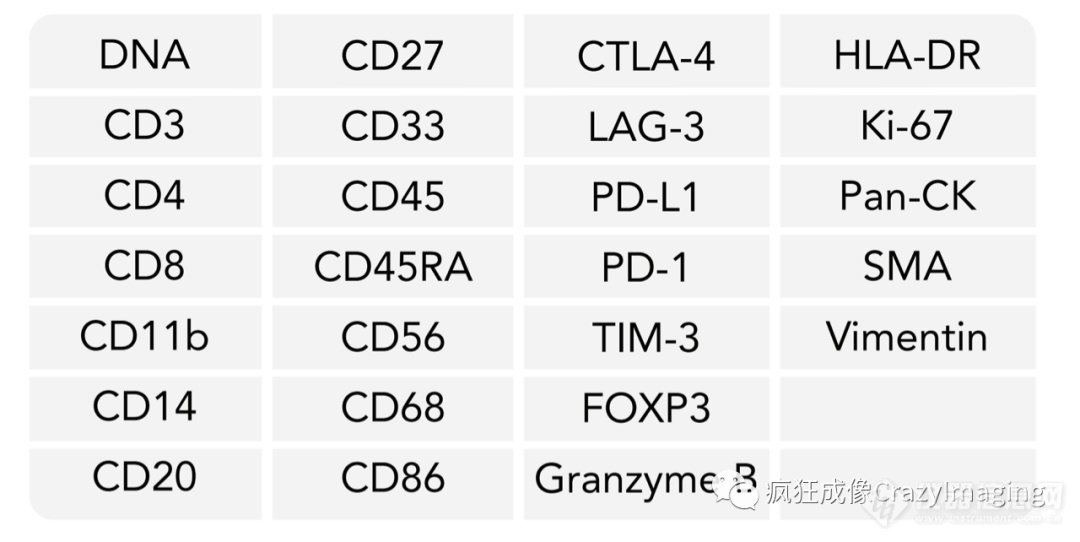
图表1:26种生物标记物列表
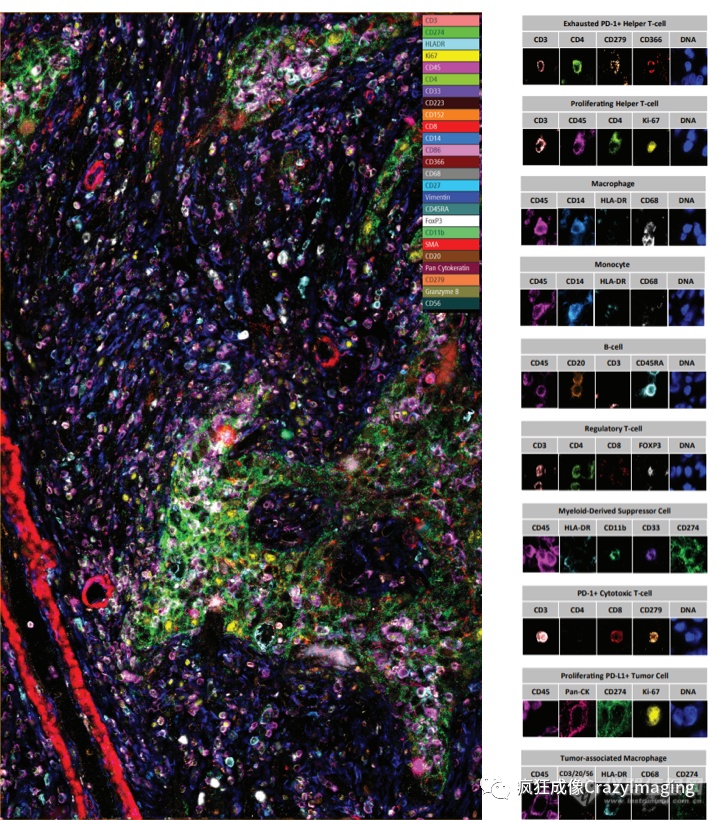
图5:肺癌样本的局部视野及细胞表型
如图5所示,肿瘤基质和肿瘤细胞附近有明显的髓样细胞浸润,而T细胞主要在肿瘤区域外聚集。 进一步的细胞定量分析发现,被认为在许多癌症中发挥促肿瘤作用的髓样细胞,具有高表达量。随后的空间分析,对肿瘤微环境中的T细胞和髓样细胞群进行了定量研究(图6),揭示了该细胞及其相关细胞类型的分布密度。
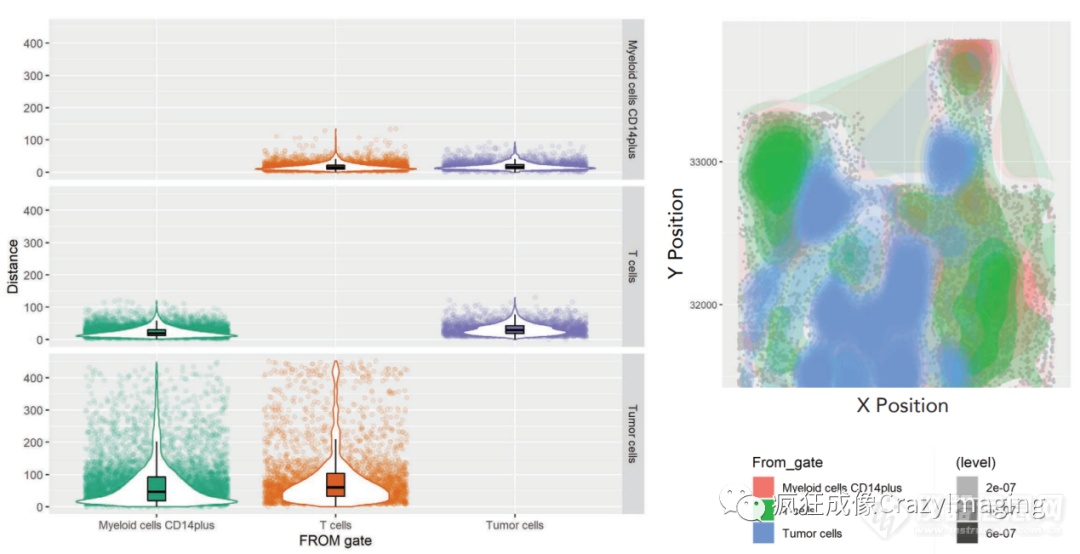
图6:T细胞及髓样细胞的空间分析
空间蛋白组学的应用,保留了组织形态和结构,又能一次性进行多种生物标记,从而能在分析复杂系统的细胞表型的同时,获得各类细胞的空间信息,更为深入的研究免疫系统及其在疾病中的作用。如图7展示的全视野的石蜡阑尾组织样本的成像,用14种生物标记物标记了免疫细胞及上皮细胞。之后分别对淋巴结(图7A)和粘膜上皮(图7B)这两个特定结构进行细胞表型分析。
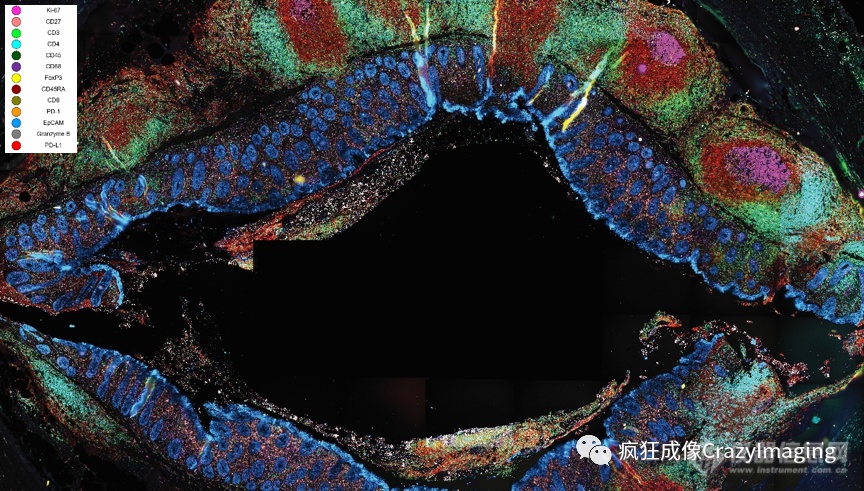
图7:石蜡阑尾组织样本的全视野超多标记成像
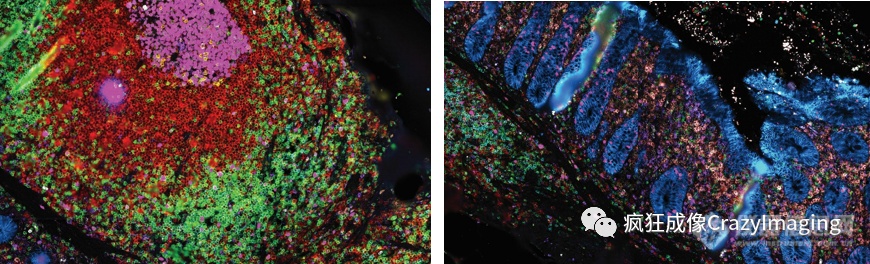
图7A:淋巴结局部视野 图7B:粘膜上皮局部视野
针对粘膜上皮区域和富含免疫细胞的淋巴结结构,对细胞数量及类型做了定量和表型分析(图表2),全面的揭示了临床组织样本不同区域和结构的免疫微环境差异。
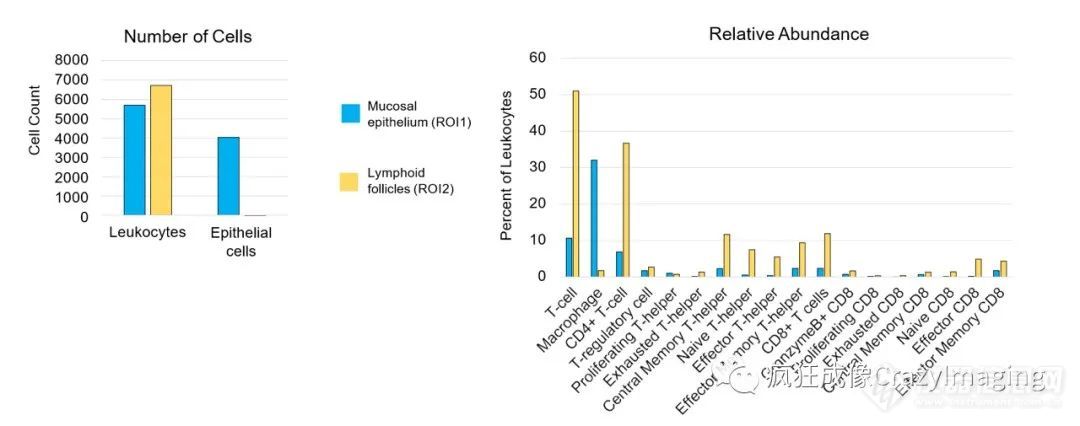
图表2:组织特异性的细胞量化和表型分析
除了石蜡和冰冻组织样本,超多标记技术还可以应用于多种特殊的液体样本,例如脑脊液,痰液(图8)/支气管肺泡灌洗液(BAL)或者是用于循环肿瘤细胞的检测。不同于传统的流式细胞技术的样本需要即时处理,并且实验也需要一次性完成的特点,新型的空间蛋白组学技术,能够保存长达2年的样本活性,期间可以进行反复的标记和成像。这一特性为稀有样本和复杂实验,提供了强大的助力。
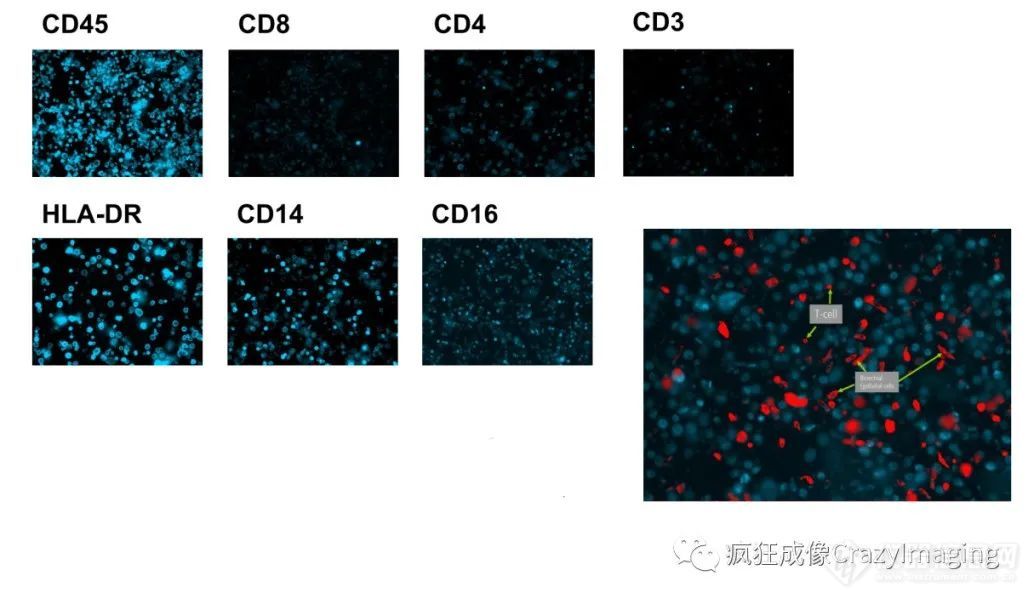
图8:对保存9天的人痰液细胞进行的六色免疫多标记成像
来源于:疯狂成像CrazyImaging
热门评论
最新资讯
新闻专题
更多推荐















