新型铜催化剂实现高效手性硫分子合成!
导读:研究开发了一种高效的手性硫分子合成方法,通过设计特定配体的铜催化剂,实现了高对映选择性的芳基硫氨基合成,为药物化学和有机合成提供了新工具。
【研究背景】
随着手性分子在药物开发和有机合成中的重要性日益增加,开发具有高对映选择性的合成方法成为了化学研究的热点。手性硫分子,特别是硫氨基(sulfilimines),由于其独特的立体中心和潜在的生物活性,正在受到越来越多的关注。硫氨基是一类具有S(IV)立体中心的手性分子,其在药物化学中表现出显著的应用价值,但其合成方法仍面临诸多挑战。现有的合成策略通常依赖于对立体差异的催化分辨,但对对映体选择性的控制仍然存在困难,尤其是在芳基和烷基硫氨基的合成中尤为如此。
为了应对这些挑战,Chan–Lam偶联反应作为一种有效构建C–N、C–O和C–S键的方法,在合成化学中得到了广泛应用。然而,在以往的研究中,Chan–Lam偶联反应在控制手性硫中心的构建方面仍然面临困难。传统的方法多依赖于底物的立体选择性,但对于芳基硫氨基的合成,尤其是当底物的芳基基团较为相似时,成对的对映体选择性较低。尽管有一些新的方法尝试克服这一难题,但普遍存在对映选择性不足或需要复杂的前体合成。
为了解决这些问题,南方科技大学贾铁争以及美国宾夕法尼亚大学Madeline E. Rotella,Marisa C. Kozlowski等携手通过引入了一种新的、高度化学选择性和对映选择性的Chan–Lam偶联反应方法。作者设计并合成了一种基于2-吡啶基N-苯基二氢咪唑配体的铜催化剂,这一催化剂能够在定义明确的手性环境中有效地控制反应的对映选择性。通过这一方法,作者能够在不需要额外制备对映体配体的情况下,实现对芳基硫氨基的高对映选择性合成。这一新方法不仅简化了催化剂的使用,还显著提高了硫氨基的立体选择性和化学选择性。
此外,作者的研究还揭示了反应机制,说明了在反应过程中Cu(II)络合物的分解作用如何影响化学选择性,而优异的对映选择性则源于过渡态之间的熵差异。作者的方法在合成了两个专利生物活性分子的硫氨基类似物方面表现出了优良的实用性。这一研究成果为制备手性骨架的药物化学和有机合成提供了新的强有力的工具,并且预计将推动相关领域的进一步发展。

【表征亮点】
1. 实验首次展示了一种高度化学选择性和对映选择性的Chan–Lam偶联反应,将硫氨酯与芳基硼酸酯进行偶联,成功合成了一系列包含立体氯原子的芳基和烷基芳基硫氨基。
2. 实验通过使用特意设计的2-吡啶基N-苯基二氢咪唑配体生成的铜催化剂实现了有效的对映选择性。该催化剂通过提供明确的手性环境和高反应性,能够超越背景的外消旋转化,从而合成了高对映纯度的硫氨基。该策略避免了使用不自然的d-氨基酸制备对映体配体的需求,使得单一手性配体能够通过交换硫氨基和芳基硼酸酯底物的芳基来生成任意对映体。
3. 2-吡啶基保护基可以从产物中去除,进一步转化为S(IV)和S(VI)衍生物,同时保持对映纯度。这一策略的合成实用性得到了两个专利生物活性分子的硫氨基类似物合成的验证,展示了其在药物化学中的应用潜力。
4. 结合实验数据和计算研究,揭示了化学选择性偏向C–S键而非C–N键的原因,这主要由于Cu(II)络合物的还原前的分解作用。此外,优异的对映选择性源于过渡态之间的熵差异。此方法为药物化学和有机合成中的手性骨架制备提供了强有力的工具。
【图文解读】
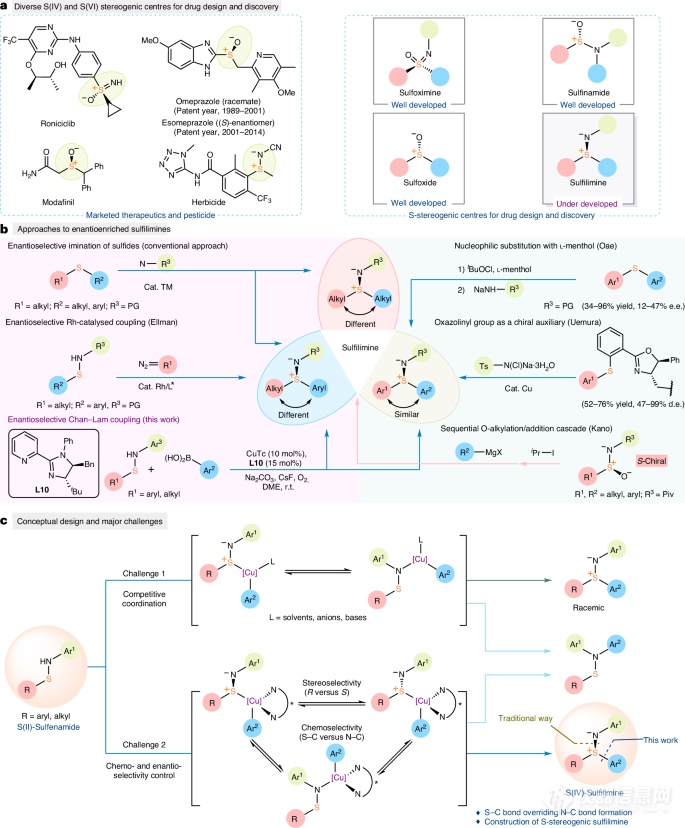
图1:研究背景和概念设计。
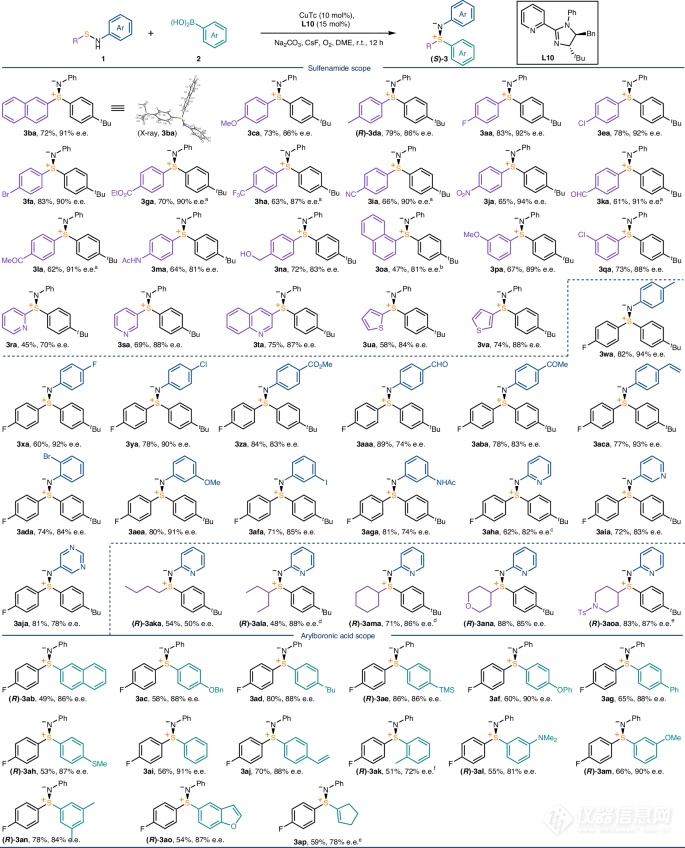
图2:基底范围。
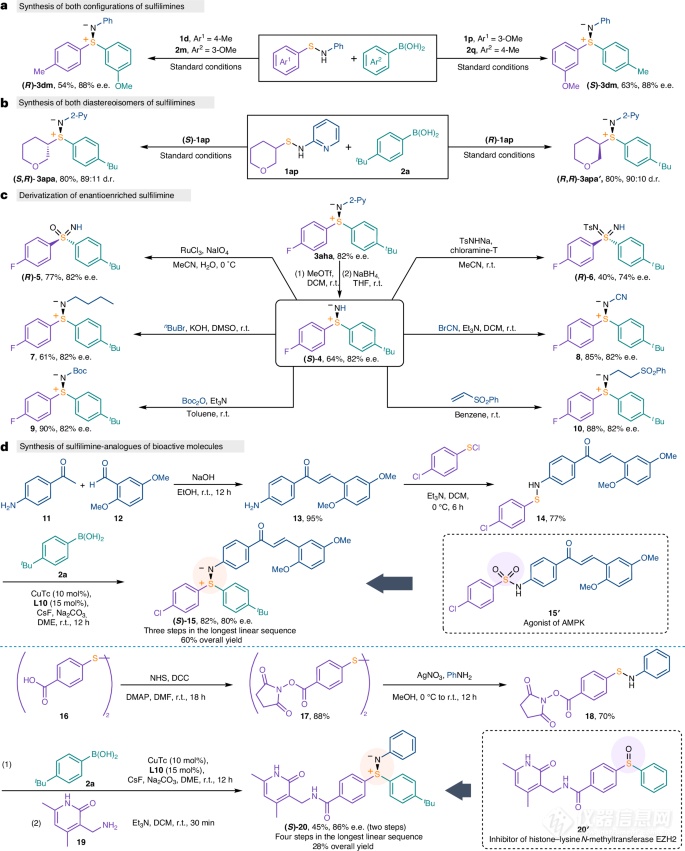
图3:合成应用。
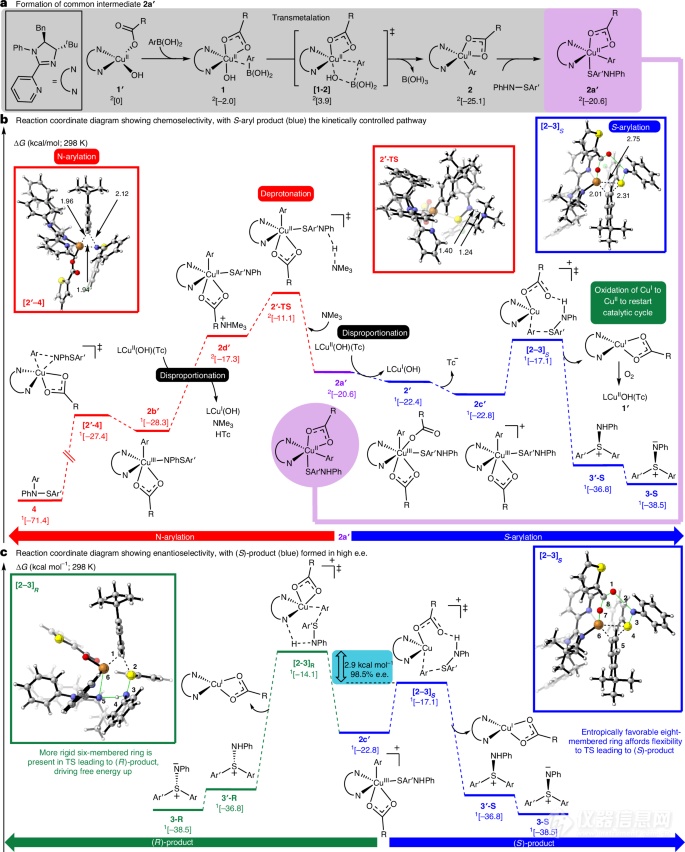
图4: 反应机理的计算研究。
【科学启迪】
总之,作者介绍了一种高度化学选择性和对映选择性的Chan–Lam偶联反应,将硫氨酯与芳基硼酸酯反应,合成了一系列含有立体氯原子的芳基和烷基芳基硫氨基。这一过程使用了由特意设计的2-吡啶基N-苯基二氢咪唑配体生成的铜催化剂,该催化剂通过提供明确的手性环境和高反应性来实现有效的对映选择性,能够超越背景的外消旋转化。该策略使得单一的手性配体可以通过交换硫氨基和芳基硼酸酯底物的芳基来产生任意的对映体,从而避免了使用不自然的d-氨基酸制备对映体配体的需求。2-吡啶基保护基可以从产物中去除,从而可方便地转化为S(IV)和S(VI)衍生物,并保持对映纯度。此外,该不对称偶联的合成实用性得到了两个专利生物活性分子的硫氨基类似物合成的验证。结合实验数据和计算研究揭示了化学选择性偏向C–S键而非C–N键的原因,这主要是由于Cu(II)络合物的还原前的分解作用。此外,优异的对映选择性源于过渡态之间的熵差异。本文描述的方案代表了对映选择性的Chan–Lam偶联反应,预计将成为药物化学和有机合成中制备手性骨架的有力工具。
参考文献:Liang, Q., Zhang, X., Rotella, M.E. et al. Enantioselective Chan–Lam S-arylation of sulfenamides. Nat Catal (2024). https://doi.org/10.1038/s41929-024-01213-5
来源于:仪器信息网
热门评论
最新资讯
新闻专题
更多推荐