推荐厂家
暂无
暂无
 金牌5年
金牌5年
 400-860-5168转4265
400-860-5168转4265
 留言咨询
留言咨询
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-885-9293
400-885-9293
 留言咨询
留言咨询

 400-885-9293
400-885-9293
 留言咨询
留言咨询

 400-885-9293
400-885-9293
 留言咨询
留言咨询




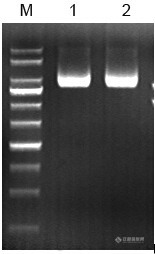
利用硅胶膜法提取纯化质粒DNA摘要:系统的阐述了质粒核酸提取过程中针对裂解和核酸纯化两大关键步骤的研究,重点介绍了利用硅胶膜法提取纯化核酸,以及在实验过程中的一些经验。关键词:硅胶膜法;纯化;质粒DNA一、前言随着分子生物学技术的发展,核酸的分子生物学技术成为了药物研发、遗传病和感染性疾病的诊断、基因研究及物种鉴定等的常用研究手段之一。然而,核酸提取质量是进行下游一系列研究的关键,因此提取的方法会直接影响后续实验。细菌质粒是一类双链闭合环状的DNA,大小范围从1kb至200kb以上不等。各种质粒都是存在于细胞质中、独立于细胞染色体之外的自主复制的遗传成份。质粒已成为目前最常用的基因克隆的载体分子,重要的条件是可获得大量纯化的质粒DNA分子。硅胶膜法是一种应用最为广泛的提取纯化质粒DNA的方法,因硅基质材料可特异吸附核酸DNA,使用方便、快捷,不需要使用有毒溶剂如酚、氯仿等,使得提取质粒核酸像过滤一样简单。二、实验部分2.1 原理硅基质材料吸附核酸的原理主要利用DNA在高盐低pH值环境下与硅基质材料相结合,在低盐高pH值环境下与硅基质材料脱离的特征。其机理是带负电荷的DNA和带正电的二氧化硅粒子之间有很强的亲和力。在高浓度盐离子的作用下,盐离子打破水中的氢和二氧化硅上带负电荷的氧离子间的氢键,DNA与硅基质紧密结合,洗涤除去其他杂质;再用低离子强度的TE缓冲液或蒸馏水洗脱结合的DNA分子,机理是当盐被清除后,再水化的硅基质破坏了基质和DNA之间的吸引力,因而DNA从硅基质上被洗脱下来。2.2 主要试剂溶液Ⅰ:50mM葡萄糖,25mM Tris-HCl(pH 8.0),10mM EDTA(pH 8.0)。溶液Ⅱ:0.2NNaOH,1% SDS。溶液Ⅲ:醋酸钾(KAc)缓冲液,pH 4.8。漂洗液:60mM 乙酸钾、10mM Tris-HCl (pH 7.5) 、60% 乙醇TE:10mMTris-HCl(pH 8.0),1mM EDTA(pH 8.0)。2.3 主要步骤该步骤采用CommaPrePTM的质粒小提纯化柱。http://ng1.17img.cn/bbsfiles/images/2015/07/201507171513_556042_3310_3.jpgCommaPrep™核酸小提柱可用在核酸提取过程中过柱结合、洗涤、洗脱步骤中http://ng1.17img.cn/bbsfiles/images/2015/07/201507171516_556043_3310_3.jpg1. 取1.5ml过夜培养的菌液,加入离心管中,使用常规台式离心机,12,000 rpm 离心1 min, 尽量吸除上清。 (注意:应根据所培养菌体的浓度与质粒的拷贝数,确定收集的菌液量。菌量过大可能导致溶菌不充分,纯化时会影响质粒纯度菌液较多时可以通过多次离心将菌体沉淀收集到一个离心管中)。2. 将细菌沉淀重悬于100uL溶液Ⅰ中,移液器或涡旋振荡器彻底悬浮细菌沉淀,使菌体分 散混匀。 (注意:如果有未彻底混匀的菌块,会影响裂解,导致提取量和纯度偏低。并且溶液Ⅰ中 要加入适量的RNA酶)3. 向离心管中加入200uL溶液Ⅱ,温和地上下翻转数次,并将离心管放置于冰上2-3min,使细胞膜裂解。(注意:温和地混合,不要剧烈震荡,以免污染基因组DNA。此时菌液应变得清亮,如果未变得清亮,可能由于菌体过多,裂解不彻底,应减少菌体量。)4. 加入150uL溶液Ⅲ,立即将管温和颠倒数次混匀,见白色絮状沉淀。12000rpm, 离心2分钟。 (注意:加入溶液Ⅲ后,要立即将管温和颠倒,避免产生局部沉淀。如果上清液中存在沉淀,可再一次离心。溶液Ⅲ为中和溶液,此时质粒DNA复性,染色体和蛋白质不可逆变性,形成不可溶复合物。)5. 吸取上清至吸附柱(内管)中(吸附柱在离心管中),尽量不要吸出沉淀,12000rpm,离心30秒。弃去废液,将吸附柱重新放入一个新的离心管中。6. 加入750uL的漂洗液(漂洗液要在实验前加入无水乙醇)12000rpm离心,1min。取出 DNA结合柱,弃废液,重新插入DNA结合柱到离心管中。7. 用500uL漂洗液重复冲洗过程。12000rpm离心,1min。(注意:重复一次可以增加质粒的回收效率。)8. 转移DNA结合柱到1个新的1.5mL离心管中,加入60uL的无核酸酶的水到DNA结合柱中,洗脱质粒DNA,室温条件下,12000rpm离心,1min。 (注意:不要转入DNA结合柱中的漂洗液,如果混有,就需要12000rpm离心,1min。洗脱缓冲液体积不少于50uL,体积小会影响回收效率。 洗脱液的pH值对于洗脱效率有很大的影响,若用水洗脱应保证pH值在7.0-8.5范围内, pH小于7会降低洗脱效率。如果长期保存DNA,洗脱液建议使用TE。)9. 加入100uL的无核酸酶水到结合柱中,洗脱质粒DNA,离心12000rpm,1min。(注意:重复一次,增加洗脱效率。)10.洗脱DNA后,从1.5mL离心管中取出DNA结合柱并废弃。11.取2uLDNA进行电泳,检测DNA质量。12.将纯化的DNA溶液于-20℃中。三、实验结果图为质粒DNA(10kb)的凝胶电泳图,说明提取效果较好。http://ng1.17img.cn/bbsfiles/images/2015/07/201507171525_556044_3310_3.jpg
核酸提取(核酸的分离与纯化)主要是指将核酸与蛋白质、多糖、脂肪等生物大分子物质分开,但在分离核酸时,应保证核酸分子一级结构的完整性,并排除其他分子污染。核酸提取方法一般包括细胞裂解、酶处理、核酸与其他生物大分子物质分离、核酸纯化等几个主要步骤,而每一步骤又可由多种不同的方法单独或联合实现。操作过程中首先通过物理、化学或酶解作用裂解细胞,使核酸释放出来,并去除与核酸结合的蛋白质以及多糖、脂肪类等生物大分子的过程。在此基础上,沉淀核酸、去除盐类和有机试剂等杂质,从而得到纯化的核酸。核酸提取仪是应用配套的核酸提取试剂来自动完成样本核酸的提取工作的仪器。在传统的手工核酸提取过程中通常采用离心澄清的方法,操作时费时费力。近年来,出现了磁珠分离技术,利用磁珠在一定条件下对核酸具有很强亲和力的特点,吸附核酸。当条件改变时,磁珠又可以与其吸附的核酸分离,从而得到纯化的核酸。这种方法简便、高效、易于操作,是目前核酸提取仪采用的主要方法。具体来说,磁珠法提取核酸是通过细胞裂解液裂解细胞,从细胞中游离出来的核酸分子被特异的吸附到磁性颗粒表面,而蛋白质等杂质不被吸附而留在溶液中。反应一定时间之后,再在磁场作用下,使磁性颗粒与液体分开,回收颗粒(即磁珠-DNA 混合物),再用洗脱液洗脱即可以得到纯净的DNA。磁珠法不需要离心、不需要加入多种试剂,操作简单,符合核酸自动化提取要求,是未来核酸纯化方法发展的一个重要方向。
[size=3]选择材料及预处理 以蛋白质和结构与功能为基础,从分子水平上认识生命现象,已经成为现代生物学发展的主要方向,研究蛋白质,首先要得到高度纯化并具有生物活性的目的物质。蛋白质的制备工作涉及物理、化学和生物等各方面知识,但基本原理不外乎两方面。一是得用混合物中几个组分分配率的差别,把它们分配到可用机械方法分离的两个或几个物相中,如盐析,有机溶剂提取,层析和结晶等;二是将混合物置于单一物相中,通过物理力场的作用使各组分分配于来同区域而达到分离目的,如电泳,超速离心,超滤等。在所有这些方法的应用中必须注意保存生物大分子的完整性,防止酸、硷、高温,剧烈机械作用而导致所提物质生物活性的丧失。蛋白质的制备一般分为以下四个阶段:选择材料和预处理,细胞的破碎及细胞器的分离,提取和纯化,浓细、干燥和保存。 微生物、植物和动物都可做为制备蛋白质的原材料,所选用的材料主要依据实验目的来确定。对于微生物,应注意它的生长期,在微生物的对数生长期,酶和核酸的含量较高,可以获得高产量,以微生物为材料时有两种情况:(1)得用微生物菌体分泌到培养基中的代谢产物和胞外酶等;(2)利用菌体含有的生化物质,如蛋白质、核酸和胞内酶等。植物材料必须经过去壳,脱脂并注意植物品种和生长发育状况不同,其中所含生物大分子的量变化很大,另外与季节性关系密切。对动物组织,必须选择有效成份含量丰富的脏器组织为原材料,先进行绞碎、脱脂等处理。另外,对预处理好的材料,若不立即进行实验,应冷冻保存,对于易分解的生物大分子应选用新鲜材料制备。 蛋白质的分离纯化 一,蛋白质(包括酶)的提取 大部分蛋白质都可溶于水、稀盐、稀酸或碱溶液,少数与脂类结合的蛋白质则溶于乙醇、丙酮、丁醇等有机溶剂中,因些,可采用不同溶剂提取分离和纯化蛋白质及酶。 (一)水溶液提取法 稀盐和缓冲系统的水溶液对蛋白质稳定性好、溶解度大、是提取蛋白质最常用的溶剂,通常用量是原材料体积的1-5倍,提取时需要均匀的搅拌,以利于蛋白质的溶解。提取的温度要视有效成份性质而定。一方面,多数蛋白质的溶解度随着温度的升高而增大,因此,温度高利于溶解,缩短提取时间。但另一方面,温度升高会使蛋白质变性失活,因此,基于这一点考虑提取蛋白质和酶时一般采用低温(5度以下)操作。为了避免蛋白质提以过程中的降解,可加入蛋白水解酶抑制剂(如二异丙基氟磷酸,碘乙酸等)。下面着重讨论提取液的pH值和盐浓度的选择。[/size]