推荐厂家
暂无
暂无

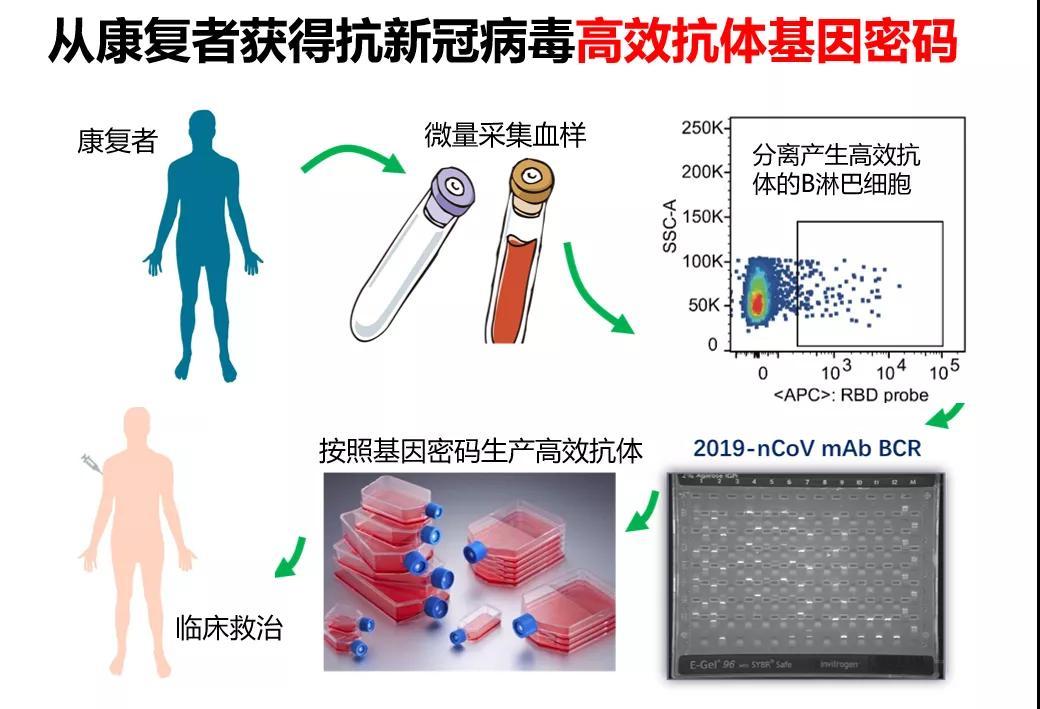




新华社巴黎9月11日电 英国医学刊物《柳叶刀》11日刊登的报告说,临床试验结果表明,法国疫苗生产商赛诺菲—巴斯德公司研发的登革热疫苗对3种登革热病毒株有预防效果,是一种安全有效的登革热疫苗。 登革热是一种由蚊子传播的急性病毒性传染病,多在热带地区传播,典型症状包括发烧、头痛和关节痛。登革热病毒有4种血清型,人体受到其中任何一种感染后不会对其他3种产生抵抗力。迄今尚无专门预防登革热的疫苗投入使用。 法国赛诺菲—安万特集团旗下从事疫苗研发和生产的赛诺菲—巴斯德公司11日发表公报说,在泰国进行的针对4000多名4岁至11岁儿童的二期临床试验结果表明,该公司研发的疫苗对3种登革热病毒株有预防效果,研究人员正在分析疫苗难以预防第四种病毒株的原因。 公报还说,该公司正在对10个亚洲和拉美国家的3.1万名儿童和青少年进行大规模的三期临床试验,以更好地了解该疫苗在不同流行病学环境下和在更广泛人群中的效力。 据世界卫生组织估计,全球每年有5000万至1亿人感染登革热,其中约50万例是较严重的出血性登革热病例,这种登革热的死亡率较高。 《柳叶刀》杂志认为,赛诺菲—巴斯德研发的“CYD-TDV”活性减毒疫苗有助于实现世卫组织提出的到2020年将登革热死亡率降低50%的目标。(记者 黄涵)

为广泛征求用户的意见和需求,了解中国科学仪器市场的实际情况和仪器应用情况,仪器信息网自2008年6月1日开始,将用两年的时间对不同行业有代表性的“100个实验室”进行走访参观。2009年4月25日,仪器信息网工作人员参观访问了本次活动的第十一站:解放军第三0七医院临床药理研究室。 解放军第三0七医院临床药理研究室(以下简称“临床药理室”)建立于1980年,是全军首家成立的临床药理学科;1986年被国家卫生部批准为国家临床药理基地,通过国家第一批GCP认证,并具备开展Ⅰ期临床试验的能力;1989年被指定为“全军新老药物临床评价中心”;2008年被确定为创新药物研究开发技术平台之“抗肿瘤新药临床研究评价技术平台”。[center][IMG]http://bimg.instrument.com.cn/lib/editor/UploadFile/20095/20095593210789.jpg[/IMG]刘泽源主任介绍解放军第三0七医院临床药理研究室[/center] 解放军第三0七医院临床药学部刘泽源主任及临床药理室郝光涛药师接待了仪器信息网工作人员。据刘泽源主任介绍,临床药理室现有工作人员14名,分为药代、药理两个研究组。目前,药代组每年开展20余项新药临床研究;药理组负责开展新药研制工作、承接合作单位的药理实验、进行血药浓度监测工作、承担国家或军队级别课题研究。此外,临床药理室还带教来自中南大学湘雅医学院、厦门大学药学院、天津医科大学等多所医科院校的实习生,接收来自全国及全军多家单位的工作人员在此进修学习。[center][img]http://ng1.17img.cn/bbsfiles/images/2009/06/200906051450_153936_1622715_3.jpg[/img]解放军第三0七医院临床药理研究室目前承担的科研课题[/center]
随着精准医学的发展、多组学研究上的突破,临床质谱迎来了发展机会。仪器信息网特别策划[color=#0070c0][url=https://www.instrument.com.cn/zt/CMS2022]“临床质谱技术及应用进展”专题[/url][/color],聚焦临床质谱新产品新技术及相关临床领域的最新应用,以增强业界相关人员之间的信息交流,展示更丰富的临床诊断质谱产品、技术解决方案。与生化、免疫等传统检测技术相比,临床质谱技术在灵敏度、特异性、多指标联检等方面具备独特优势。它既是生化、免疫等检测技术的补充,又是传统检测技术的延伸,可以提高现有检验项目的精准度,也可以检测其他技术不能检测的指标,能够更好地指导临床诊断,为患者提供更准确的检测结果。临床质谱技术正在新生儿遗传代谢病筛查、维生素检测、药物浓度监测、激素检测、微生物鉴定、微量元素检测等多个临床应用场景发挥着越来越重要的作用。[color=#ff0000]解决仪器和试剂适配问题是临床质谱落地路径 [/color]从商业模式角度来说,由于医疗服务体系和保险制度的不同,美国大部分质谱服务都是LDT模式(Laboratory Developed Test, 独立医学实验室),形成了像Quest和Labcorp这样的第三方服务龙头。美国60%以上的医学检验都是外包,医院只采样。而国内临床检验的市场主要还是以公立医院检验科为主,以第三方医学检验为辅的市场结构。大医院的检验科能力强,有能力在院内开展检测。同时,报告时间、政策监管及医院管理的需求,也更倾向样本在院内检测。因此,IVD模式(In Vitro Diagnosis,体外诊断)更适合中国。临近两年中国整个临床质谱行业发展非常迅猛,临床质谱这个赛道上涌入的企业也越来越多,资本的投资热度逐渐升高。由于临床看重的是检验性能和临床价值,需要仪器、试剂、服务一站式解决方案,而非单一的仪器。随着国内临床质谱企业增多,首先解决仪器和试剂的适配问题,成为打通质谱分析临床落地路径。[color=#ff0000]多组学背景下,临床质谱行业发展三大趋势[/color]在临床质谱几大技术平台中,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱是临床最为成熟的技术平台之一,布局企业多、仪器多、试剂多,是临床质谱市场的核心板块。在精准医疗技术迭代、临床需求持续扩大、多组学趋势背景下,临床质谱政策环境、资本环境等持续向好,临床质谱行业未来技术及应用整体呈现几大趋势:[b]1、以[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱为核心的多组学研究已成为各类疾病筛查、早期诊断、治疗监测和预后评估的生物标志物创新发现的关键应用平台。[/b]生命组学时代来临,临床质谱技术有望成为常规底层技术。疾病发生发展复杂,单一组学无法解决所有问题,已有大量研究表明依靠单一组学存在较大局限性,多组学在致病机理研究、疾病标志物与致病靶点筛选,以及早期诊断和治疗上都有着巨大的潜力,临床医学正在快速过渡至多组学整合分析。而组学研究样本复杂,通常样本中含有数十万个化合物,分子丰度低,对检测灵敏度要求极高,数据分析庞大,质谱技术多指标检测、高灵敏度、高特异性、高通量的特点非常契合多组学发展趋势,有望在多组学时代中大放异彩。相比基因组学和转录组学,蛋白质组学和代谢组学在精准诊断的普检和特检、精准治疗的创新药研发和伴随诊断中具有更加深远和广泛的意义。其中,蛋白质组学研究难度更高、与临床结合更为紧密、药物医学转化程度更高,是推动临床应用与医学转化的重中之重。[b]2、在应用场景上,常规检测应用成红海,针对大病种的精准诊疗将成为未来临床质谱主力市场。[/b][url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱临床应用分为两类,一类是常规检测应用,对现有方法学进行升级,如新生儿遗传代谢病筛查、药物浓度监测、维生素检测等,另一类是基于组学研究,开辟空白、创新应用场景,如慢病诊疗跟踪、肿瘤标志物发现等。随着我国临床质谱常规应用渗透率提高,新生儿遗传代谢病筛查、维生素检测等已成为红海市场,传统检验替代、大病种尤其是阿尔茨海默症、心血管病和肿瘤等疾病的精准诊疗将成为未来重要的临床质谱增量市场。[b]3、未来,各类质谱仪器会持续向国产替代方向发展。[/b]从近年来提出的精准医疗等热点可以得知,人们越发重视生活质量提升,实现精准医疗的目标就离不开[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析技术。由于现有的质谱属于高精尖仪器,需要专业人员操作和维护,且几乎依赖进口,无法满足我国对该技术日益增长的需求,质谱技术向国产化、POCT化、自动化方向发展是未来趋势,推动临床质谱市场成熟。我们相信,2020-2030年是生命组学时代,质谱技术将助推代谢组学、蛋白质组学等组学技术在精准医疗领域发挥重大作用。基于组学技术的疾病特检、伴随诊断未来将有大的发展。一个行业的持续发展需要构建良好的生态,虽然目前我国质谱行业还处于行业发展的早期阶段,但行业生态已经逐步形成。临床质谱产业链的全面发展,硬件厂家、试剂厂家、服务提供商的水平都在快速提升,医院、终端用户的需求日益增长,科研院校、医药企业的参与增多,生态中各种参与者之间的联系越来越紧密。

 400-877-2799
400-877-2799
 留言咨询
留言咨询

 400-877-2799
400-877-2799
 留言咨询
留言咨询

 400-803-1191
400-803-1191
 留言咨询
留言咨询