推荐厂家
暂无
暂无






菊苣酸是世界上广受欢迎的药用植物紫锥菊([b]Echinacea purpurea[/b] (L.) Menoch)的主要活性成分,被公认为商业热销紫锥菊产品的质量指标。虽然紫锥菊中菊苣酸的生物合成途径已被近期阐明,但其调控网络仍然不清楚。通过共表达和系统发育分析,该研究发现了[b]EpMYB2[/b],一个典型的R2R3型MYB转录因子(TF),对甲基茉莉酸甲酯(MeJA)刺激有响应,是菊苣酸生物合成的正调控因子。除了直接调控菊苣酸生物合成基因外,[b]EpMYB2[/b]还正向调控上游莽草酸途径的基因。我们还发现[b]EpMYC2[/b]可以通过结合其G-box位点激活[b]EpMYB2[/b]的表达,[b]EpMYC2-EpMYB2[/b]模块参与了MeJA诱导的菊苣酸生物合成。总的来说,我们鉴定了一个通过激活初级和特化代谢基因正向调控菊苣酸生物合成的MYB转录因子[b]EpMYB2[/b],连接了茉莉酸信号通路与菊苣酸生物合成之间的缺口。这项工作为利用生物技术手段提高紫锥菊药用质量开辟了新方向。 [align=left][b]前言[/b][/align] 几千年来,人类一直使用植物来维持健康。天然产物分子是药物开发的重要资源)。紫锥菊([b]Echinacea purpurea[/b] (L.) Menoch)原产于北美,并在全球广泛种植。除了作为观赏植物种植外,它还被用作草药治疗口疮、感冒和蛇咬伤。现代药理学实验已经证明它具有免疫调节、抗炎、抗氧化和抗病毒活性。紫锥菊产品几十年来在全球范围内畅销,通常用于预防和治疗普通感冒。在紫锥菊中发现了许多不同的化学成分,包括咖啡酸衍生物、糖蛋白、烷基胺和黄酮类化合物。其中,菊苣酸作为一种咖啡酸衍生物,是这些多种化学成分中最具代表性的,广泛积累在整个植物中,已被用作紫锥菊产品和原材料的质量指标。许多研究报告已经证明,菊苣酸具有多种生物活性,例如抗病毒、抗氧化、抗炎、肝脏保护、肾脏保护和抗癌,这些生物活性已经在最近的综述中得到了介绍。到目前为止,紫锥菊一直是菊苣酸补充剂的主要来源。由于市场对紫锥菊及其菊苣酸的需求量大,有必要提高植物中菊苣酸的含量,这依赖于生物合成途径和调控网络的阐明。 我们之前已经阐明了紫锥菊中菊苣酸的生物合成途径。首先,苯丙氨酸通过限速酶苯丙氨酸解氨酶(PAL)和随后的一些酶(如肉桂酸4-羟化酶(C4H)和4-香豆酸连接酶(4CL))转化为对香豆酰CoA。对香豆酰CoA是多种苯丙素类化合物生物合成的关键中间体,包括黄酮类化合物、羟基肉桂酸衍生物和白藜芦醇类化合物(Vogt, 2010)。在菊苣酸的生物合成过程中,对香豆酰CoA通过羟基肉桂酰CoA:莽草酸/奎宁酸羟基肉桂酰转移酶(HCT)和对香豆酰莽草酸/奎宁酸3'-羟化酶(C3'H)转化为咖啡酰CoA。两种BAHD型酰基转移酶(羟基肉桂酰CoA:酒石酸羟基肉桂酰转移酶(HTT)和羟基肉桂酰CoA:奎宁酸羟基肉桂酰转移酶(HQT))利用咖啡酰CoA作为酰基供体,分别以酒石酸和奎宁酸为酰基受体,生成槲皮素酸和绿原酸。最后,一种特殊的丝氨酸羧肽酶样(SCPL)型酰基转移酶——菊苣酸合酶(CAS)催化菊苣酸的生物合成,以槲皮素酸为酰基受体,绿原酸为酰基供体(Fu, Zhang, Jin等,2021)。我们进一步描述了酰基转移酶的底物多样性,并描绘了紫锥菊中菊苣酸及其类似物的整个生物合成网络。毫无疑问,菊苣酸的积累是由其生物合成基因的表达决定的。与此同时,生物合成基因的表达通常受到转录因子(TFs)的调控。尽管我们已经阐明了生物合成途径,但菊苣酸的调控网络仍然不清楚。 植物的各种转录因子(TFs)家族已经被发现参与植物次生代谢的调控,例如v-Myb髓样细胞白血病病毒癌基因同源物(MYB)、基础/螺旋-环-螺旋(bHLH)、WD重复、乙烯响应因子(ERF)、WRKY和基础亮氨酸拉链(bZIP)。其中,MYB转录因子被认为是苯丙素代谢的主要调控因子。它们包含一个保守的N端DNA结合结构域重复(R)和一个可变的C端调控区域。根据R的数量,MYBs可以分为四类,包括1R-、R2R3-、3R-和4R-MYB蛋白。R2R3-MYBs是植物MYBs中占主导地位的,被认为在功能多样化中帮助植物从水生环境适应到陆地环境。亚家族3、4、5、6、7、8、13、21、31、32、44和79的R2R3-MYBs主要被报道调控苯丙素生物合成途径,通过直接结合启动子作为激活因子或抑制因子发挥作用。许多植物R2R3-MYBs识别DNA靶点的AC元件,这些元件富含腺嘌呤和胞嘧啶残基。例如,AtMYB12,亚家族7的成员,被报道直接结合启动子的MYB12BS位点(CACCTACC、TACCTAMC和TAGCWACC),调控蔗糖磷酸合酶(DAHPS)、苯丙氨酸解氨酶(PAL)、查尔酮合酶(CHS)和黄烷酮3-羟化酶(F3H)的表达。 此外,生物和非生物刺激也影响植物次生代谢物的生物合成。植物防御机制的诱导通常伴随着大量次生代谢物的产生。在此过程中,脂质衍生植物激素——茉莉酸(JAs)发挥了关键作用。例如,JAs诱导了许多次生代谢物的生物合成,如长春碱、青蒿素、尼古丁和紫杉醇。许多转录因子家族的成员对JAs有响应,并调控JAs诱导的次生代谢物积累。在茉莉酸信号通路中,茉莉酸ZIM域(JAZ)家族的抑制蛋白通常与转录因子结合并抑制其激活功能。在JAs存在的情况下,JAZ蛋白被SCFCOI1复合物降解,最终释放转录因子。该通路中研究最透彻的转录因子属于MYC家族(bHLH型TF),包括MYC2、MYC3和MYC4。例如,MYC2s直接和间接地调控次生代谢物的诱导,通过结合下游基因启动子上的G-box位点并激活其表达。 有趣的是,菊苣酸的生物合成在紫锥菊的毛状根、幼苗和细胞悬浮培养物中显著受到甲基茉莉酸甲酯(MeJA)的诱导。目前尚不清楚哪种转录因子参与了紫锥菊中MeJA诱导的菊苣酸生物合成。将转录因子与生物合成基因结合使用将显著提高目标代谢物的产量。因此,必须识别潜在的正向调控因子以实现高产量的菊苣酸生产。最近,我们建立了紫锥菊开花期不同组织的转录组,并鉴定了一个属于亚家族6的R2R3-MYB转录因子[b]EpMYB1[/b],该转录因子正向调控紫锥菊中的花青素生物合成。在此基础上,我们通过共表达和系统发育分析鉴定了可能参与菊苣酸生物合成的转录因子。通过系统表征和体内转基因验证,鉴定出一个MYB转录因子,并阐明了其调控机制。进一步的研究还解释了其在MeJA诱导的菊苣酸生物合成中的作用。这项研究进一步阐明了菊苣酸的生物合成,并为利用生物技术手段提高紫锥菊中菊苣酸含量奠定了基础。 [align=left][b]结果[/b][/align] [b][b]参与菊苣酸生物合成的TF的筛选[/b][/b] 该团队之前已经阐明了紫锥菊中菊苣酸的生物合成途径(图1A)。利用最近建立的多组织转录组数据集,我们通过BLASTP方法识别出了菊苣酸生物合成基因。通过对这些生物合成基因表达水平的层次聚类分析,我们发现它们的表达模式相似,并且在根部高表达(图1B)。尤其是[b]EpPAL[/b]、[b]EpC4H[/b]、[b]Ep4CL[/b]、[b]EpC3’H[/b]、[b]EpHTT[/b]和[b]EpCAS[/b]具有紧密的共表达关系(图1B)。这些结果通过RT-q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]得到了验证。共表达分析已经被广泛应用于中间代谢物、生物合成基因和调控因子的鉴定。随后,我们使用这六个高度相关的菊苣酸生物合成基因作为诱饵进行共表达分析。通过与这六个基因共表达且线性相关系数高于0.8的基因的交集,共获得了139个转录因子(图1C)。MYB转录因子已经被证明可以调控苯丙素代谢。在这139个转录因子中,21个被注释为MYB。在去除冗余序列后,我们将这21个[b]EpMYBs[/b]与[b]AtMYBs[/b]进行比对并用于系统发育分析。这些[b]EpMYBs[/b]分布在几个亚家族中,包括2、7、14、20和78。之前有报道指出,亚家族3、4、5、6、7、8、13、21、31、32、44和79的成员参与调控苯丙素代谢。在这10个[b]EpMYBs[/b]中,亚家族7的两个成员(即CL4945.Contig5_All和CL4945.Contig7_All)可能具有调控苯丙素的潜力。当这两个[b]EpMYBs[/b]在[b]Nicotiana benthamiana[/b]叶片中瞬时过表达时,CL4945.Contig5_All(命名为[b]EpMYB2[/b])显著增加了总酚含量(图1D)。总体而言,我们通过共表达、系统发育分析和异源功能研究确定了[b]EpMYB2[/b]为潜在的菊苣酸生物合成调控因子。 [b][b]EpMYB2[/b] 正向调控菊苣酸生物合成[/b] 对[b]EpMYB2[/b]与拟南芥亚家族7成员的多序列分析表明,[b]EpMYB2[/b]具有完整的R2和R3结构域,可被鉴定为R2R3-MYB。进一步对[b]EpMYB2[/b]与其他植物物种亚家族7成员的系统发育分析显示,[b]EpMYB2[/b]与[b]Gentiana trifloral[/b]的[b]GtMYBP4[/b]较为接近,后者已被报道能促进类黄酮生物合成(图2A)。RT-q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]分析表明,[b]EpMYB2[/b]在根、茎和叶柄中高表达,这与RNA-seq数据一致(图2B)。通过在烟草叶片中瞬时表达[b]EpMYB2-GFP[/b]融合蛋白,发现[b]EpMYB2[/b]定位于细胞核中(图2C)。此外,[b]EpMYB2[/b]的表达对不同的胁迫处理(尤其是MeJA)具有响应(图2D),这表明它可能在环境胁迫与次生代谢之间起到链接作用。 为了探索[b]EpMYB2[/b]的体内功能,我们构建了[b]EpMYB2-OE[/b]紫锥菊愈伤组织。对照组和[b]EpMYB2-OE[/b]组愈伤组织的表型都呈现淡黄色,彼此之间没有显著差异(图3A)。[b]EpMYB2-OE[/b]组的[b]EpMYB2[/b]表达水平显著高于对照组(P 0.05)(图3B)。采用基于[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-高分辨率质谱(LC-HRMS)的非靶向代谢组学方法,对紫锥菊愈伤组织进行代谢物变化评估。在主成分分析(PCA)得分图中,对照组与[b]EpMYB2-OE[/b]组显著分离(图3C)。进一步的载荷图评估表明,主要的差异离子属于菊苣酸及其类似物甲基菊苣酸和其底物槲皮素酸与绿原酸,根据保留时间和质谱进行鉴定(图3D)。与对照组相比,[b]EpMYB2-OE[/b]组中这些化学物质的含量显著增加(图3E)。此外,菊苣酸生物合成基因,包括[b]EpPAL[/b]、[b]EpC4H[/b]、[b]Ep4CL[/b]、[b]EpHCT[/b]、[b]EpC3’H[/b]、[b]EpHQT[/b]、[b]EpHTT[/b]和[b]EpCAS[/b],均受[b]EpMYB2[/b]上调(图3F)。这些结果表明,[b]EpMYB2[/b]是菊苣酸生物合成的正向调控因子。另一方面,鉴于亚家族7的成员被确认是类黄酮调控因子,我们进一步研究了[b]EpMYB2[/b]对类黄酮的影响。[b]EpMYB2[/b]对关键生物合成基因的表达和类黄酮代表性化学物质的水平没有表现出一致的促进作用。它显著增加了芸香苷的含量,但未显著增加紫茉莉苷的含量。菊苣酸的增加幅度远高于芸香苷,这表明[b]EpMYB2[/b]对菊苣酸生物合成的激活作用比对类黄酮的更强。所有这些结果表明,[b]EpMYB2[/b]主要在紫锥菊中促进菊苣酸的生物合成。 [b][b]EpMYB2[/b] 正向调控上游的初级代谢基因[/b] 许多转录因子被发现具有多个调控靶点,尤其是一些调控次生代谢的转录因子,它们也被发现参与初级代谢的调控。为了进一步评估[b]EpMYB2[/b]的功能,我们对转基因愈伤组织进行了RNA-seq分析。将上调的基因进行KEGG途径富集分析。令人感兴趣的是,除了苯丙氨酸代谢外,苯丙氨酸、酪氨酸和色氨酸的生物合成途径也得到了富集(图4A)。这些芳香族氨基酸来源于莽草酸途径,属于初级代谢途径,并且是苯丙素代谢的上游(图4B;表S1)。我们使用RT-q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]评估了这些上游生物合成基因的表达水平。几种结构基因,包括[b]EpDAHPS[/b]、[b]EpEPSPS[/b]、[b]EpCM[/b]、[b]EpPAT[/b]和[b]EpADT[/b],被[b]EpMYB2[/b]显著上调(P 0.05)(图4C)。因此,色氨酸、酪氨酸和苯丙氨酸的含量均显著增加(P 0.05)(图4D)。综上所述,[b]EpMYB2[/b]被发现具有多个潜在的调控靶点,覆盖了初级和次级代谢途径。 [b][b]EpMYB2[/b] 通过直接结合激活关键的苯丙氨酸和菊苣酸生物合成基因的表达[/b] 为了探索[b]EpMYB2[/b]对菊苣酸生物合成的调控机制,我们尝试克隆这些初级和次级代谢基因的启动子。使用之前报道的方法,我们成功克隆了10个启动子(图5B)。然后,我们采用双荧光素酶测定法来测试[b]EpMYB2[/b]对这些启动子激活的作用(图5A)。[b]EpMYB2[/b]对[b]proEpCM[/b]、[b]proEpPAT[/b]、[b]proEpPAL[/b]、[b]proEpC4H[/b]、[b]proEp4CL[/b]、[b]proEpHCT[/b]、[b]proEpC3’H[/b]、[b]proEpHTT[/b]和[b]proEpCAS[/b]表现出激活效应,但对[b]proEpHQT[/b]没有影响(图5C)。在菊苣酸生物合成中起主导作用的关键代谢基因[b]EpPAL[/b]、[b]EpHCT[/b]和[b]EpHTT[/b]被广泛激活(图5C)。[b]EpHQT[/b]在紫锥菊种子发芽过程中的表达模式也表现出明显的差异,这表明其具有不同的调控网络。这些结果表明,[b]EpMYB2[/b]可以通过直接激活重要代谢基因的启动子来调控菊苣酸的生物合成。为了进一步识别潜在的结合位点,我们对这些启动子进行了分析,发现[b]proEpCM[/b]、[b]proEpPAT[/b]、[b]proEpPAL[/b]、[b]proEpHCT[/b]、[b]proEpC3’H[/b]和[b]proEpHTT[/b]在ATG上游500 bp内都包含[b]MYB12BS[/b]位点(图5B)。我们选择了[b]EpPAL[/b]、[b]EpHCT[/b]和[b]EpHTT[/b]这三个菊苣酸生物合成的关键代谢基因,来研究潜在的结合位点。在[b]EpPAL[/b]、[b]EpHCT[/b]和[b]EpHTT[/b]的启动子上突变[b]MYB12BS[/b]位点后,在双荧光素酶测定法中[b]EpMYB2[/b]对这些启动子的激活水平显著降低(图S7A;图5D、F)。此外,我们采用酵母单杂交(Y1H)实验来确认直接的结合效应。[b]EpMYB2[/b]显示出直接结合在[b]proEpHCT[/b]和[b]proEpHTT[/b]的[b]MYB12BS[/b]位点上(图5E、G)。由于[b]proEpPAL[/b]具有较高的自活性,因此难以验证[b]EpMYB2[/b]对其的直接结合作用(图S7B)。这些结果表明,[b]MYB12BS[/b]至少是[b]EpMYB2[/b]的一个结合位点。综上所述,我们发现[b]EpMYB2[/b]可以通过与启动子结合直接激活基因表达,并识别了一个结合位点。 [b][b]EpMYC2-EpMYB2[/b] 模块介导了MeJA诱导的菊苣酸生物合成[/b] 先前的研究表明,紫锥菊中菊苣酸的生物合成受到MeJA的诱导。在本研究中,我们注意到[b]EpMYB2[/b]的表达显著受到MeJA的影响(图2D),这让我们推测[b]EpMYB2[/b]是否参与了MeJA诱导的菊苣酸生物合成。由于[b]EpMYB2[/b]主要在根部表达(图2),我们处理了紫锥菊根部以进一步探索[b]EpMYB2[/b]在JA信号响应中的作用。结果表明,[b]EpMYB2[/b]的表达水平显著被MeJA处理所诱导(图6A)。此外,菊苣酸生物合成基因的表达水平和化学物质的含量也均受诱导(图6B)。考虑到[b]MYC2[/b]在JA信号途径中的重要作用,我们通过BLASTP分析发现了[b]EpMYC2[/b],该基因是从[b]Artemisia annua[/b]中鉴定出的[b]AaMYC2[/b]的同源基因。多序列比对分析表明,[b]EpMYC2[/b]包含完整的[b]MYC2[/b]结构域,包括基础和HLH(螺旋-环-螺旋)结构域、JAZ结合域(JID)以及与MED25蛋白结合的转录激活域(TAD)。系统发育分析显示,[b]EpMYC2[/b]与[b]AaMYC2[/b]较为接近,是bHLH亚家族7的典型成员(图6C)。为了探究[b]EpMYC2[/b]是否会影响[b]EpMYB2[/b]的表达,我们克隆了包含两个G-box位点的[b]EpMYB2[/b]启动子。[b]EpMYC2[/b]通过双荧光素酶测定法验证了其对[b]EpMYB2[/b]启动子的激活作用(图6D)。当启动子上距ATG 126 bp的G-box位点被突变后,[b]EpMYC2[/b]对[b]EpMYB2[/b]启动子的激活水平显著下降(图6D)。通过酵母单杂交(Y1H)实验确认了[b]EpMYC2[/b]直接结合[b]proEpMYB2[/b]–126 bp G-box位点的作用)。因此,[b]EpMYC2[/b]通过G-box位点激活了[b]EpMYB2[/b]启动子的表达。以上结果表明,[b]EpMYC2-EpMYB2[/b]模块介导了MeJA诱导的菊苣酸生物合成。 [align=left][b]结论[/b][/align]该研究发现了一种 MYB TF,即 EpMYB2,它能通过直接激活涵盖初级和特化代谢基因的初级和特化代谢基因的表达,正向调控紫锥菊中的菊苣酸生物合成通过直接激活涵盖初级和次级代谢的初级和特化代谢基因的表达,积极调控紫锥菊的菊苣酸生物合成。次生代谢基因的表达。鉴定EpMYC2-EpMYB2模块还连接了JA信号途径与菊苣酸生物合成之间的联系。这些结果进一步解释了菊苣酸的生物合成,并为菊苣酸的工程生产铺平了道路。此外,与 CK 组几乎不产生菊苣酸相比,EpMYB2 过度表达的紫锥菊中的菊苣酸含量相当可观,可将其视为提取菊苣酸的原料。
MicroRNAs (miRNAs) 是真核生物中广泛存在的一种长约21到23个核苷酸的RNA分子,可调节其他基因的表达。miRNA来自一些从DNA转录而来,但无法进一步转译成蛋白质的RNA(属于非编码RNA)。这些RNA从初级转录本(primary transcript),也就是pri-miRNA,转变成为称为miRNA前体(pre-miRNA)的茎环结构,最后成为了具有功能的miRNA。细胞借助于一种特殊的机器——“微处理器”复合物("Microprocessor" complex)将这些长链的miRNA前体切断,然后将它们转变为较短的功能性的miRNA形式。生成的miRNAs与特异性信使RNA(mRNA)分子结合,抑制转录后基因表达,在调控基因表达、细胞周期、生物体发育时序等方面起实验室耗材重要作用。在动物中,miRNAs通常可以调控成百上千不同基因的表达。然而微处理器复合物也可以切断其他类型的RNA,例如mRNAs,这些mRNAs有时会生成与miRNAs靶位点相似的不稳定结构。裂解这种错误的RNAs有可能对生物体带来灾难性后果。在近期发布在《自然结构与分子生物学》(Nature Structural and Molecular Biology)杂志的一篇论文中,来自魏茨曼科学研究所分子遗传学系的Eran Hornstein博士、Naama Barkai教授和前博士生Omer Barad与Mati Mann侧重了解了这种微处理器在miRNAs生成中平衡有效性和特异性之间相互作用的机制。“一方面,它不应该过于有效,因为这可能会导致裂解不必要的非特异性RNA底物为代价。另一方面,也不应该太‘严格’因为过度的特异性会带来不充分加工真正miRNAs的风险,”Hornstein说。在一个跨学科研究项目中,科学家们利用数学建模确定了微处理器系统的特征,然后在细胞中测试了它们的理论。他们预测有效性和特异性之间的平衡是通过一个反馈回路维持,在这个人血清 混合反馈回路中微处理器检测到细胞内可用pre-miRNA的数量,相应地改变自身的生产。在小鼠和人类组织中检测这一假说,研究人员能够证实微处理器确实调控了miRNA前体的水平,当细胞充满miRNA前体时则提高自身的生产,或在前体量下降时作出反应停止生产。这是通过消化一种在结构上与miRNA相似的Dgcr8 mRNA而实现的。通过与miRNAs维持水平一致,微处理器由此减少了切断靶RNAs的机会。由于合成小RNAs是对于多种疾病一种可能的新疗法,这一研究或可直接促成未来有效的治疗。此外,许多其他的生物系统需要兼顾有效性和特异性,该研究小组的结果表明许多可能是细胞培养以相似的方式来实现的。
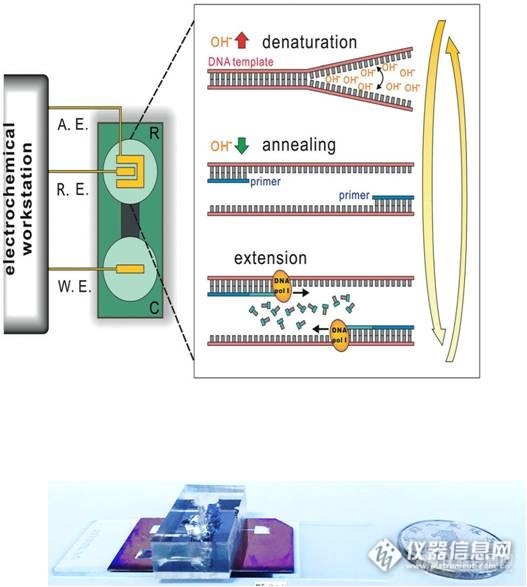
http://ng1.17img.cn/bbsfiles/images/2016/11/201611141442_616419_0_3.jpg 近日,中国科学院上海应用物理研究所与清华大学合作,发展了一种新型的离子介导聚合酶链式反应(Ion-Mediated Polymerase Chain Reaction, IM-PCR),通过精确调控溶液pH值(即质子和氢氧根离子),可以在室温下完成PCR扩增,相关结果发表于《德国应用化学》(Angew. Chem. Int. Ed.)杂志,并申请了美国和国际专利。 PCR是体外通过酶反应合成、高灵敏扩增目标基因片段的一种方法,是最常用的分子生物学技术之一。常规PCR是通过控制溶液温度来实现DNA分子的可逆变复性,从而达到复制扩增的目的。而这种升降温过程通常需要复杂的控温装置并消耗大量能源。从理论上来说,DNA变复性还可以通过酸碱变性来实现,然而如何在不改变溶液体积的情况下精确控制溶液pH值则是一个难题。上海应物所物理生物学研究室樊春海课题组与清华大学化学系刘冬生课题组合作,建立了一种基于微流控的电化学芯片,可以通过电压驱动快速、精确调控溶液pH值,并实现了对DNA分子机器的电驱动控制(Nano Lett. 2010,10,1393)。基于这一研究基础,上海应物所博士张一和副研究员李茜发现微流控电化学可以有效控制PCR反应体系的pH值,实现了室温下的酸碱驱动的IM-PCR扩增。与传统PCR技术相比,这一新型的集成化IM-PCR技术无需变温过程,所有反应步骤均在室温下进行。这一小型化、低成本、易于集成的PCR新技术有望在生物检测、临床诊断及环境监测中发挥作用。

 400-860-5168转1895
400-860-5168转1895
 留言咨询
留言咨询

 400-860-5168转1263
400-860-5168转1263
 留言咨询
留言咨询

 400-860-5168转1895
400-860-5168转1895
 留言咨询
留言咨询


