推荐厂家
暂无
暂无






如果没有标准参考物质,怎样评价数据的可靠性??请各位赐教!!![em49] [em61]
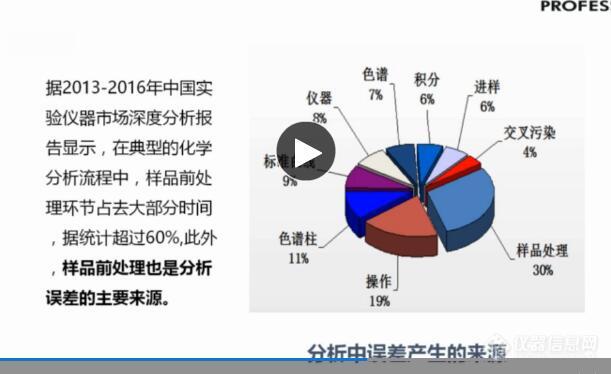
实验数据的可靠性和结果可重现是实验室的生存之本,影响实验数据可靠性和结果可重现的因素有很多,什么才是影响实验数据可靠性和结果可重现的源头呢?FDA审查的重点一个是计量验证,另外一个常被大家忽视的就是清洁验证。据调查实验数据误差的来源影响因素如下:[img=,611,374]http://ng1.17img.cn/bbsfiles/images/2018/03/201803140810186081_5945_1810231_3.jpg!w611x374.jpg[/img]前处理为最大的误差来源因素,其中[b]玻璃器皿的科学化清洁又是样品前处理最大的容易忽视的因素。[/b]随着国家对实验室能力验证的进一步监管,[b]实验室保障性的设备必将热销。有一位院士曾经说过:[color=#ff0000]良好先进的实验室,不仅仅有高精尖的分析仪器,而是同时具备过程可追溯、结果可重复、进程可验证的环境安全,方法可靠的完善的管理体系。[/color][/b]实验室自动化清洗:过程标准化、过程安全化、可追溯、可验证,是实验室现代化管理体系中的很重要的环节。以上是我的一些看法,欢迎大家踊跃积极的讨论,根据实际工作经验谈谈自己的看法。

[b]从“疫苗事件"浅谈制药生产数据可靠性[/b] [img=,690,462]http://ng1.17img.cn/bbsfiles/images/2018/07/201807261523211521_3351_271_3.png!w690x462.jpg[/img] 最近持续发酵的“疫苗事件”引起了社会对于药品安全的巨大关注,相关企业生产记录造假,严重违反《药品生产质量管理规范》,国家领导人也分别对这起事件的调查做出了重要指示。很多人甚至对接种疫苗本身的必要性都产生了怀疑。首先我们应该明确一点,疫苗作为人类医学最伟大的发明之一,每年都能拯救数百万的生命。纵然由于目前个别批次疫苗存在问题,我们也不能否认疫苗本身的正面作用。 而对于制药企业本身而言[b]生产记录[/b]这一个小小的方面对于药品质量究竟有多重要则不言而喻。[b]生产记录是产品的“身份证”[/b]一般来说,一份生产记录主要包括:供应部门的原辅料进货记录;仓储原辅料以及产品的进、出货记录;财务部门的相应原辅料购买凭证和记录;质检部门相应的原辅料以及产品的取样记录、检验记录、检验报告单等;生产部门的领用记录、批生产记录;销售部门的产品调出记录等。其内容包括产品名称、生产批号、生产日期、操作者与复核者的签名、有关操作与设备、相关生产阶段的产品数量、物料平衡的计算、生产过程的控制记录及特殊问题记录。一旦产品出现问题,这些记录便可以查找企业生产存在的问题,掌握产品的去向,可是如此关键的生产记录却被人动了手脚,这种造假不仅暴露出企业管理不善,而且存在着巨大危害。所以关于数据可靠性的问题不仅是此次事件的症结所在,更一直都是各类现场检查、跟踪检查、飞行检查等各类检查的重中之重。[b]什么是数据可靠性?数据可靠性[/b]指在数据生命周期内,数据完整、一致、准确的程度。应当以安全的方式收集和维护数据,从而保证数据归属至人、清晰可溯、同步记录、原始一致、准确真实(国际上,常用缩略词“ALCOA”或“ALCOA+”概括)。在《2017年度药品检查报告》中国家药品监督管理局共计完成了751项各类检查。其中国家药品监督管理局发现的可靠性相关的问题主要包括:修改系统时间后检测、关键数据无法溯源,原始记录、原始图谱、原始数据及计算过程缺失,检验原始记录内容不一致,恶意修改积分参数,套用图谱,生产和检验记录管理混乱,提前填写记录,未对分析仪器的计算机系统进行权限管理和有效控制等。国家药品监督管理局对药品生产数据的可靠性进行审计的重点是:[table][tr][td=1,1,489] [/td][/tr][tr][td=1,1,489] l [b]未及时记录生产过程中的数据,补记录[/b][/td][/tr][tr][td=1,1,489] l [b]生产现场实际与批记录数据不一致[/b][/td][/tr][tr][td=1,1,489] l [b]生产批记录与实际设备产能不一致[/b][/td][/tr][tr][td=1,1,489] l [b]代替别人签字[/b][/td][/tr][tr][td=1,1,489] l [b]补签时间和日期[/b][/td][/tr][tr][td=1,1,489] l [b]数据转移没有过程记录[/b][/td][/tr][tr][td=1,1,489] l [b]现场设备运行参数与记录数据不一致[/b][/td][/tr][/table]相关的检查清单: [table][tr][td=1,1,489][b][color=white]数据有效性检查清单[/color][/b] [/td][/tr][tr][td=1,1,489] l [b]是否存在不同用户共用计算机化系统账户的情况?包括车间的工艺设备。[/b][/td][/tr][tr][td=1,1,489] l [b]涉及电子记录的计算机化系统是否具备审计追踪功能?[/b][/td][/tr][tr][td=1,1,489] l [b]电子签名是否经过验证/确认? [/b][/td][/tr][tr][td=1,1,489] l [b]是否存在使用个人手写签名的电子图片代替电子签名的情况?[/b][/td][/tr][tr][td=1,1,489] l [b]审计追踪功能或其替代方法是否被开启并激活?[/b][/td][/tr][tr][td=1,1,489] l [b]审计追踪功能或其替代方法是否被修改?[/b][/td][/tr][tr][td=1,1,489] l [b]计算机化系统的时间戳(时间/日期/时区)是否被人为篡改?[/b][/td][/tr][tr][td=1,1,489] l [b]电子签名是否真实、安全?[/b][/td][/tr][/table][b]由此可见确保整个制药生产过程的数据可靠性,这已成为全球药企合规性的基础,并成为监管部门重点核查的领域。 [/b]看到这里您肯定会问那么梅特勒-托利多又能做些什么?梅特勒-托利多基于现有相关数据完整性法规的要求,帮助制药厂家针对制药的整个生产流程:从实验室原料、成品的称量及分析;原料、辅料配料混合搅拌;工艺参数控制;罐装、压片或制粒;到药品包装与物流提供不同层次的解决方案,使用部分或全部无纸化系统解决方案来管控生产流程,确保制药企业及时、准确的记录,实现相关数据的追溯和安全存储。 [b][b]原料、成品实验室检验环节对于实验室常见的中小型仪器,诸如密度、折光、电导率、pH计、滴定、水分、天平等梅特勒-托利多产品系列,可以利用LabX软件整合在同一个操作平台上进行统一管理。LabX提供多样化的用户管理、集中化的数据管理和统一化的SOP方法管理。用户不仅可以在电脑屏幕控制仪器进行分析,而且可以在仪器触摸屏调用相关方法,按照屏幕提示步骤操作即可,无需人工计算,无需纸质版SOP,实验数据自动上传到安全的数据库中,消除计算和转录的错误,有助于满足ALCOA原则规范,实现检验数据可靠性。[b][/b][/b]在工艺控制环节梅特勒-托利多过程分析部门的智能传感器管理(ISM)技术,帮助优化在线传感器的管理和使用;同时,配套的软件iSense,可有效采集、分析和管理电极的校准信息并保持连贯记录。iSense CFR在技术上符合21CFR第11部分和EudraLex第4卷附录11的要求,帮助企业在确保生产速度的同时最大限度提升产品质量,保障客户的利益,最大限度的确保制药企业的数据完整性与可靠性。同时,可提供完整的[b]电子文件记录并进行用户管理[/b]。将诸如校准或维护等与传感器相关的所有活动进行存储,并通过电子方式或打印方式进行文件记录;另外,用户管理与电子日志簿可控制与跟踪各项活动,以确保在传感器资产的整个使用寿命期内对其进行完整文件记录。凭借可轻松访问的,关于每一台传感器的完整与可靠文件,可以很容易地满足法规要求。在制药的生产环节称重[/b]是药品生产中的重要过程,我们从配料称量和质量管理等方面提升数据的可靠性,确保符合GMP要求。[b] 我们的ICS689标签打印解决方案,帮助制药企业打印完整的原始数据及元数据,方便物料核对和复核,配合Collect+数据采集软件,实现自动化数据传输,避免转录错误。[/b]在配料称量环节,我们的FormWeigh.Net配方称量系统是一套合规的联网系统,实时监控、控制、追踪并验证配制工艺的各个方面,系统具备锁定时间戳,权限分级,审计追踪等功能,确保可靠完整的记录,避免人为修改,全流程可追溯。[b]在制药生产成品包装前后环节[/b]特勒-托利多的Tablex金属检测机提供符合FDA 21 CFR part 11的严格规定的电子签名及生产日志,[color=black]多级密码权限,防止越级操作,可确保所有操作追溯到人[/color],从而支持完全符合标准要求,使得生产企业可以始终全面掌控药品的生产过程。 对于制药企业来说,符合质量标准的药品=合格的操作人员+符合要求的设备+良好的流程如何符合法规,控制风险,确保质量,把人为差错降到最低,杜绝造假,防患于未然,是赢得市场和用户信任的关键梅特勒-托利多希望通过我们的解决方案,帮助制药企业完善GMP流程,重铸市场信心。欢迎您点击阅读原文了解我们相关的解决方案
 留言咨询
留言咨询

 留言咨询
留言咨询

 400-860-5168转3546
400-860-5168转3546
 留言咨询
留言咨询


