推荐厂家
暂无
暂无
[size=15px][font=宋体]结直肠癌([/font][font=&]Colorectal Cancer[/font][font=宋体],[/font][font=&]CRC[/font][font=宋体])是全球常见的恶性肿瘤,术后复发转移已成为结直肠癌患者死亡的主要原因,特别是结直肠癌肝转移([/font][font=Georgia, &][color=#333333]CRLM[/color][/font][font=宋体])。因此,迫切需要深入研究[/font][font=Georgia, &][color=#333333]CRLM[/color][/font][font=宋体]的病理和分子机制。原发性肿瘤细胞与远端器官中的免疫细胞或基质细胞之间的信息传递是转移前微环境([/font][font=&]PMN[/font][font=宋体])形成的关键因素,了解这一机制对于制定有效的肿瘤转移治疗策略至关重要。[/font][font=&][/font][/size][size=15px][font=宋体]细胞外囊泡([/font][font=&]EV[/font][font=宋体])作为各种细胞分泌的功能实体,富含蛋白质、核酸、脂质和其他分子,促进肿瘤细胞和基质细胞之间的重要通讯。越来越多的报道表明,肿瘤衍生的[/font][font=&]EV[/font][font=宋体]([/font][font=&]TEV[/font][font=宋体])有助于[/font][font=&]PMN[/font][color=#333333]和[/color][font=Georgia, &][color=#333333]CRLM[/color][/font][font=宋体]的形成,为转移器官中循环肿瘤细胞的增殖提供必需肿瘤微环境([/font][font=&]TME[/font][font=宋体])。作者推测[/font][font=&]circRNA[/font][font=宋体]富集的[/font][font=&]TEVs[/font][font=宋体]介导[/font][font=&]PMN[/font][font=宋体]的形成,并且靶向[/font][font=&]circRNA[/font][font=宋体]富集的[/font][font=&]TEVs[/font][font=宋体]可能是针对[/font][font=&]PMN[/font][font=宋体]形成和[/font][font=&]CRLM [/font][font=宋体]的有效治疗策略。[/font][/size][size=15px][font=宋体]肿瘤细胞分泌的富含[/font][font=&]circ-0034880[/font][font=宋体]的细胞外囊泡通过增强[/font][font=&] SPP1[sup]high[/sup]CD206[sup] +[/sup][/font][font=宋体]促肿瘤巨噬细胞的活化来促进结直肠癌肝转移。重要的是,研究确定人参皂苷[/font][font=&]Rb1[/font][font=宋体]是一种潜在的治疗剂,通过直接靶向[/font][font=&]QKI [/font][font=宋体]蛋白,从而减少[/font][font=&]circ-0034880[/font][font=宋体]的生物合成并抑制[/font][font=&]SPP1[sup]high[/sup]CD206[sup] +[/sup][/font][font=宋体]促肿瘤巨噬细胞的活化,最终抑制结直肠癌肝转移。研究从调控[/font][font=&]TME[/font][font=宋体]的角度,特别是抑制[/font][font=&]circ-0034880[/font][font=宋体]的生物合成和细胞外囊泡的生成,首次揭示了人参皂苷[/font][font=&]Rb1[/font][font=宋体]在肿瘤防治领域的特殊作用,为今后的临床药物转化奠定了坚实的基础。 [size=15px][b]1、富含Circ-0034880的血浆EV与CRLM相关[/b][/size][font=宋体]基于细胞外囊泡在肿瘤转移中的重要作用,作[/font][font=宋体]者首先人类血液外泌体数据库、GSE159669数据集,以及临床血浆细胞外囊泡样本发现[/font][size=15px]一个环状RNA circ-0034880在结直肠癌肝转移患者中具有更高的表达水平,表明该环状RNA与结直肠癌的肝转移密切相关[/size] [size=15px][b]2、富含Circ-0034880的TEV在体内促进CRLM[/b][/size][size=15px]为了进一步研究circ-0034880富集的TEVs对CRC肝转移的体内影响,作者通过体内示踪实验发现了肿瘤细胞MC38来源的EVs在肝中高度积累。体内注射肿瘤细胞MC38来源的EVs可以促进肝转移,而缺失circ-0034880的EVs却丧失其促肝转移的作用,结果表明EVs依赖于其携带的circ-0034880发挥作用[/size] [size=15px][b]3、Circ-0034880富集的TEV激活肝脏转移前微环境中的CD206+促肿瘤巨噬细胞[/b][/size][size=15px]为了全面评估circ-0034880富集的TEV对肝脏转移前微环境的影响,研究人员对小鼠持续进行TEV注射和肿瘤细胞注射,建立了一个肝转移小鼠模型,多重免疫荧光分析显示TEV处理促进CD206 +促肿瘤巨噬细胞在转移前肝脏中的显著浸润,且circ-0034880表达水平与CD206 +促肿瘤TAM浸润之间存在正相关性 [/size][size=15px][/size][size=15px][b]4、Circ-0034880富集的TEV通过激活CD206 +促肿瘤巨噬细胞促进CRC细胞迁移[/b][/size][size=15px]由于有多项报道显示活化的巨噬细胞对CRC细胞迁移有促进作用,作者进一步研究利用示踪实验发现TEV可以携带circ-0034880被巨噬细胞所吸收。此外,功能实验表明富含circ-0034880 的TEV可以促进CD206+促肿瘤巨噬细胞的活化,并且携带circ-0034880的TEV的巨噬细胞上清会显著促进肿瘤细胞的迁移 [/size][size=15px][b]5、Circ-0034880富集的TEV促进SPP1[sup]high[/sup]CD206 +促肿瘤巨噬细胞的激活[/b][/size][size=15px]为了探究携带circ-0034880的TEV对CD206+促肿瘤巨噬细胞的激活机制,研究人员对TEV处理的巨噬细胞进行了转录组数据分析,进一步通过体外基因和蛋白检测和体内IF实验验证了巨噬细胞中SPP1是其调控的靶点,这些发现表明circ-0034880富集的TEV促进了SPP1[sup]high[/sup] CD206 +促肿瘤巨噬细胞的激活。鉴于已知circRNA可作为miRNA海绵发挥作用,作者分析了circ-0034880靶向的miRNA和SPP1结合的miRNA,发现了有2个miRNA重叠:miR-200a-3p和miR-141-3p。结合实验证明这两个miRNA可结合circ-0034880和SPP1,表明 circ-0034880和SPP1竞争结合miRNA,使SPP1不被miRNA所抑制。SPP1是巨噬细胞活化的关键蛋白,因此,研究结果表明TEV释放的circ-0034880通过保护SPP1免受miR-200a-3p和miR-141-3p介导的降解来提高巨噬细胞中SPP1的表达,促进SPP1[sup]high[/sup]巨噬细胞亚群增加 [/size][size=15px][b]6、人参皂苷Rb1给药可通过阻止富含circ-0034880的TEVs介导SPP1[sup]high[/sup]CD206+促肿瘤巨噬细胞的激活来阻止CRC细胞迁移[/b][/size][size=15px]鉴于circ-0034880的重要作用,下调其表达可以作为抑制癌症肝转移的策略,于是作者对103种天然药物进行了筛选,发现4种天然产物(人参皂苷Rb1、异鼠李素、山奈酚和槲皮素)对该circ-0034880的抑制作用最强,其中人参皂苷Rb1具有更强抑制作用。同样人参皂苷Rb1预处理的肿瘤细胞来源的TEV,其作用于巨噬细胞后下游的SPP1的蛋白表达造成下调作用,后续对结直肠癌细胞迁移能力下降,效果类似于沉默circ-0034880。总之,研究结果表明人参皂苷Rb1给药可通过抑制富含circ-0034880的TEV介导的SPP1[sup]high[/sup] CD206+促肿瘤巨噬细胞的激活来阻止CRC细胞迁移 [/size][size=15px][b]7、人参皂苷Rb1直接与QKI蛋白结合,抑制circ-0034880的生物合成[/b][/size][size=15px]为了确定影响circ-0034880表达的Rb1的直接靶点,作者进行了DARTS实验筛选出151种差异表达蛋白,其中一个蛋白QKI被报道与调控前mRNA剪接和促进circRNA生物合成。研究者接下来采用CETSA分析来验证了QKI和Rb1的结合,证实了Rb1能够显著增加QKI的热稳定性。进一步采用SPR分析验证了Rb1与QKI之间的很强的结合亲和力,通过分子对接预测了结合模式。此外,敲低QKI能够显著抑制该circRNA的表达。研究结果表明Rb1直接与QKI蛋白结合,抑制circ-0034880的生物合成[/size] [size=15px][/size][size=15px][b]8、[/b][/size][size=15px][b]人参皂苷[/b][/size][size=15px][b]Rb1给药通过阻止circ-0034880富集的TEV介导SPP1[sup]high[/sup]CD206+促肿瘤TAM的激活来抑制CRLM[/b][/size][size=15px]最后,作者验证了Rb1 给药的[i]体内[/i]效果,发现与单独使用TEV相比,使用Rb1预处理的TEV给药组的肝转移显著减少,与直接沉默circ-0034880的效果非常相似。然而,在沉默circ-0034880的情况下,使用Rb1预处理的TEV给药对肝转移的影响很小。接下来,作者探讨了Rb1对肝转移中CD206+促肿瘤TAM浸润的影响,发现在Rb1预处理的TEVs给药组中,SPP1表达显著下调,类似于直接沉默circ-0034880的效果。然而,在沉默circ-0034880的前提下,相应肝转移中的SPP1表达受到Rb1预处理的TEVs给药的影响最小。总之,体内功能实验证明Rb1预处理的肿瘤细胞来源的TEV失去了促进癌症肝转移的作用[/size][/font][/size]
[b]芍药苷靶向GSDMD抑制细胞焦亡缓解胆汁淤积[/b] [font=宋体][size=15px][color=black]胆汁淤积(CT)是由胆汁产生、分泌或排泄受损引起的疾病,可进展为严重并发症,包括肝硬化、肝衰竭和可能危及生命的疾病。在CT期间小鼠肝组织的焦亡加剧,靶向焦亡可能在减轻CT方面具有治疗潜力。[/color][/size][/font] [font=宋体][size=15px][color=black]芍药苷(PF)是一种源自芍药属的生物活性天然化合物,在各种肝脏疾病中显示出显著的保肝作用。作者之前的研究表明,PF不仅对对乙酰氨基酚诱导的肝损伤具有治疗益处,还可以调节胆汁酸代谢。已有研究表明PF不仅促进胆汁酸分泌,还增强了胆汁酸的运输和代谢。然而PF是否通过靶向特定的NLRP3/GSDMD信号通路发挥其保肝和利胆作用,以及治疗靶点尚不清楚。[/color][/size][/font] [font=宋体][size=15px][color=black]2024年9月3日,成都中医药大学药学院马骁团队在Phytomedicine[i][/i]上发表了题为“Paeoniflorin inhibited GSDMD to alleviate ANIT-induced cholestasis via pyroptosis signaling pathway”的文章,发现PF给药可减轻 ANIT 诱导的肝脏病理,增强肝功能标志物,并提高细胞活力,GSDMD被确定为PF的直接靶标。机制上,PF靶向GSDMD通过NLRP3依赖性焦亡途径和随后的炎症介质释放,减轻胆汁淤积。[/color][/size][/font] [size=15px][b][font=宋体][color=#0070c0]1[/color][/font][font=宋体][color=#0070c0]、PF改善ANIT诱导的CT模型肝损伤[/color][/font][font=宋体][color=#0070c0][/color][/font][/b][/size] 作者首先构建了ANIT(Alpha-naphthylisothiocyanate)诱导的胆汁淤积大鼠模型,发现PF显著降低ANIT诱导的ALT、AST水平的升高,减轻肝损伤,降低BA, [color=var(--weui-LINK)]TBIL[i][/i][/color]和DBIL水平,降低ALP和γ-GT水平,表明PF可有效减轻ct诱导的肝损伤。此外,PF治疗组炎症细胞浸润程度及胆管增生程度明显减少,且PF显著提高ANIT处理的[color=var(--weui-LINK)]HepG2细胞[i][/i][/color]的活力(图1)。 [align=center] [/align][align=center] [/align] [size=15px][b][font=宋体][color=#0070c0]2[/color][/font][font=宋体][color=#0070c0]、PF通过NLRP3途径改善ANIT诱导的焦亡[/color][/font][font=宋体][color=#0070c0][/color][/font][/b][/size] [font=宋体][size=15px][color=black]先前的研究已经证实,芍药可以通过NF-κB/NLRP3信号通路缓解ANIT诱导的CT。PF作为芍药的主要活性成分,在缓解CT方面显示出显著的治疗潜力。作者推测PF可能通过nlrp3介导细胞焦亡来降低ANIT诱导的CT。通过网络药理学显示高评分值的靶标中包括NLRP3,且处于核心地位。此外,关键靶点的GO和KEGG通路进行富集分析均提示PF通过调节nlrp3依赖性焦亡来改善CT(图2)。[/color][/size][/font] [align=center] [/align][align=center] [/align][size=15px][b][font=宋体][color=#0070c0]3[/color][/font][font=宋体][color=#0070c0]、PF介导NLRP3/GSDMD通路改善ANIT诱导的焦亡[/color][/font][font=宋体][color=#0070c0][/color][/font][/b][/size] [font=宋体][size=15px][color=black]上述研究表明PF可能通过NLRP3依赖经典焦亡途径缓解ANIT诱导的CT。作者进一步通过电镜对焦亡进行研究,发现PF处理组线粒体肿胀明显减少,且PF治疗减少模型组出现的细胞肿胀,膜上有明显的孔并伴有许多水泡状突起。WB表明实验模型组NLRP3、GSDMD-N、ASC、Caspase 1 P20蛋白表达明显上调,而PF显著逆转上述情况(图3)。[/color][/size][/font] [align=center] [/align][align=center][font=宋体][size=15px][color=black][/color][/size][/font][/align][align=center] [/align] [size=15px][b][font=宋体][color=#0070c0]4[/color][/font][font=宋体][color=#0070c0]、PF通过靶向GSDMD改善ANIT诱导的焦亡[/color][/font][/b][/size] [font=宋体][size=15px][color=black]作者接着研究PF抑制ANIT诱导细胞焦亡的分子机制,通过蛋白芯片来筛选PF的直接作用靶标。结果表明,PF与GSDMD具有较高的亲和力,提示PF可能通过直接结合GSDMD抑制焦亡。进一步作者通过分子对接、CETSA、SPR等实验验证了PF与GSDMD之间的结合,这些结果共同表明PF直接与GSDMD蛋白结合(图4)。[/color][/size][/font] [align=center] [/align][align=center][font=宋体][size=15px][color=black][/color][/size][/font][/align][align=center] [/align] [size=15px][b][font=宋体][color=#0070c0]5[/color][/font][font=宋体][color=#0070c0]、PF通过GSDMD抑制炎症因子的释放[/color][/font][font=宋体][color=#0070c0][/color][/font][/b][/size] [font=宋体][size=15px][color=black]在焦亡信号通路中,细胞通常积累大量的pro-il -1β和pro-IL-18。caspase-1的激活是将这些促炎因子切割成活性形式所必需的。Caspase-1也裂解GSDMD,导致膜孔的形成,GSDMD的激活和随后的毛孔形成促进了裂解的活性炎症因子的快速释放引起局部或全身炎症反应。作者发现模型组炎症因子的表达明显升高,然而,体内和体外实验均表明高剂量PF组IL-1β、IL-18、IL-1β和IL-18的表达显著下调。LDH水平升高是焦亡的常见指标,作者发现模型组大鼠血清和肝组织中LDH释放量明显增加,PF治疗显著逆转了这些效应。这些结果表明,PF可能通过靶向GSDMD来减轻ANIT诱导的焦亡,从而抑制下游炎症因子的释放(图5)。[/color][/size][/font] [align=center] [/align][align=center][font=宋体][size=15px][color=black][/color][/size][/font][/align][align=center] [/align] [size=15px][b][font=宋体][color=#0070c0]总结[/color][/font][font=宋体][color=#0070c0][/color][/font][/b][/size] [font=宋体][size=15px][color=black]研究发现 PF 给药可减轻ANIT诱导的肝脏病理,增强肝功能标志物,并提高细胞活力。网络药理学和焦亡抑制剂研究表明,PF可能通过NLRP3依赖性焦亡途径减轻CT。Western blot、IF 和IHC 分析进一步支持了这一假设,这表明PF有可能抑制CT中NLRP3依赖性焦亡。通过蛋白芯片筛选将GSDMD确定为靶点。通过MD、 MDS[i][/i]、CETSA和SPR技术验证PF与 GSDMD 的结合亲和力。此外,ELISA和IHC证实了GSDMD对下游炎症通路的调节影响。总之,PF在ANIT诱导的CT中表现出保肝作用,主要是通过靶向GSDMD,从而抑制ANIT诱导的细胞焦亡和随后的炎症介质释放。[/color][/size][/font] [align=center][img=,690,430]https://ng1.17img.cn/bbsfiles/images/2024/09/202409101152102873_6541_6561489_3.png!w690x430.jpg[/img][img=,690,683]https://ng1.17img.cn/bbsfiles/images/2024/09/202409101152107014_173_6561489_3.png!w690x683.jpg[/img][img=,690,843]https://ng1.17img.cn/bbsfiles/images/2024/09/202409101152103146_2762_6561489_3.png!w690x843.jpg[/img][img=,690,453]https://ng1.17img.cn/bbsfiles/images/2024/09/202409101152108627_6893_6561489_3.png!w690x453.jpg[/img][img=,690,460]https://ng1.17img.cn/bbsfiles/images/2024/09/202409101152108231_8089_6561489_3.png!w690x460.jpg[/img][img=,690,726]https://ng1.17img.cn/bbsfiles/images/2024/09/202409101152104087_8784_6561489_3.png!w690x726.jpg[/img] [/align][align=center][font=宋体][size=15px][color=black][/color][/size][/font][/align][align=center] [/align] [font=宋体][size=15px] [/size][/font]
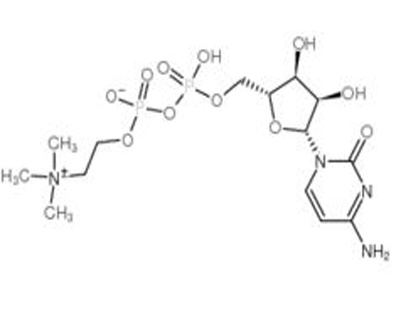
β-D-阿糖胞苷与阿糖胞苷红外图有没有区别呀?






 400-611-9236
400-611-9236
 留言咨询
留言咨询
 留言咨询
留言咨询

 留言咨询
留言咨询


