推荐厂家
暂无
暂无

【作者】 刘近荣;【机构】 山西泰盛制药有限公司;【摘要】 目的建立以高效液相色谱法测定黄芪总皂苷氯化钠注射液中黄芪甲苷含量的方法。方法色谱柱为DiamonsilC18(5μm,4.6×250mm),流动相为乙腈-水(36:64),流速为0.8ml/min,柱温为室温。结果黄芪甲苷进样量在5μg~40μg范围内与峰面积积分值线性关系良好(r=0.9993,n=5),平均加样回收率为99.75%(RSD=0.57%)。结论本方法测定结果准确、操作简便、灵敏度高、重复性好,可用于本品的质量控制。 更多还原http://ng1.17img.cn/bbsfiles/images/2012/08/201208131255_383443_2379123_3.jpg
[align=center][b]HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS法测定黄芪醇提物中的黄芪甲苷的含量[/b][/align][b]黄芪甲苷是黄芪皂苷提取物中的特征性成分,也是具有代表性的主要成分,黄芪甲苷可以促进患者心肌细胞的供氧能力,使冠状动脉供血区供血充足,避免因缺血导致的大范围心肌坏死,继而缓解患者心绞痛症状,平稳心跳速率[sup][/sup]。药典中有关于黄芪药材中黄芪甲苷含量的测定方法,但此方法并不完全适用于黄芪醇提物中的黄芪甲苷的含量测定,而且黄芪水提物与黄芪醇提物中化学成分有差异,预实验中发现测定黄芪水提物中黄芪甲苷含量建立的方法也不适应于黄芪醇提物中中黄芪甲苷含量的测定。本章实验利用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用仪[/color][/url]建立黄芪醇提物中黄芪甲苷含量测定方法,并利用该方法测定其含量,计算出黄芪甲苷的转移率,用于黄芪醇提最佳提取工艺的优选。同时,本章实验系统地验证所建立的方法的可行性,为选择黄芪甲苷的含量测定方法提供参考。[b]1 材料和仪器1.1 样品 [/b] 收集9组黄芪醇提物样品,所有黄芪药材均由济宁华能制药厂提供。[b]1.2 试剂 [/b]黄芪甲苷对照品(成都瑞芬思生物科技有限公司批号H-013-170117);乙腈为色谱纯(赛默飞世尔科技有限公司);D101大孔吸附树脂(廊坊淼阳化工有限公司生产20160310);盐酸溶液(国药集团化学试剂有限公司生产);氢氧化钠溶液(国药集团化学试剂有限公司生产20160824);超纯水。[b]1.3 仪器 [/b]液相色谱仪系统(美国Agligent Technology 公司1260型液相色谱仪,包括G1312B二元泵,G1322A在线脱气机,G1316A柱温箱);NASCA F5100型自动进样器(日本SHISEIDO公司);资生堂CAPCELL PAC CN 色谱柱(2.0*150 mm,5 mm,日本SHISEIDO公司);API 4000型三重四级杆串联离子肼质谱仪(美国Applicated Biosystem Scuex公司)。[b]2 方法学考察2.1 色谱条件[/b]色谱柱为 Synergi C18 80A(250 mm×4.6 mm,4 μm),以十八烷基硅烷键合硅胶为填充剂,以乙腈-水(35 : 65)进行等度洗脱;进样量10 μL;检测波长为203 nm;柱温30 ℃,流速为1 mL/min。黄芪甲苷保留时间约为10 min。黄芪醇提物和黄芪甲苷标准品HPLC色谱图见表5-1,表5-2。[/b][align=center][img=,690,365]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711071808_2711_3237657_3.png!w690x365.jpg[/img][/align][align=center]图5-1 黄芪醇提物HPLC色谱图[/align][align=center][img=,690,373]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711240945_4181_3237657_3.png!w690x373.jpg[/img][/align][align=center]图5-2 黄芪甲苷标准品HPLC色谱图[/align][b]2.2 质谱条件 [/b]电喷雾电离,正离子模式(喷雾电压:4.5 kV);鞘气压力:30 arb;辅助气压力:10 arb;离子传输管温度:550 ℃;扫描模式:全扫描;扫描范围:m/z 100-1000。按“2.1.3”项下色谱条件进样,进样量10 μL。为进一步验证10 min出峰的物质是黄芪甲苷,利用LC/MS技术对黄芪皂苷提取物的化学成分进行研究,采用正离子源ESI检测。黄芪甲苷分子量784.97 Da,由于仪器差异,黄芪甲苷出峰时间后移至12.5 min,此峰的鉴定结果质谱图显示含大量黄芪甲苷。图5-3为黄芪皂苷提取物的正离子模式HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]总离子流图、分离子流图和质谱图。[align=center][img=,690,426]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711415732_2681_3237657_3.png!w690x426.jpg[/img][/align][align=center]图5-3 黄芪甲苷正离子模式HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] 总离子流图、分离子流图和质谱图[/align][b]2.3 供试品溶液的制备[/b]对D101大孔吸附树脂预处理:第一步用乙醇或甲醇清洗吸附柱内壁,向柱内加入称量好的树脂体积0.4-0.5倍的乙醇或甲醇,然后将新的D101大孔吸附树脂投入吸附柱中,使乙醇液面高于D101大孔吸附树脂层0.5 m,浸泡过夜。用2 个柱体积的乙醇或甲醇通过D101大孔吸附树脂层,用乙醇缓慢浸泡D101大孔吸附4-5 h,观察洗脱液加水后不呈白色浑浊为止。再用蒸馏水以2 BV洗柱,洗至洗脱液呈中性。用2 BV的5 %盐酸溶液以4-6 BV/h过柱,浸泡2-4 h。用蒸馏水以2 BV/h洗至洗脱液呈中性。用2 BV的2 %氢氧化钠溶液以4-6 BV/h过柱,浸泡2-4 h。最后用蒸馏水洗D101大孔吸附树脂,洗至洗脱液显中性即可。上样:取黄芪醇提物加水溶解至15 mL得黄芪提取液,以1 mL/min过树脂,先以4 BV蒸馏水洗脱,弃去水液,再用4 BV的70 %乙醇溶液洗脱,用烧杯收集吸附柱内的洗脱液,转入蒸发皿,水浴蒸干后,用甲醇溶解并转移至10 mL容量瓶定容。[b]2.4 对照品溶液的制备[/b]用万分之一天平精密称取10.1 mg黄芪甲苷对照品至10 mL容量瓶,加甲醇定容,得1.01mg/mL的对照品溶液,用0.22μm的微孔滤膜过滤,备用。[b]3 结果3.1 线性关系考察[/b]精密量取黄芪甲苷标准品10.1 mg黄芪甲苷,用甲醇10 mL制备成1.01 mg/mL黄芪甲苷储备液,然后吸取相应体积稀释成浓度梯度为150 μg/mL、250 μg/mL、300 μg/mL、400 μg/mL 、500 μg/mL的对照品溶液,上述对照品溶液按“2.3”项下色谱条件分别进样10 μL,利用自动积分功能测定峰面积积分值,以黄芪皂苷提取物中黄芪甲苷的峰面积积分值对标准品浓度进行线性回归,所得回归方程为y = 2821.6x + 12.438(回归系数[i]R[sup]2[/sup][/i]= 0.9989),证明蒙古黄芪中黄芪甲苷在150~500 μg/mL范围内线性关系良好,黄芪甲苷对照品标准曲线如图5-4所示。[align=center][img=,542,346]https://ng1.17img.cn/bbsfiles/images/2019/08/201908131711574358_4557_3237657_3.png!w542x346.jpg[/img][/align][align=center]图5-4 黄芪甲苷标准曲线[/align][b]3.2 精密度试验[/b]在拟定分析条件下,精密吸取供试品溶液10 μL,连续进样 6 次,记录提取离子流图峰面积,测定黄芪甲苷量,计算得相对标准偏差RSD为1.9% ,提示该方法具有较好的精密度。[b]3.3 重复性实验[/b]取同一黄芪样品 6份,按2. 2 项下方法制备供试品溶液,在拟定分析条件下,准确吸取10 μl 进样分析,测定黄芪甲苷量,计算得 RSD为2.0%,提示该方法重复性良好。[b]3.4 稳定性试验[/b]取黄芪药材供试品溶液,分别在0 h、3 h、6 h、9 h、24 h、48 h后,在拟定分析条件下,准确吸取10 μl 进样分析,测定黄芪甲苷量,计算得RSD为 4.4% ,提示黄芪供试品溶液稳定性较差。[b]3.5 加样回收率试验[/b]精密称取 6 份黄芪甲苷量已知的黄芪水提物样品,每份折合黄芪药材 0. 5 g,分别准确加入浓度为 0. 0 342 mg /ml 黄芪甲苷溶液1 ml,1 ml,2ml,2ml,3ml,3ml,按 2. 2 项下方法制备供试品溶液,准确吸取 1. 0 μl 进样分析,测定黄芪甲苷量,计算回收率,结果见表3-1。由表3-1可见,方法平均回收率为 97.92%,表明该方法具有较好的回收率。[align=center]表5-1 黄芪甲苷加样回收率测定结果[/align] [table][tr][td] [align=center]样号[/align] [/td][td] [align=center]样品中的量/mg[/align] [/td][td] [align=center]加入量/mg[/align] [/td][td] [align=center]测得量/mg[/align] [/td][td] [align=center]回收率/%[/align] [/td][td] [align=center]平均值/%[/align] [/td][td] [align=center]RSD/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]0.96 [/align] [/td][td] [align=center]2.88 [/align] [/td][td] [align=center]97.92 [/align] [/td][td=1,6] [align=center]97.92 [/align] [/td][td=1,6] [align=center]0.7 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]0.96 [/align] [/td][td] [align=center]2.89 [/align] [/td][td] [align=center]98.96 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]1.92 [/align] [/td][td] [align=center]3.83 [/align] [/td][td] [align=center]98.44 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]1.92 [/align] [/td][td] [align=center]3.81 [/align] [/td][td] [align=center]97.40 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]2.88 [/align] [/td][td] [align=center]4.76 [/align] [/td][td] [align=center]97.92 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]1.94 [/align] [/td][td] [align=center]2.88 [/align] [/td][td] [align=center]4.73 [/align] [/td][td] [align=center]96.88 [/align] [/td][/tr][/table][b]3.6 黄芪甲苷的含量测定结果[/b]取9组黄芪水提物按照“2.3”项下操作,制备供试品溶液,准确吸取 1 0 μL 进样分析,在拟定的分析条件下,测定黄芪甲苷峰面积积分值,计算相应的黄芪甲苷含量。9组蒙古黄芪中黄芪甲苷含量测定结果如表5-2所示。[align=center]表5-2 9组蒙古黄芪中黄芪甲苷含量测定结果[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]峰面积[/align] [/td][td] [align=center]含量(mg/g)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]560.07 [/align] [/td][td] [align=center]0.13 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]501.70 [/align] [/td][td] [align=center]0.12 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]564.61 [/align] [/td][td] [align=center]0.13 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]507.19 [/align] [/td][td] [align=center]0.12 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]524.05 [/align] [/td][td] [align=center]0.12 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]477.02 [/align] [/td][td] [align=center]0.11 [/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]921.07 [/align] [/td][td] [align=center]0.21 [/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]783.88 [/align] [/td][td] [align=center]0.18 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]924.71 [/align] [/td][td] [align=center]0.22 [/align] [/td][/tr][/table][b]3.7 黄芪甲苷转移率正交试验设计及结果[/b]醇提的黄芪甲苷转移率考察正交试验与醇提的出膏率考察正交试验设计相同,首先以乙醇作为提取溶剂,把影响药材提取效果的提取溶剂乙醇用量(A)、提取次数(B)、提取时间(C)确定为考察因素,以上三个考查因素各分3个水平考察,见表5-3。[align=center]表5-3 实验因素水平表[/align] [table][tr][td=1,2] [align=center]水平[/align] [/td][td=3,1] [align=center]因素[/align] [/td][/tr][tr][td] [align=center]A(乙醇用量/倍)[/align] [/td][td] [align=center]B(提取次数/次)[/align] [/td][td] [align=center]C(提取时间/h)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]4[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]8[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]10[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][/tr][/table]黄芪甲苷转移率=各实验组黄芪提取物中黄芪甲苷含量/原黄芪药材中黄芪甲苷含量×100%。原药材中毛蕊异黄酮苷的含量按照药典的方法测得的结果为0.4042mg/g。跟据实验数据,得到水提实验中设定的不同工艺条件下的毛蕊异黄酮苷的转移率,其中因素D为误差项,作直观分析表和方差分析表,见表5-4,5-5。[align=center]表5-4 黄芪甲苷转移率考察 L[sub]9[/sub](3[sup]4[/sup])正交试验表[/align] [table][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]32.01 [/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]28.60 [/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]32.28 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]28.92 [/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]29.91 [/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]27.16 [/align] [/td][/tr][tr][td] [align=center]试验号[/align] [/td][td] [align=center]A[/align] [/td][td] [align=center]B[/align] [/td][td] [align=center]C[/align] [/td][td] [align=center]D[/align] [/td][td] [align=center]黄芪甲苷 转移率/%[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]53.11 [/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]45.09 [/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]53.33 [/align] [/td][/tr][tr][td] [align=center]K1[/align] [/td][td] [align=center]92.89[/align] [/td][td] [align=center]114.04[/align] [/td][td] [align=center]104.26[/align] [/td][td] [align=center]115.25[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K2[/align] [/td][td] [align=center]85.99[/align] [/td][td] [align=center]103.60[/align] [/td][td] [align=center]110.85[/align] [/td][td] [align=center]108.87[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]K3[/align] [/td][td] [align=center]151.53[/align] [/td][td] [align=center]112.77[/align] [/td][td] [align=center]115.30[/align] [/td][td] [align=center]106.29[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]优水平[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center]3[/align] [/td][td] [align=center]1[/align] [/td][td] [align=center] [/align] [/td][/tr][tr][td] [align=center]R[/align] [/td][td] [align=center]65.54[/align] [/td][td] [align=center]9.17[/align] [/td][td] [align=center]11.04[/align] [/td][td] [align=center]8.96[/align] [/td][td] [align=center] [/align] [/td][/tr][/table][align=center]表5-5 黄芪甲苷转移率考察方差分析结果[/align] [table][tr][td] [align=center]方差来源[/align] [/td][td] [align=center]离差平方和[/align] [/td][td] [align=center]自由度[/align] [/td][td] [align=center]F[/align] [/td][td] [align=center]显著性[/align] [/td][/tr][tr][td] [align=center]A[/align] [/td][td] [align=center]864.64[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]46.01[/align] [/td][td] [align=center]*[/align] [/td][/tr][tr][td] [align=center]B[/align] [/td][td] [align=center]21.63[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]0.07[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]C[/align] [/td][td] [align=center]20.57[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]0.07[/align] [/td][td] [align=center]-[/align] [/td][/tr][tr][td] [align=center]D [/align] [/td][td] [align=center]14.18[/align] [/td][td] [align=center]2[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]-[/align] [/td][/tr][/table]注:F[sub]0.1[/sub](2,2)=9,F[sub]0.05[/sub](2,2)=19,*为有显著性,-为无显著性。从正交试验结果可知:醇提实验中,各因素对黄芪甲苷转移率的影响大小顺序为:A(乙醇用量)B(提取次数)C(提取时间);每个因素3水平之间的趋势为A[sub]3[/sub]A[sub]1[/sub]A[sub]2[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]3[/sub]C[sub]2[/sub]C[sub]1[/sub],直观分析得最佳提取工艺为A[sub]3[/sub]B[sub]1[/sub]C[sub]3[/sub],即加醇10倍量,提取1次,每次3h。表5-5的方差分析结果表明: A因素的影响具有统计学差异(PB(提取次数)C(提取时间);每个因素3水平之间的趋势为A[sub]3[/sub]A[sub]1[/sub]A[sub]2[/sub],B[sub]1[/sub]B[sub]3[/sub]B[sub]2[/sub],C[sub]3[/sub]C[sub]2[/sub]C[sub]1[/sub],直观分析得最佳提取工艺为A[sub]3[/sub]B[sub]1[/sub]C[sub]3[/sub],即加醇10倍量,提取1次,每次3h。表5-7的方差分析结果表明: A因素的影响具有统计学差异(P0.05),即乙醇用量对黄芪甲苷转移率具有显著影响。[b]4 讨论[/b]本章实验利用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]技术,测定了黄芪醇提物中黄芪甲苷的含量,并系统地验证所建立的方法的可行性,经过试验条件的摸索,黄芪甲苷的色谱条件为35 %乙腈洗脱,所建立的方法能够较好的将黄芪甲苷与其他成分分开,可用于黄芪皂苷中黄芪甲苷含量测定,黄芪甲苷稳定性试验结果RSD值高于2 %,可能是由于黄芪皂苷Ⅰ或黄芪皂苷Ⅱ在酸性水解的条件下易转化成黄芪皂苷Ⅳ,即黄芪甲苷,使黄芪水提物中黄芪甲苷在48h内的稳定性不好。根据三个因素水平趋势可知,随着乙醇的用量增加,黄芪甲苷的提取效率越来越高,实验设置中每次10倍量是最大乙醇用量,这是从大工业生产和节能降耗等方面考虑的结果。根据煎煮次数水平趋势,提取1次的黄芪甲苷转移率最大,这有可能是因为黄芪皂苷Ⅰ或黄芪皂苷Ⅱ在酸性水解的条件下易转化成黄芪皂苷Ⅳ,即黄芪甲苷,而黄芪皂苷Ⅰ或黄芪皂苷Ⅱ在第一次就较完全的被提取出来,随着时间增加,转换成黄芪皂苷Ⅳ,即黄芪甲苷,第二次时黄芪皂苷Ⅰ或黄芪皂苷Ⅱ的结构可能被破坏,影响其转化成黄芪甲苷。第三次时可能黄芪甲苷被提取的更彻底,转移率又开始小幅增大。在3h内,当提取时间增加,黄芪甲苷会逐渐增大,原因可能是黄芪甲苷的提取更加彻底,黄芪皂苷Ⅰ或黄芪皂苷Ⅱ转化成黄芪甲苷最多。实验设置中每次3h是最大提取时间,这也是从综合成本与效率的角度考虑的结果。因此,综合考虑,将加醇10倍量,提取1次,共3h作为最佳醇提实验工艺。由黄芪甲苷转移率结合出膏率的到的综合评分的结果可以看出,不同提取工艺对黄芪醇提物中黄芪甲苷的含量和出膏率的影响不同,其中7、8、9组评分较高,三个组的黄芪甲苷转移率相较于其他组也是最高,但第8组出膏率却相对较低,另外出膏率高低的顺序也不与黄芪醇提物中黄芪甲苷的转移率高低的顺序项一致,这说明出膏率与黄芪醇提物中黄芪甲苷的转移率并无明显的对应关系。[align=center]参考文献[/align] 朱燕辉, 严奉祥. 黄芪甲苷及其生物学活性.现代生物医学进展,2008, 8 ( 4 ) : 781-783.
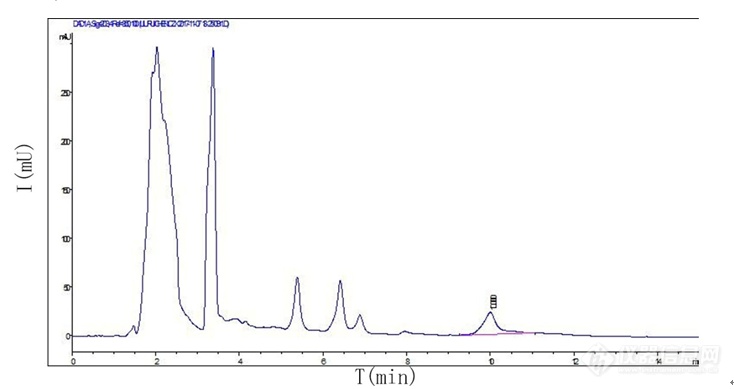
检测黄芪药材中的黄芪甲苷,用elsd检测器,c18柱,雾化管30 漂移管70 药典方法乙腈比水32比68 对照品塔板数11000,但是样品塔板数才2800,含量合格,要求塔板数是4000这是怎么回事,重做了好多次塔板数就是上不去






 400-892-9759
400-892-9759
 留言咨询
留言咨询

 留言咨询
留言咨询

 留言咨询
留言咨询


