推荐厂家
暂无
暂无
α-淀粉酶活性是衡量小麦穗发芽的一个生理指标,为此提出了对小麦α-淀粉酶活性的快速测定方法的研究。α-淀粉酶活性的测定方法有多种,本文仅探讨了常用的3,5-二硝基水杨酸法和凝胶扩散法。结果表明,两种方法的测定结果差异不显著,而且两者呈显著正相关;从变异系数上看,后者的变异程度较低,其精度较高;从误差来源上看,前者引起误差的因素较后者多;后者较为简便快速,准确度较高,重复性较好,可用于大批量样品的分析。关键词: 小麦, α-淀粉酶活性, 3,5-二硝基水杨酸法,凝胶扩散法1 材料和方法1.1 材料和试剂(1)萌芽的小麦:取当年小麦种子,按小麦萌发试验培养,两天后用于测验.(2)1%淀粉溶液.(3)0.4N NaOH.(4)pH5.6的柠檬酸缓冲液:A. 称取柠檬酸20.01克,溶解后稀释至1升;B.称取柠檬酸钠29.41克,溶解后稀释至1升。取A液13.7毫升与B液26.3毫升混匀,即为pH5.6的缓冲液.(5)3,5-二硝基水杨酸: 精确称取3,5-二硝基水杨酸1克溶于20毫升1N氢氧化钠中,加入50毫升蒸馏水,再加入30克酒石酸钾钠,待溶解后,用蒸馏水稀释至100毫升,盖紧瓶塞,勿使二氧化碳进入.(6)麦芽糖标准液:称取麦芽糖0.100克溶于少量蒸馏水中,仔细移入100ml容量瓶中,用蒸馏水稀释至刻度.(7)α_淀粉酶提取缓冲液:20mmol/L醋酸钠(2.7216g/L),1mmol/L氯化钙(0.11099g/L),pH 5.5.(8)%5(V/V)碘—碘化钾溶液:1.95gKI+0.65gI2溶解在100毫升蒸馏水中.(9)α_淀粉酶36.18u/mg (Sigma公司):逐级稀释10, 2.5,0.625 ,0.15625,0.03906, 0.009765mg/mL系列标准液.(10)20%冰乙酸,琼脂糖,可溶性淀粉.1.2 方法1.2.1 3.5一二硝基水杨酸测定法酶液提取从五个培养皿的发芽小麦中,各随机称取1克于研钵中,加少许α_淀粉酶提取缓冲液,研磨至匀浆,倒入离心杯中,于4000rpm离心10分钟,取上清液并并定容至25ml,即为酶提取液,备用。α_淀粉酶活性测定(1)取试管,注明对照管,测定器,每样品三个重复.(2)于每试管中各加酶液1ml,加70℃恒温水浴中加热15分钟,此期间β_淀粉酶受热钝化(3)每管中各加入1毫升pH5.06的柠檬酸缓冲液.(4)对照管中加入4毫升0.4NnaOH.(5)测定管与对照管置40℃水浴中保温10分钟,再向各管加入40℃下预热的淀粉溶液2毫升摇匀,立即放入40℃水浴中准确保温5分钟取出,向各测定管迅速加入4毫升0.4N的氢氧化钠,以终止酶活动.麦芽糖测定取以上各管中酶作用后的溶液及对照管中溶液各2毫升,分别放入25毫升试管中,再加2毫升3,5-二硝基水杨酸,混匀,置水浴中5分钟,冷却后定容至25毫升,混匀,用分光光度计在520nm波长下进行比色记录消光值,取麦芽糖标准液(1ml/mg)0,0.2,0.6 ,1.0,1.4,1.8,2.0ml。按上述同样方法比色后,将测得的消光值与麦芽糖标准液进行直线回归后,代入求得样品的麦芽糖含量,并换算成每克种子α_淀粉酶的活力单位。1.2.2 凝胶扩散测定法凝胶板制备取一长方形优质玻璃,除一宽边外,其余三边边缘各边一条透明胶片,再在上面盖一同等大小玻璃,两块玻璃两侧用夹子固定,放温箱中预热50-60℃,取三角烧杯,加30毫升α-淀粉酶提取缓冲液,0.36克琼脂糖和0.30克可溶性淀粉(作反应底物),在电炉上加热煮沸至透明后,冷却至70℃左右,将预热的玻璃胶片框架斜放在桌面上30℃,用预热的移液管吸取凝胶液,从玻璃架高一端空隙中均匀注入,直至其流遍整个胶片表面为止,不能有气泡。用量约25毫升冷却后形成凝胶板,贮存在4℃冰箱备用。α_淀粉酶活性测定取出预制冷藏的凝胶板,揭开上面一块玻璃,用塑料打孔器在凝胶板上每隔一定距离打一个1.33毫米的孔,用微量移释管向每孔内注入提取液。上述1.2.1制得的酶液于70℃水浴加热15分钟后钝化β-淀粉酶后备用。同时,在每块凝胶板孔中加入淀粉酶系列标准液(重复两次)。将凝胶板置10℃恒温箱中反应24小时后,取出,将胶板浸入I-KI溶液中染色5min,加入冰乙酸酸化终止反应。用蒸馏水淋洗3min,洗净染色液,由于加α_淀粉酶孔周围淀粉被分解,因而染色后出现未能染色的圆。未与α-淀粉酶反应的呈蓝色,用直径测量仪测圆直径。用α_淀粉酶标准液浓度对数与褪色圈直径直线回归,计算每克样品含α-淀粉酶活力单位数。2 结果和分析2.1 两种方法标准曲线2.1.1 麦芽糖标准曲线麦芽糖标准液含量越高,比色后记录的OD值越大,麦芽糖标准液比色后,测得的OD值(x)与麦芽糖浓度(y)进行直线回归,结果为:y=1.0240x+0.0897,r=0.9998,相关系数极显著,表明麦芽糖标准液含量与消光值呈直线关系,通过此直线方程可进一步测得酶活性;即将各样品的消光值代入回归方程,求得样品麦芽糖含量,然后计算可得每克种子的α_淀粉酶活力。2.1.2 α-淀粉酶标准曲线α_淀粉酶标准液浓度越高,其褪色圈直径越大,5个样品的褪色圈直径也有明显差异。将α-淀粉酶标样所测得褪色圈直径(x)与α-淀粉酶浓度对数(y)进行直线回归。结果为:y=2.4659x-3.8994, r=0.9860,相关系数极显著,表明褪色圈直径与淀粉酶标准液的浓度对数呈直线关系,通过此直线方程可进一步测得酶活性,即将各样品的褪色圈直径代入回归方程,求得各样品的α_淀粉酶浓度,然后换算成每克种子中α_淀粉酶的活力单位。2.2 两种方法测定结果比较对5个样品的淀粉酶活性,用两种方法测定,并记录了测定结果(表1)。表1 3,5-二硝基水杨酸法和凝胶扩散法结果 样品 3,5-二硝基水杨酸法 凝胶扩散法 消光值 酶活性 (u/g) 直径 酶活性(cm) (u/g) 1 0.1010 2.191.20 4.03 2 0.1580 6.701.35 6.72 3 0.1460 5.241.27 5.06 4 0.1667 6.961.45 7.14 5 0.1477 5.481.28 5.86对两组样本进行t测验,测定结果为:t=1.2855, t0.05=2.0776,|t|r0.05,表明两种结果相关系数显著,即两种方法从其中之一测定结果可以推算出另一方法的测定结果。2.3 两种方法的精度比较表2 两种方法变异数分析结果 方法 平均数(u/g) 标准差(u/g) 变异系数CV(%) 3,5-二硝基水杨酸法 5.314 [
[b]将玉米直链淀粉标准品与玉米支链淀粉标准品按不同比例混合,进行α-淀粉酶酶解反应,除直链淀粉与支链淀粉比例不同以外,其他条件均相同,结果见下图。 由图可知,淀粉中直链淀粉的含量影响α-淀粉酶酶解效率,直链淀粉含量越高,酶解速率越慢,酶解程度越低。 反应后,纯直链淀粉酶解产物的值为47% ,而纯支链淀粉酶解产物的值则达到56%。 Rendleman的研究结果也表明,玉米直链淀粉的α-淀粉酶酶解效率要明显低于支链淀粉,但张力田等人却得到相反的结果, 这可能是由于淀粉的酶解性能受多种因素影响,如分子量、直链淀粉脂质复合结构等。 原淀粉中直链含量较高的马铃薯淀粉和豌豆淀粉的α-淀粉酶酶解效率都较高,与图结果并不一致,这说明直链淀粉的含量可能不是导致几种淀粉酶解性能差异的主要因素,而结构更为复杂的支链淀粉则可能是其主要因素[/b]
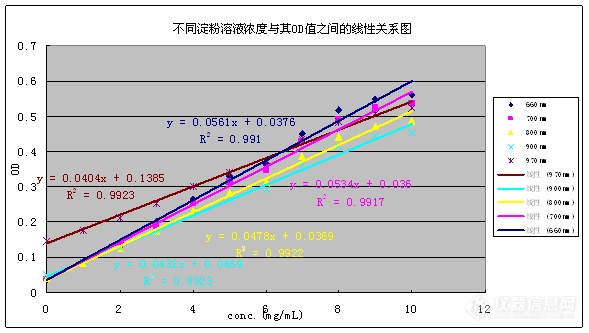
[align=center][b]使用酶标仪测定α-淀粉酶抑制率方法的研究[/b][/align][align=left][b]1.实验原理[/b][/align][align=left] 淀粉的消化主要有α-淀粉酶与α-葡萄糖苷酶的参与,α-淀粉酶水解α-1,4-连接键,消化的产物主要有麦芽糖、麦芽三糖、α-糊精,这些物质的进一步消化要在小肠上靠α-葡萄糖苷酶进行,α-葡萄糖苷酶主要包含麦芽-葡糖淀粉酶与蔗糖-异麦芽糖酶,α-葡萄糖苷酶水解的产物是葡萄糖。因此,通过抑制淀粉酶或葡萄糖苷酶的活性,阻碍食物中碳水化合物的水解与消化,减少糖分的吸收,以达到控制体内血糖浓度水平。[/align][align=left] 本实验是针对淀粉酶水解淀粉溶液而导致溶液中浑浊度的变化,测定溶液吸光度值的变化,以抑制剂阿卡波糖作为参照标准,抑制淀粉酶的能力以阿卡波糖当量来表达。[/align][align=left][b]2.实验方法与数据处理[/b] 将空白、样品或标准抑制剂Acarbose(阿卡波糖)与α-淀粉酶溶液混合均匀,37℃保温孵育15min,然后再加入淀粉溶液,快速振荡后在660nm迅速开始测定,利用酶标仪配备软件记录吸光度OD,初始吸光度值记为f1,以后每隔一段时间测定一个点,吸光度分别记为f1, f2 …,抑制剂作用下衰减曲线下的积分面积,扣除无抑制剂的空白曲线下面积,得出抑制剂的曲线下净面积(Net AUC)。衰退曲线下面积AUC可以近似看作各梯形面积之和,可以表达为:AUC=0.5×(f[sub]1[/sub]+f[sub]2[/sub])×ΔT+0.5×(f[sub]2[/sub]+f[sub]3[/sub])×ΔT+...+0.5×(f[sub]x[/sub]+f[sub]x+1[/sub])×ΔT+...+0.5×(f[sub]n-1[/sub] +f[sub]n[/sub])×ΔT=0.5×[2×(f[sub]1[/sub] +f[sub]2[/sub] +...+ f[sub]n-1[/sub] +f[sub]n[/sub])-f[sub]1[/sub] -f[sub]n[/sub]]×ΔT其中f[sub]n[/sub]代表第n个测定点时的吸光度,ΔT为相邻两个测定点之间的时间间隔,因本实验测定方法中ΔT设定为2min,一共有61测定点,因此该公式可以简化为:AUC=2×(f[sub]2[/sub]+f[sub]3[/sub]+...+f[sub]60[/sub])+ f[sub]1[/sub] + f[sub]61[/sub]以Acarbose当量μmol Acarbose equivalent/g (μmol AE/g)表达。[/align][align=left][b]3.试剂溶液的制备3.1 磷酸盐缓冲溶液3.1.1 CaCl[sub]2[/sub]溶液[/b]准确称取CaCl[sub]2[/sub]2H[sub]2[/sub]O粉末0.25g溶于100 mL ddH[sub]2[/sub]O,即为CaCl[sub]2[/sub]溶液2500mg/L。[b]3.1.2缓冲溶液工作液[/b]分别称取8.9g Na[sub]2[/sub]HPO[sub]4[/sub]2H[sub]2[/sub]O与6.9g NaH[sub]2[/sub]PO[sub]4[/sub]H[sub]2[/sub]O于1000 mL容量瓶中,再量取CaCl[sub]2[/sub]溶液20 mL,混合后用ddH[sub]2[/sub]O定容至1000 mL,这样得到0.1M,pH 6.9的缓冲溶液,冰箱下贮存。[b]3.2 玉米淀粉溶液[/b]玉米淀粉储备液:准确称取约1.0000g大米淀粉,加入50mL缓冲液,磁力搅拌数分钟后置于78℃左右水浴10分钟,于磁力搅拌器中搅拌自然冷却至室温,即为2%的淀粉溶液(20mg/mL);玉米淀粉工作液:将储备液用缓冲溶液依次分别稀释至1.0-10mg/mL的工作液。[b]3.3 α-淀粉酶溶液[/b]准确称取α-淀粉酶固体粉末(23U/mg)40mg,用缓冲溶液定容至10 mL,即为4mg /mL的α-淀粉酶储备液,再依次稀释至0.2、0.1、0.05、0.04、0.025 mg /mL的α-淀粉酶工作液。[b]3.4 Acarbose标准溶液的配制[/b]0.1g acarbose定容到100 mL磷酸缓冲液中,得到1mg /mL贮备液,然后用磷酸缓冲溶液依次稀释成的工作液0.01、0.02、0.03、0.04、0.05 mg /mL。[b]4.研究步骤[/b][/align][align=left][b]4.1 淀粉溶液的线性范围[/b] 由于本实验是对样品中浑浊度的变化来进行,而对浑浊度的测量不像紫外-可见分光光度计那样有理想的波长以及会出现明显的特征峰,根据文献大多数浑浊度的测量波长在620-700nm之间。为了确定玉米淀粉溶液的线性,我们选择玉米淀粉溶液的浓度在0-10mg/mL,波长选择660、700、800、900、970nm进行比较。使用玉米淀粉工作液0-10mg/mL,分别在660nm、700nm、800nm、900nm、970nm波长下测定其吸光度,重复测定3次。不同波长下淀粉溶液浓度与其OD值之间的线性关系图如下:[/align][align=left][img=,589,333]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171420555396_7331_1613776_3.png!w589x333.jpg[/img][/align][align=left][table][tr][td][align=center]波长/nm[/align][/td][td][align=center]线性相关系数R[sup]2[/sup][/align][/td][td][align=center]线性斜率[/align][/td][td][align=center]空白OD值[/align][/td][td][align=center]LOD检测限[/align][/td][td][align=center]LOQ定量限[/align][/td][/tr][tr][td][align=center]660[/align][/td][td][align=center]0.9910[/align][/td][td][align=center]0.0561[/align][/td][td][align=center]0.038±0.001[/align][/td][td][align=center]0.048[/align][/td][td][align=center]0.159[/align][/td][/tr][tr][td][align=center]700[/align][/td][td][align=center]0.9917[/align][/td][td][align=center]0.0534[/align][/td][td][align=center]0.038±0.001[/align][/td][td][align=center]0.052[/align][/td][td][align=center]0.174[/align][/td][/tr][tr][td][align=center]800[/align][/td][td][align=center]0.9922[/align][/td][td][align=center]0.0478[/align][/td][td][align=center]0.041±0.002[/align][/td][td][align=center]0.093[/align][/td][td][align=center]0.310[/align][/td][/tr][tr][td][align=center]900[/align][/td][td][align=center]0.9923[/align][/td][td][align=center]0.0432[/align][/td][td][align=center]0.051±0.002[/align][/td][td][align=center]0.108[/align][/td][td][align=center]0.361[/align][/td][/tr][tr][td][align=center]970[/align][/td][td][align=center]0.9923[/align][/td][td][align=center]0.0404[/align][/td][td][align=center]0.145±0.002[/align][/td][td][align=center]0.138[/align][/td][td][align=center]0.458[/align][/td][/tr][/table]从上图及上表中可以知道,玉米淀粉浓度在0-10mg/mL时的线性关系均较好,相关系数均在0.99以上。虽然线性相关系数较低,但在波长660nm下的线性斜率高于其他波长下的线性斜率,且LOD检测限与LOQ定量限均是最小,因此选择波长660nm作为测定波长。[/align][align=left][b]4.2 淀粉酶的活力[/b] 将20μL的缓冲溶液与20μL的不同浓度α-淀粉酶溶液混合均匀,37℃保温孵育15min,然后再加入60μL的2%淀粉溶液,快速振荡后在660nm迅速开始测定其吸光度值。以不同浓度的淀粉酶浓度0.4、0.2、0.1、0.05、0.04、0.025 mg /mL,底物选择20mg/mL的淀粉溶液进行试验,在660nm下测定其吸光度值的变化曲线。660nm下其吸光度值的衰退曲线图:[/align][align=left][img=,672,359]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171423163167_2471_1613776_3.png!w672x359.jpg[/img][/align][align=left]从上图,在660nm波长下,不同淀粉酶浓度使淀粉溶液的吸光度下降,而且淀粉酶浓度越大,吸光度下降的越快。AUC与淀粉酶浓度成负相关关系,随着酶浓度的增大,曲线下面积AUC逐渐减小。[/align][align=left][b]4.3 抑制剂阿卡波糖活力[/b] 采用不同浓度的阿卡波糖浓度0.01、0.02、0.03、0.04、0.05 mg /mL分别进行试验(n=3),淀粉溶液的浓度选择20mg/mL,淀粉酶浓度选择0.2mg /mL。通过试验,各个不同浓度的阿卡波糖抑制曲线图如下:[/align][align=left][img=,687,390]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171426550249_8100_1613776_3.png!w687x390.jpg[/img][img=,668,320]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171426580379_7253_1613776_3.png!w668x320.jpg[/img][/align][align=left]从上图看出,阿卡波糖浓度 在0.01-0.05 mg /mL之间与其曲线下净面积Net AUC的线性较好,相关系数R[sup]2[/sup]=0.9972。[/align][align=left][b]4.4 线性研究[/b] 以不同浓度的阿卡波糖0.01、0.02、0.03、0.04、0.05、0.06、0.07mg /mL分别进行试验,淀粉溶液的浓度选择20mg/mL,淀粉酶浓度选择0.2mg /mL。通过试验,各个不同浓度的阿卡波糖抑制曲线图如下:[/align][align=left][img=,690,359]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171427557847_1976_1613776_3.png!w690x359.jpg[/img][/align][align=left]不同浓度的阿卡波糖与其曲线下净面积Net AUC的线性关系图如下(重复试验7次):[/align][align=left][img=,690,359]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171427580179_2403_1613776_3.png!w690x359.jpg[/img][/align][align=left][table][tr][td][align=center]n[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][td][align=center]6[/align][/td][td][align=center]7[/align][/td][td][align=center]av[/align][/td][td][align=center]SD[/align][/td][td][align=center]%RSD[/align][/td][/tr][tr][td][align=center]R[sup]2[/sup][/align][/td][td][align=center]0.9909[/align][/td][td][align=center]0.9806[/align][/td][td][align=center]0.9788[/align][/td][td][align=center]0.9942[/align][/td][td][align=center]0.9934[/align][/td][td][align=center]0.991[/align][/td][td][align=center]0.9932[/align][/td][td][align=center]0.9889[/align][/td][td][align=center]0.0064[/align][/td][td][align=center]0.6477[/align][/td][/tr][tr][td][align=center]SLOPE[/align][/td][td][align=center]4433.9[/align][/td][td][align=center]4850.1[/align][/td][td][align=center]4500[/align][/td][td][align=center]4219.3[/align][/td][td][align=center]5675.1[/align][/td][td][align=center]4468[/align][/td][td][align=center]5110.9[/align][/td][td][align=center]4751[/align][/td][td][align=center]503.27[/align][/td][td][align=center]10.593[/align][/td][/tr][/table]从上表看出,不同浓度的阿卡波糖与其曲线下净面积Net AUC之间的线性相关系数R[sup]2[/sup]在0.9889±0.0064之间,相对标准偏差0.65%;斜率在4751±503.3之间,相对标准偏差10.6%。[/align][align=left][b]4.5 提取溶剂的影响[/b]对提取溶剂(丙酮:乙醇:水的混合溶剂)进行研究,即以提取溶剂代替缓冲溶液进行试验,并与缓冲溶液进行比较。[/align][align=left][img=,609,340]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171437196510_7149_1613776_3.png!w609x340.jpg[/img][/align][align=left]其中:BLK——20μL缓冲溶液+20μL淀粉酶+60μL淀粉;BLK1——20μL提取溶剂+20μL淀粉酶+60μL淀粉;Emp——40μL缓冲溶液+60μL淀粉;Emp1——40μL提取溶剂+60μL淀粉。[/align][align=left]通过对提取溶剂稀释10、100、1000、10000倍后再进行同样试验(如下图):[/align][align=left][img=,657,362]https://ng1.17img.cn/bbsfiles/images/2018/10/201810171438035079_1244_1613776_3.png!w657x362.jpg[/img][/align][align=left]从图上看出,通过对提取溶剂稀释10、100、1000、10000倍后试验,基本对测定无影响。[/align][align=left][b][b]4.6 样品检测[/b][/b][/align][align=left][b] 将[/b]样品提取液代替阿卡波糖加入到淀粉酶溶液中,37℃保温孵育15min,然后再加入淀粉溶液,快速振荡后在660nm迅速开始测定。通过计算得出样品中的AE(阿卡波糖当量)。也可以通过比较抑制率IC50,来判断样品中的淀粉酶抑制率强弱。[/align][align=left][b]5.小结[/b] 通过以上对α-淀粉酶抑制率试验方法进行研究,实验表明,该方法适用于样品中α-淀粉酶抑制率的筛选。[/align][align=left]注意事项:[/align][align=left]1. 标准溶液或者样品与淀粉酶溶液混合后需在37℃保温孵育15min,再加入淀粉溶液;[/align][align=left]2. 加入淀粉溶液让后需要快速振荡后在660nm迅速开始测定;[/align][align=left][b]6.参考文献[/b]1. LEE WAH KOH, LIN LING WONG, YING YAN LOO, STEFAN KASAPIS, AND DEJIAN HUANG. J. Agric. Food Chem. 2010, 58, 148-1542. ALVIN ENG KIAT LOO AND DEJIAN HUANG. J. Agric. Food Chem. 2007, 55, 9805-98103. Elena Lo Piparo, Holger Scheib,Nathalie Frei, Gary Williamson, Martin Grigorov, and Chieh Jason Chou. J. Med. Chem. 2008, 51, 3555-35614. TOSHIRO MATSUI, TAKASHI TANAKA, SATOMI TAMURA, ASAMI TOSHIMA,KEI TAMAYA,YUJI MIYATA,KAZUNARI TANAKA, AND KIYOSHI MATSUMOTO. J. Agric. Food Chem. 2007, 55, 99-105[/align]







 400-801-9298
400-801-9298
 留言咨询
留言咨询

 400-860-5168转2390
400-860-5168转2390
 留言咨询
留言咨询

 400-860-5168转6008
400-860-5168转6008
 留言咨询
留言咨询