推荐厂家
暂无
暂无
[font=宋体]中国食品药品检定研究院(以下简称“中检院”)对卡铂、来那度胺和硫普罗宁杂质Ⅱ标准物质原料采购项目进行公告,现诚邀符合项目要求的供应商报名参加。[/font][font=宋体]一、项目基本情况[/font][font=宋体]项目名称:中检院卡铂、来那度胺和硫普罗宁杂质Ⅱ标准物质原料采购项目[/font][font=宋体]项目编号:ZFCG202300002[/font][font=宋体]项目需求:[/font][table][tr][td=1,1,52][font=宋体]序号[/font][/td][td=1,1,124][font=宋体]品种名字[/font][/td][td=1,1,150][font=宋体]预算金额(万元)[/font][/td][td=1,1,94][font=宋体]采购数量[/font][/td][td=1,1,98][font=宋体]货期要求[/font][/td][/tr][tr][td=1,1,52][font=宋体]1[/font][/td][td=1,1,124][font=宋体]卡铂[/font][/td][td=1,1,150][font=宋体]5.1[/font][/td][td=1,1,94][font=宋体]300g[/font][/td][td=1,1,98][font=宋体]一个月[/font][/td][/tr][tr][td=1,1,52][font=宋体]2[/font][/td][td=1,1,124][font=宋体]来那度胺[/font][/td][td=1,1,150][font=宋体]6[/font][/td][td=1,1,94][font=宋体]300g[/font][/td][td=1,1,98][font=宋体]二个月[/font][/td][/tr][tr][td=1,1,52][font=宋体]3[/font][/td][td=1,1,124][font=宋体]硫普罗宁杂质Ⅱ[/font][/td][td=1,1,150][font=宋体]10[/font][/td][td=1,1,94][font=宋体]200g[/font][/td][td=1,1,98][font=宋体]三个月[/font][/td][/tr][/table][font=宋体] [/font][font=宋体]技术要求:[/font][font=宋体]1.[/font][font=宋体]卡铂:同一批号、均匀且纯度≥99.5%,符合现行国家药品标准规定,提供检验报告书;资质要求:具有该品种原料生产许可证或持有该品种制剂批准文号的生产企业。[/font][font=宋体]2.[/font][font=宋体]来那度胺:同一批号、均匀且纯度≥99.5%,符合现行国家药品标准规定,提供检验报告书;资质要求:具有该品种原料生产许可证或持有该品种制剂批准文号的生产企业。[/font][font=宋体]3.[/font][font=宋体]硫普罗宁杂质Ⅱ:同一批号、均匀且纯度≥99%,符合现行国家药品标准规定。提供检验报告书,并附结构确证、纯度分析、稳定性资料及相关图谱。[/font][font=宋体]4.[/font][font=宋体]原料质保期要求:在标化合格后一年内。[/font][font=宋体]二、供应商资格要求[/font][font=宋体]1.[/font][font=宋体]具有独立承担民事责任的能力;[/font][font=宋体]2.[/font][font=宋体]具有良好的商业信誉和健全的财务会计制度;[/font][font=宋体]3.[/font][font=宋体]具有履行合同所必需的专业技术能力;[/font][font=宋体]4.[/font][font=宋体]有依法缴纳税收和社会保障资金的良好记录;[/font][font=宋体]5.[/font][font=宋体]参加政府采购活动前三年内,在经营活动中没有重大违法记录;[/font][font=宋体]6.[/font][font=宋体]资格审查时,通过“信用中国”网站、中国政府采购网、国家企业信用信息公示系统、天眼查、企查查网站等渠道查询供应商信用记录,经查询列入失信被执行人、重大税收违法案件当事人名单、政府采购严重违法失信行为记录名单、经营异常名录信息、严重违法失信企业名单(黑名单)信息的,经查询在经营活动中有重大违法记录的,截至本项目采购活动开始前三年内因违法经营受到刑事处罚或者责令停产停业、吊销许可证或者执照、较大数额罚款等行政处罚的,不得参加本项目;[/font][font=宋体]7.[/font][font=宋体]单位负责人为同一人或者存在控股、管理关系的不同单位,不得参加同一项目响应;[/font][font=宋体]8.[/font][font=宋体]本项目不接受联合体参加,禁止转包或分包;[/font][font=宋体]9.[/font][font=宋体]法律、行政法规规定的其他条件。[/font][font=宋体]三、报名方式[/font][font=宋体]1.[/font][font=宋体]本项目采取网上报名的方式,不设现场报名及其他形式的报名。符合项目要求的潜在供应商需填写完整报名表(附件1)发送至邮箱hqzc@nifdc.org.cn。(邮件命名:项目名称+报名单位名称)[/font][font=宋体]2.[/font][font=宋体]报名供应商需提交真实有效的响应文件(附件2)并加盖公章,密封邮寄至中检院联系人处。[/font][font=宋体]3.[/font][font=宋体]报名和文件邮寄送达时间截止至2023年1月19日(北京时间),逾期送达不予接收。[/font][font=宋体]四、供应商确定原则[/font][font=宋体]请报名供应商以单品种总价进行报价,本项目根据质量和服务均能满足实质性响应且报价最低原则确定供应商。[/font][font=宋体]五、联系方式[/font][font=宋体]采购单位:中国食品药品检定研究院[/font][font=宋体]地址:北京市大兴区生物医药产业基地华佗路31号院后勤政采部[/font][font=宋体]联系人: 袁玉萍[/font][font=宋体]联系电话:010-53852873[/font][font=宋体]电子邮箱:hqzc@nifdc.org.cn [/font][font=宋体]附件:[/font][font=宋体]1.[/font][font=宋体]报名表[/font][font=宋体]2.[/font][font=宋体]供应商响应文件[/font][align=right][font=宋体]中检院[/font][/align][align=right][font=宋体]2023[/font][font=宋体]年1月11日[/font][/align]【附件】[list][*][img]https://www.nifdc.org.cn/directory/web/fileTypeImages/icon_xls.gif[/img] [url=https://www.nifdc.org.cn/directory/web/nifdc/infoAttach/161b0e45-7a85-425c-ba18-db5c6983f1db.xlsx]附件1:报名表.xlsx[/url][*][img]https://www.nifdc.org.cn/directory/web/fileTypeImages/icon_xls.gif[/img] [url=https://www.nifdc.org.cn/directory/web/nifdc/infoAttach/7df1e302-bf54-4d16-8982-4be1494103e4.xlsx]附件2:供应商响应文件.xlsx[/url][/list]
如题,俺第一次测盐酸左氧氟沙星,做有关物质时杂质A与左氧保留时间完全重叠,排除了乙酸铵、高氯酸钠等试剂滴原因,实在没辙咧,请教大虾帮忙。盐酸左氧氟沙星有关物质测定方法(来源:中国药典2010年版第一增补本): 有关物质 取本品,精密称定,加0.lmol/L盐酸溶液溶解并定量稀释制成每1ml中约含1.2mg的溶液,作为供试品溶液,精密量取适量,用0.1mol/L盐酸溶液定量稀释制成每1ml中含2.4ug的溶液,作为对照溶液。另精密称取杂质A对照品约18mg,置100ml量瓶中,加6mol/L氨溶液1ml与水适量使溶解,用水稀释至刻度,摇匀,精密量取2ml,置100ml量瓶中,用水稀释至刻度,摇匀,作为杂质A对照品溶液。照高效液相色谱法(附录V D)测定,用十八烷基硅烷键合硅胶为填充剂;以醋酸铵高氯酸钠溶液(取醋酸铵4.0g和高氯酸钠7.0g,加水1300ml使溶解,用磷酸调节pH值至2.2)-乙腈(85 :15)为流动相A,乙腈为流动相B;按下表进行线性梯度洗脱。柱温为40°C;流速为每分钟1ml。称取左氧氟沙星对照品、环丙沙星对照品和杂质E对照品各适量,加0.1mol/L盐酸溶液溶解并稀释制成每1ml中约含左氧氟沙星1.2mg、环丙沙星和杂质E各6ug的混合溶液,取10ul注人液相色谱仪,以294nm为检测波长,记录色谱图,左氧氟沙星峰的保留时间约为15分钟。左氧氟沙星峰与杂质E峰和左氧氟沙星峰与环丙沙星峰的分离度应分别大于2.0与2.5。量取对照溶液10ul注人液相色谱仪,以294mn为检测波长,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%。精密量取供试品溶液、对照溶液和杂质A对照品溶液各10ul,分别注人液相色谱仪,以294nm和238nm为检测波长,记录色谱图。供试品溶液色谱图中如有杂质峰,杂质A(238nm检测)按外标法以峰面积计算,不得过0.3%。其他单个杂质(294nm检测)峰面积不得大于对照溶液主峰面积(0.2%),其他各杂质(294nm检测)峰面积的和不得大于对照溶液主峰面积的2.5倍(0.5%)。供试品溶液色谱图中任何小于对照溶液主峰面积0.1倍的峰可忽略不计。时间(分钟) 流动相A(%) 流动相B(%) 0 100 0 18 100 0 25 70 30 39 70 30 40 100 0 50 100 0
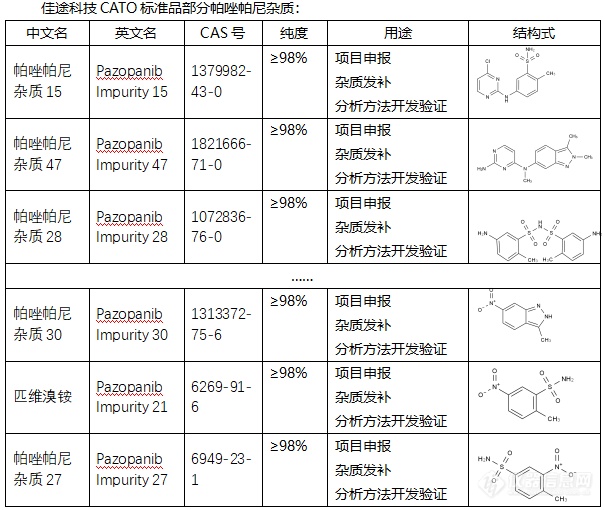
◇帕唑帕尼杂质 帕唑帕尼杂质是在帕唑帕尼药物制备或存储过程中可能产生的物质。帕唑帕尼杂质有多种,其中一些具有特定的CAS号、化学式和分子量。例如,帕唑帕尼杂质(Pazopanib Impurities)的CAS号为59816-94-3,化学式为C22H22N8,分子量为398.46。此外,帕唑帕尼杂质还包括一些异构体和其他结构类似物,如Pazopanib Isomer等。 CATO标准品提供的帕唑帕尼全套的杂质,这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分。[img=,605,510]https://ng1.17img.cn/bbsfiles/images/2024/02/202402192050040241_6306_6381607_3.png!w605x510.jpg[/img] 广州佳途科技股份有限公司深知药物研发与质量控制的重要性,CATO标准品厂家,提供帕唑帕尼全套的杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展,以满足客户在药物研发和质量控制方面的需求。







 400-860-5168转2831
400-860-5168转2831
 留言咨询
留言咨询

 400-860-5168转1610
400-860-5168转1610
 留言咨询
留言咨询

 400-860-5168转1610
400-860-5168转1610
 留言咨询
留言咨询