【瑞士步琦】冷冻干燥含酵母菌的微球应用
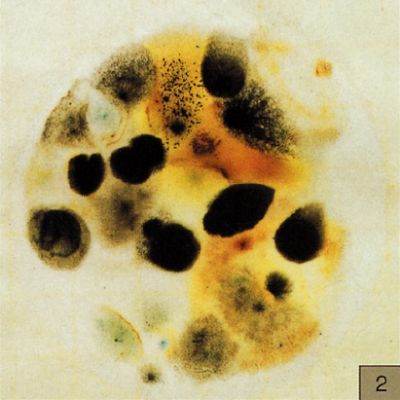
瑞士步琦冷冻干燥含酵母菌的微球应用冷冻干燥应用”益生菌是一种有益于人体健康的微生物,常被用于改善肠道菌群。微胶囊包埋技术可以帮助保护菌株,延长其在体内的存活时间,不易受外界环境的影响而失活。因此,在生产益生菌产品时,需要考虑选择合适的微胶囊技术,以确保益生菌的稳定性和活性。下面这篇应用非常好的结合了微胶囊包埋和冷冻干燥技术,证明菌种经过包埋干燥后仍具有生物活性,为发酵工艺和食品转化等领域开辟新的可能性。1介绍冷冻干燥,也称为冻干是一种非常通用的脱水方法,常用于保存微生物、食物或药物,如蛋白质类药物。它将冷冻和干燥结合在一个独特的操作中,可以创造出高质量的干燥终产品。冷冻干燥通常用于保存微生物培养物,因为它具有不可忽视的优点:储存的方便性和增加邮寄微生物的可能性。此外,制得的产品只需要少量维护,培养基在储存过程中不会受到污染,微生物可以长时间保持活力。然而,众所周知,冷冻干燥技术对微生物至关重要,因为它对微生物的生存能力和生理状态都有负面影响。根据方法和生物体的不同,微生物存活率也各有不同;然而,活力水平明显低于液氮储存 2。观察到的活力下降主要是由于一些不良副作用引起的,例如细胞内冰晶的形成1、敏感蛋白的变性或在此过程中膜脂质的物理状态发生一些不可逆的变化 3,5。为了防止这种影响,通常在冷冻或冷冻干燥前使用脱脂牛奶、蔗糖、甘油、 DMSO 或海藻糖等作为冻干保护物质1,3。据报道,海藻糖在干燥、冷冻、渗透胁迫和热休克等极端环境下对酵母和细菌具有保护作用。这些保护效果与膜的稳定和酶活性的保存有关。关于海藻糖的保护作用,已经报道了几种假设。一些报道认为它的作用是通过多个外部氢键取代参与维持蛋白质三级结构的水分子,另一些报道认为它形成玻璃态结构以确保物理稳定性。除了发酵过程或食品转化,酿酒酵母或乳酸菌等微生物在益生菌膳食食品和饲料补充剂领域具有重要的经济意义。然而,这些应用需要在储存过程中保持细胞活力。通过造粒和冷冻干燥技术相结合,可以得到大小和组成均匀的无尘颗粒。由于具有更高的颗粒表面积,这使得产品将具有良好的颗粒流动性,更容易掌握的剂量和更快的产品复原性。尽管存在上述挑战,冷冻干燥仍然是一种酵母、孢子真菌和细菌的方便保存方法,因为它们的长期生存能力通常保持得相当好,而且菌株的储存和分发要求也很简单。因此,本应用旨在生产酿酒酵母颗粒作为模型微生物,使用微胶囊造粒仪 Encapsulator B-390 作为造粒机,将酵母悬浮液挤压进入液氮中形成单分散球体,然后使用冷冻干燥机 Lyovapor&trade L – 200 进行冷冻干燥处理。2仪器,试剂和器材仪器:ESCO NordicSafe, Biosafety Cabinet Class IIBUCHI 微胶囊造粒仪 Encapsulator B-390BUCHI 冷冻干燥机 LyovaporTM L-200 Pro,干燥腔体搭配可加热搁板BUCHI LyovaporTM Software试剂:YPD 培养基, Sigma Aldrich海藻糖, Sigma Aldrich脱脂奶粉琼脂去离子水液氮器材:玻璃培养皿液氮杜瓦瓶3实验本应用中描述的工作是在无菌条件下进行的。将 84g 市售面包酵母悬浮溶解在 50mL 无菌 YPD 培养基(Sigma Aldrich)中。在酵母悬浮液中加入 50mL 无菌冻干保护剂培养基(5g 海藻糖(Sigma Aldrich)和 5g 脱脂牛奶溶于去离子水中),然后用微胶囊造粒仪 B-390 进行制粒(表1)。将挤压后的液滴收集在液氮浴中冷冻,然后转移到不锈钢托盘中,保存在 -25°C 的冰箱中进行冷冻干燥。表1:微胶囊包埋参数_300μm 喷嘴1mm 喷嘴频率[Hz]68060电压[V]7502500压力[mbar]500500冷冻干燥步骤(初级干燥和次级干燥)使用 LyovaporTM 编程软件,如表 2 所示。使用 LyovaporTM L-200 Pro 干燥腔体、可加热的搁板和环境空气。表2:初级干燥和次级干燥冻干参数无酵母菌微球采用与含酵母菌微球相同成分培养基和参数进行制备。冷冻干燥后,将 1mL 无菌水加入 1mL 微球中,用以复原样品。对于含有酵母菌的菌珠,对每个重组溶液进行10倍、100 倍和 1000 倍的连续稀释。将复原后的溶液和稀释液分别涂于 YPD 琼脂平板上,如图 1 所示。琼脂板在 28℃ 培养 24h,评价细胞活力。▲ 图1:琼脂平板上的酵母活力测试4结果与讨论含有酵母的微球可以通过使用微胶囊造粒仪B-390 进行包埋制备,结果表明:用微胶囊造粒仪 B-390 将酵母滴入液氮中,可使酵母迅速颗粒化;用 300μm 的喷嘴和 1mm 的喷嘴分别制备了 700μm 和 1500μm 左右的微球。仅使用含冻干保护剂介质的溶液也得到了类似的结果。如图 2 所示,冻干后的微球在形状和大小上与湿冻微球保持相似。▲ 图2:用微胶囊造粒仪 B-390 制得的 300μm 酵母微球,在冻干前(左)后(右)的对比通过扫描电镜对其结构进行分析。在图 3 中,可以观察到含有酵母的球珠(下两图)和仅由冻干保护剂培养基制成的球珠(上两图)在形态上的差异。含有酵母菌的微球具有由 5μm 颗粒组成的粗糙结构,可以认为是微生物,而只含有冻干保护剂的微球具有更光滑的结构。▲ 图3:含酵母菌的冻干微球(下)和不含酵母菌冻干微球(上)的结构对比当冷冻干燥时,考虑到膜中脂质物理状态的变化或由于某些蛋白质结构的变化,生物系统可能受到破坏3,9。为了验证酵母菌的活力,将酵母菌重新水合,稀释,并在 28°C 的 YPD 琼脂板上培养 24 小时。图 4 证实了文献报道的内容,即便失去了部分活力,酵母在冻干后仍然可以生长2,4,6,10。▲ 图4:在 28℃ 琼脂板中培养 24 小时后的酵母菌活力5结论含有酵母菌的微粒可以很容易地用微胶囊造粒仪 B-390 进行制备,并使用冻干机 LyovaporTM L-200 进行冷冻干燥处理。B-390 的喷嘴直径分别为300 μm和1000 μm,制得的微粒直径分别为 700μm 和 1500μm。冷冻干燥后,珠粒的大小和形状没有变化。该颗粒流动性好,容易掌握使用剂量,且与水混合后溶解速度快。冻干后的微生物在贮藏过程中仍能保持良好的活力,并能在复水化后成功生长。在本应用中,造粒包埋和冷冻干燥的结合显示出了非常好的实验结果。它可以在发酵工艺和食品转化等领域开辟新的可能性,有利于生产制备剂量易控制和重组的培养发酵剂;另外,在益生菌和食品补充剂领域中获得无尘且可自由流动的粉末,同时保证产品颗粒大小和组成的均匀度。6参考文献N’Guessan, F. K. Coulibaly, H. W. Alloue-Boraud, M. W. A. Cot, M. Djè, K. M. Production of Freeze-Dried Yeast Culture for the Brewing of Traditional Sorghum Beer, Tchapalo. Food Sci. Nutr. 2016, 4 (1), 34–41.Bond, C. Freeze-Drying of Yeast Cultures. In Cryopreservation and Freeze-Drying Protocols Day, J., Stacey, G., Eds. Methods in Molecular BiologyTM Humana Press, 2007 pp 99–107.Leslie, S. B. Israeli, E. Lighthart, B. Crowe, J. H. Crowe, L. M. Trehalose and Sucrose Protect Both Membranes and Proteins in Intact Bacteria during Drying. Appl. Environ.Microbiol. 1995, 61 (10), 3592–3597.Miyamoto-Shinohara, Y. Imaizumi, T. Sukenobe, J. Murakami, Y. Kawamura, S. Komatsu, Y. Survival Rate of Microbes after Freeze-Drying and Long-Term Storage.Cryobiology 2000, 41 (3), 251–255.Wolkers, W. F. Tablin, F. Crowe, J. H. From Anhydrobiosis to Freeze-Drying of Eukaryotic Cells. Comp. Biochem. Physiol. A. Mol. Integr. Physiol. 2002, 131 (3), 535–543.Lodato, P. Huergo, M. S. de Buera, M. P. Viability and Thermal Stability of a Strain of Saccharomyces Cerevisiae Freeze-Dried in Different Sugar and Polymer Matrices. Appl. Microbiol. Biotechnol. 1999, 52 (2), 215–220.Strasser, S. Neureiter, M. Geppl, M. Braun, R. Danner, H. Influence of Lyophilization,Fluidized Bed Drying, Addition of Protectants, and Storage on the Viability of Lactic Acid Bacteria. J. Appl. Microbiol. 2009, 107 (1), 167–177.Miyamoto, T. (Kyushu U. Kawabata, K. Honjoh, K. Hatano, S. Effects of Trehalose on Freeze Tolerance of Baker’s Yeast. J. Fac. Agric. - Kyushu Univ. Jpn. 1996.Giulio, B. D. Orlando, P. Barba, G. Coppola, R. Rosa, M. D. Sada, A. Prisco, P. P. D. Nazzaro, F. Use of Alginate and Cryo-Protective Sugars to Improve the Viability of Lactic Acid Bacteria after Freezing and Freeze-Drying. World J. Microbiol. Biotechnol. 2005, 21 (5), 739–746.Cerrutti, P. Huergo, M. S. de Galvagno, M. Schebor, C. Buera, M. del P. Commercial Baker’s Yeast Stability as Affected by Intracellular Content of Trehalose, Dehydration Procedure and the Physical Properties of External Matrices. Appl. Microbiol. Biotechnol. 2000, 54 (4), 575–580.




 留言咨询
留言咨询
 留言咨询
留言咨询

 留言咨询
留言咨询